Isótopos y masa_atómica-handout
- 1. Documento, adaptado modificado por GAToledo de un material obtenido de la web: Copyright © 2011 Pearson Education, Inc. ISÓTOPOS Y MASA ATÓMICA
- 2. Isótopos Isótopos • son átomos del mismo elemento que tienen diferentes números másicos • tienen el mismo número de protones, pero diferente número de neutrones 2 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 3. Símbolo nuclear Un símbolo nuclear • representa un átomo particular de un elemento • entrega el número másico en la esquina superior izquierda y el número atómico en la esquina inferior izquierda Ejemplo: Un átomo de Magnesio con un número atómico de 12 y un número másico de 24 tiene el siguiente símbolo atómico: 3 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 4. Información del símbolo Nuclear • El símbolo nuclear indica el número de protones (p+), neutrones, (n) y electrones (e-) en un átomo particular. 16 31 65 O P Zn 8 15 30 8 p+ 15 p+ 30 p+ 8 n 16 n 35 n 8 e- 15 e- 30 e- 4 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 5. Chequeo de aprendizaje El Carbono que está presente en la naturaleza consta de tres Isótopos, 12C, 13C, y 14C. Indica el Nº de protones, de neutrones y de electrones en cada uno de los siguientes. 12C 13C 14C 6 6 6 protones neutrones electrones 5 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 6. Chequeo de aprendizaje Escribe los símbolos nucleares para los átomos con las siguientes partículas subatómicas: A. 8 p+, 8 n, 8 e- B. 17 p+, 20 n, 17e- C. 47 p+, 60 n, 47 e- 6 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 7. Chequeo de aprendizaje 1. ¿Cuál de los siguientes pares son Isótopos del mismo elemento? 2. ¿En cuál de los siguientes pares de átomos hay 8 neutrones? A. 15X 15X 8 7 B. 12X 14X 6 6 C. 15X 16X 7 8 7 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 8. Masa atómica La Masa atómica de un elemento • es listada bajo el Símbolo de cada elemento en la tabla periódica • Informa la masa “promedio” de un átomo de cada elemento comparado con la masa del 12C (vea la explicación en la página 17) • No es lo mismo que el número másico 11 Na 22.99 8 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
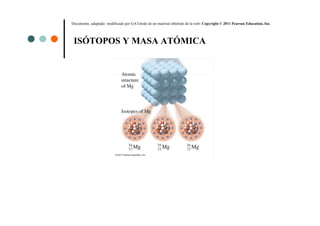
- 9. Isótopos del Magnesio En la naturaleza hay tres isótopos del magnesio. 9 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 10. Ejemplos de Isótopos y sus Masas atómicas Muchos elementos tienen dos o más Isótopos que contribuyen a la Masa atómica de ese elemento. 10 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 11. Cálculo de la Masa atómica Para calcular la Masa atómica se requiere de: • la abundancia en porcentaje(%) de cada isótopo • la Masa atómica de cada isótopo de ese elemento • la suma de los promedios de las masas atómica masa del isótopo(1) x (%) + masa del isótopo(2) x (%) + … 100 100 11 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 12. Masa atómica del Magnesio La Masa atómica del Mg • se debe a todos los isótopos del Mg • es un promedio de las masas atómicas del Mg • no es un número entero 12 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 13. = 23.99 uma x 78.70/100 = 18.88 uma = 24.99 uma x 10.13/100 = 2.531 uma = 25.98 uma x 11.17/100 = 2.902 uma Cálculo de la Masa atómica Isótopo Masa Abundancia G G G 24Mg 25Mg 26Mg Masa atómica (masa promedio) Mg = 24.31 uma Mg 24.31 13 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 14. Chequeo de aprendizaje Usando la tabla periódica, especifica la Masa atómica de cada elemento: A. Calcio B. Aluminio C. Plomo D. Bario E. Hierro 14 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 15. Masa atómica para el Cl • La Masa atómica del cloro es la masa promedio de los dos Isótopos 35Cl y 37Cl. El Cloro, con dos isótopos naturales, tiene una Masa atómica de 35.45. 15 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 16. Cálculo de la Masa atómica del Cl 35Cl tiene una Masa atómica de 34.97 (75.76%) y 37C tiene una Masa atómica de 36.97 (24.24%). • Use la Masa atómica y el porcentaje de cada isótopo para calcular la contribución de cada isótopo a la masa promedio. 34.97 x 75.76 = 26.49 uma 100 35.97 x 24.24 = 8.962 uma 100 35.45 uma • La suma es la masa promedio o Masa atómica del Cl. 35.45 uma 16 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
- 17. Desde 1961, la IUPAC (International Union 0f Pure and Applied Chemistry) acordó utilizar un nuevo patrón: el isótopo del carbono de número másico 12 (que se representa como C12 ó como C-12), al que se le adjudicó la masa atómica exacta de 12 uma. En un principio, se tomaba al hidrógeno como patrón, por su cualidad de ser el elemento más ligero, y se le adjudicó también arbitrariamente el peso unidad. A la masa correspondiente se la denominó «unidad de masa atómica UMA. De esta manera, el que el cloro tenga, por ejemplo, una masa atómica de 35,5, significa que sus átomos son 35,5 veces más pesados que 1/12 del átomo de C12 . En definitiva, hay que considerar que: a) La masa atómica de un elemento es una masa relativa, comparada con la masa de un átomo de C-12. b) La masa atómica de un elemento es, en realidad, el la masa atómica media de todos los isótopos de ese elemento, teniendo en cuenta la cantidad relativa de cada isótopo, tal como se presenta dicho elemento en la naturaleza (abundancia relativa) 17 Departamento de Ciencias, SFC Prof. Gustavo Toledo C.
