Calculos atómicos mecanica cuantica II
- 2. FORMAS Y TAMAÑOS DE LOS ORBITALES Los orbitales s (l=0) tienen forma esférica. La extensión de este orbital depende del valor del número cuántico principal, asi un orbital 3s tiene la misma forma pero es mayor que un orbital 2s.
- 3. FORMAS Y TAMAÑOS DE LOS ORBITALES Los orbitales p (l=1) están formados por dos lóbulos idénticos que se proyectan a lo largo de un eje. La zona de unión de ambos lóbulos coincide con el núcleo atómico. Hay tres orbitales p (m=-1, m=0 y m=+1) de idéntica forma, que difieren sólo en su orientación a lo largo de los ejes x, y o z.
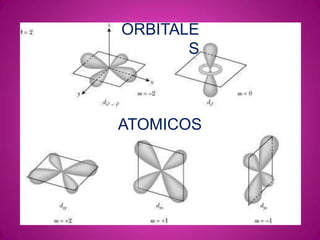
- 4. FORMAS Y TAMAÑOS DE LOS ORBITALES Los orbitales d (l=2) también están formados por lóbulos. Hay cinco tipos de orbitales d (que corresponden a m=-2, -1, 0, 1, 2)
- 5. FORMAS Y TAMAÑOS DE LOS ORBITALES Los orbitales f (l=3) también tienen un aspecto multilobu-lar. Existen siete tipos de orbitales f (que corresponden a m=-3, -2, -1, 0, +1, +2, +3). Tomado de: http://www.eis.uva.es/~qgintro/atom/tutorial-11.html
- 6. LAS ENERGÍAS DE LOS ORBITALES Energías relativas entre subniveles: s < p < d< f Dos factores controlan la energía de un orbital: su tamaño y forma. A mayor tamaño y forma más compleja, requiere más energía.
- 7. CONFIGURACIÓN ELECTRÓNICA Principio de Aufbau: Los electrones se asignan al átomo, uno a la vez, comenzando con el orbital de menor energía, hasta que todos los e estén en el orbital apropiado. Orbitales degenerados: son aquellos que tienen la misma energía, como los orbitales p (px, py, pz ) queaunque con diferenteorientacióntienenigual forma y tamaño. Regla de Hund:se adiciona un ḗ a cada orbital, antes de llenaralguno con dos ḗ. los ḗ se adicionan con el mismo spin hastaquecada orbital degeneradotenga al menos 1 ḗ. N (Z = 7): 1s2 2s2 2p3
- 8. Cuandocomparamos la configuraciónelectrónica de elementos en unamismafila de la tablaperiódica, se encuentraquecorresponden al llenado de un nivel de orbitales. Porejemplo, la segundafilacontieneelementoscuyosorbitales en el niveln = 2 estánllenos.
- 9. Los elementos de un mismogrupotienenconfiguracionessimilaresparasuselectronesmásexternos.
- 10. LAS ENERGÍAS DE LOS ORBITALES http://chemed.chem.purdue.edu/genchem/topicreview/bp/ch6/quantum.html#relative
- 11. ESPECTROS DE EMISIÓN CONTINUO Descomposición de la luzblanca, cada color se debe a unadiferentelongitud de onda de la radiación. DISCONTINUO Descomposición de elementosquímicos en estadogaseoso a altas T, solo emitenalgunas longitudes de onda. http://herramientas.educa.madrid.org/tabla/espectros/spespectro.html
- 12. ESPECTROS DE EMISIÓN El salto de un electrón de una órbita de mayor energía(E2) a otra de menor energía(E1) provoca la emisión de un fotón de energía igual a la diferencia entre los dos niveles energéticos(E2-E1). Para que un electrón salte de una órbita de menor energía(E1) a otra de mayor(E2) es necesario que absorba un fotón con energía igual a la diferencia de energías entre los dos niveles.(E2-E1).
- 13. ESPECTROS DE EMISIÓN Electrón en un nivel de energía superior E2: Estado Excitado Electrón en un nivel de energía inferior E1: Estado Fundamental ƛ Espectro de Emisión
- 14. ESPECTRO DE EMISIÓN DEL HIDRÓGENO http://www.uclm.es/profesorado/jaorganero/subpaginas/apuntes/introduccion_a_la_experimentacion_en_quimica_fisica/practica8.pdf
- 15. Ecuación de Planck Ecuación de Rydberg h = 6,62x10-34 J·s, constante de Planck ν = frecuencia de la radiación RH = 2,18 x 10-18 J
- 16. Ecuación de DeBroglie Las ondas se comportan como partículas, y éstas exhiben propiedades ondulatorias. Ambas propiedades se relacionan con la expresión: h=6,62 10-34 J·s, constante de Planck m= masa de la partícula (e) (Kg) u = rapidez (m/s) http://courses.science.fau.edu/~rjordan/bb_12/answers_12.htm
- 17. TALLER Calcule la Energía en Joules de: Un fotón con ƛ=5x10_4 nm y Un fotón que tiene ƛ=5x10_-2 nm. 2. Cuál es la ƛ (nm) de un fotón emitido durante la transición desde el nivel ni = 5 al nf= 2 en el átomo de Hidrógeno?
- 18. CUESTIONARIO Cuál es la ƛ (nm) de la luz con una ν de 8,6x10_13 Hz? Cuál es la ν, en Hz, de la luz con una ƛ de 566 nm? Calcule la energía en Joules de un fotón con una ƛ = 5x10_4 nm. Cuál es la ƛ (nm) de un fotón emitido durante la transición desde el estado ni = 5 al estadonf = 2 en el átomo de H? Calcule la ƛ asociada a un electrón (9,1094x10_ -31 Kg) que se desplaza a 68 m/s. 5. Cuál es la ƛ de deBroglie, en cm, de un colibrí de 12,4 g que vuela a 1,20x10_2 mph (1 milla = 1,61 Km)