Qyf101 clase a_clase_quimica_general (1)
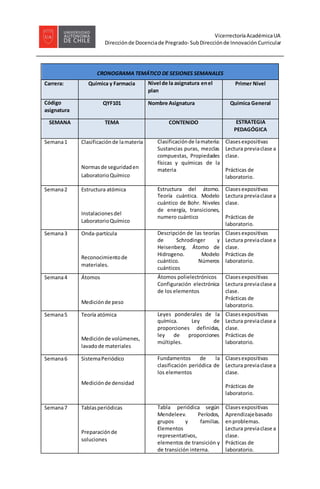
- 1. VicerrectoríaAcadémicaUA Direcciónde Docenciade Pregrado- SubDirecciónde Innovación Curricular CRONOGRAMA TEMÁTICO DE SESIONES SEMANALES Carrera: Química y Farmacia Nivel de la asignatura enel plan Primer Nivel Código asignatura QYF101 Nombre Asignatura Química General SEMANA TEMA CONTENIDO ESTRATEGIA PEDAGÓGICA Semana1 Clasificaciónde lamateria Normasde seguridaden LaboratorioQuímico Clasificaciónde lamateria: Sustancias puras, mezclas compuestas, Propiedades físicas y químicas de la materia Clasesexpositivas Lectura previaclase a clase. Prácticas de laboratorio. Semana2 Estructura atómica Instalacionesdel LaboratorioQuímico Estructura del átomo. Teoría cuántica. Modelo cuántico de Bohr. Niveles de energía, transiciones, numero cuántico Clasesexpositivas Lectura previaclase a clase. Prácticas de laboratorio. Semana3 Onda-partícula Reconocimientode materiales. Descripción de las teorías de Schrodinger y Heisenberg. Átomo de Hidrogeno. Modelo cuántico. Números cuánticos Clasesexpositivas Lectura previaclase a clase. Prácticas de laboratorio. Semana4 Átomos Mediciónde peso Átomos polielectrónicos Configuración electrónica de los elementos Clasesexpositivas Lectura previaclase a clase. Prácticas de laboratorio. Semana5 Teoría atómica Mediciónde volúmenes, lavadode materiales Leyes ponderales de la química. Ley de proporciones definidas, ley de proporciones múltiples. Clasesexpositivas Lectura previaclase a clase. Prácticas de laboratorio. Semana6 SistemaPeriódico Mediciónde densidad Fundamentos de la clasificación periódica de los elementos Clasesexpositivas Lectura previaclase a clase. Prácticas de laboratorio. Semana7 Tablasperiódicas Preparaciónde soluciones Tabla periódica según Mendeleev. Períodos, grupos y familias. Elementos representativos, elementos de transición y de transición interna. Clasesexpositivas Aprendizajebasado enproblemas. Lectura previaclase a clase. Prácticas de laboratorio.
- 2. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana8 Propiedades periódicas de loselementos Sistemasde calefacción Radio atómico, iónico y covalente, volumen, numero de oxidación potencial de ionización, electronegatividad, electroafinidad y series electrónicas. Clasesexpositivas Aprendizajebasado enproblemas. Lectura previaclase a clase. Prácticas de laboratorio. Semana9 Prueba mitad de semestre Semana10 Enlace químico Técnicasde separación Teorías sobre naturaleza de enlace químico. Enlace covalente, covalente coordinado, y enlace iónico Clasesexpositivas Aprendizajebasado enproblemas. Lectura previaclase a clase. Prácticas de laboratorio. Semana11 Teoría de enlacesde valencia Técnicasde separacióny de purificación Notación de Lewis, formación de enlaces simples y múltiples. Regla del dueto y octeto. Excepcionesde moléculas. Clasesexpositivas Aprendizajebasado enproblemas. Lectura previaclase a clase. Prácticas de laboratorio. Semana12 Característicasdel enlace Extraccióncon solvente Energía, longitud, polaridadde enlace yde la molécula, momento dipolar,modelopariónico, orden de enlace, propiedades magnéticas, carga formal, resonancia. Clasesexpositivas Aprendizajebasado enproblemas. Prácticas de laboratorio. Semana13 Enlace covalente Destilaciónsimple Enlace covalente coordinado, formación de aductos. Expansión de capa de valencia Clasesexpositivas Aprendizajebasado enproblemas. Prácticas de laboratorio. Semana14 Estequiometria Titulación Concepto de mol, fórmula empírica, formula molecular. Relación y cálculosestequiométricos. Reactivos en exceso, limitante, rendimiento. Clasesexpositivas Aprendizajebasado enproblemas. Prácticas de laboratorio. Semana15 Soluciones Preparaciónde soluciones Expresión de soluciones. %p/p, %p/v, molaridad, molalidad. Soluto, solvente, densidad. Propiedades coligativas. Clasesexpositivas Aprendizajebasado enproblemas. Prácticas de laboratorio. Semana16 Semana17 Semana18 Prueba término de semestre Nota: Se debenindicarlassesionesdestinadasapruebassolemnesuotrasformasde evaluaciónsumativa. Estas no requierenclase aclase.
- 3. [Escriba aquí] [Escriba aquí] [Escribaaquí] PROGRAMACIÓN CLASE A CLASE Nombre del curso: QUIMICAGENERAL Código:QYF101 Carrera: QUIMICA Y FARMACIA Desarrollode las Sesiones Semana Nº1: Clasificaciónde lamateria Descripción de la Sesión: Clasificaciónde lamateria:Sustanciapuras,mezclascompuestas,Propiedadesfísicasyquímicasde la materia Lectura Previa La químicaesel estudiode lamateriay loscambiosque experimenta.Lamateriaescualquiercosaque ocupa un espacioyque tiene masa.La materiaescualquiercosaque se puede verytocar (comoagua, tierray árboles) ono (comoel aire).Así,cada cosa del universotieneunarelación"química".Losquímicosdistinguen variossubtiposde materiasegúnsucomposiciónypropiedades.Laclasificaciónde lamateriacomprende las sustancias.lasmezclas,loselementosyloscompuestos,asícomolosátomos ylas moléculas,que se estudiaránenel capítulo2, Sustancias y mezclas Una sustanciaes unaforma de materiaque tiene unacomposicióndefinida(constante) ypropiedades características.Algunosejemplossonel agua,el amoniaco,el azúcar(sacarosa),el oroy el oxígeno.Las sustanciasdifierenentre síensucomposiciónypuedenidentificarse porsuapariencia,olor,saboryotras propiedades.Unamezclaesuna combinaciónde dosomás sustanciasenla cual las sustanciasconservansus propiedadescaracterísticas.Algunosejemplosfamiliaressonel aire,lasbebidasgaseosas,laleche yel cemento.Lasmezclasnotienenunacomposiciónconstante,portanto,lasmuestrasde aire recolectadasde variasciudadesprobablementetendránunacomposicióndistintadebidoasusdiferenciasenaltitudy contaminación,entre otrosfactores.Lasmezclaspuedenserhomogéneasoheterogéneas,Cuandouna cucharada de azúcar se disuelveenagua,obtenemosuna mezclahomogénea,esdecir,lacomposiciónde la mezclaesla mismaentoda ladisolución.Sinembargo,si se juntanarenayvirutasde hierropermanecerán como tal.Este tipo de mezclase conoce como mezclaheterogéneadebidoaque sucomposiciónnoes uniforme. Estalecturaincluye losconceptos,definiciones,informaciónovocabulariobásicoparalaclase,lo que debe serpertinente alascaracterísticasde la asignaturao actividaddocente;loque el estudiante deberá tenerpara entenderlaclase.De estamanerapermite que el estudiante puedaparticiparactivamente ensu procesode enseñanza-aprendizaje (lo que leenlespermiteentenderloque el profesorexplicaraenlaclase), dominandolosconocimientospreviosque exigeel nuevotemaoresolverlasdudas. Las sustancias se caracterizanpor sus propiedadesyporsu composición.El color,puntode fusiónypuntode ebulliciónsonpropiedadesfísicas. Lapropiedadfísicase puede mediryobservarsinque cambie la composiciónoidentidadde lasustancia,Porejemplo,esposibledeterminarel puntode fusióndel hielo calentandountrozode él y registrando latemperaturaala cual se transformaenagua.El agua difiere del hielosóloenapariencia,noensu composición,porloque este cambioesfísico;esposible congelarel agua para recuperarel hielooriginal,Portanto,el puntode fusiónde unasustanciaesuna propiedadfísica.De igual manera,cuandose dice que el heliogaseosoesmásligeroque el aire,se hace referenciaa una propiedadfísica.Porotrolado,el enunciado"el hidrógenogaseosose quemaenpresenciade oxígeno gaseosopara formaragua" describe una propiedadquímicadel hidrógeno,yaque para observarla propiedadse debe efectuaruncambioquímico,enese casola combustión.Despuésdel cambio,losgases originales,hidrógenoyoxígeno,habrán desaparecido yquedaráunasustanciaquímicadistinta,el agua.No esposible recuperarel oxígenodel aguapormediode uncambiofísicocomo laebulliciónolacongelación. Cada vezque se prepara unhuevococidose produce un cambioquímico.Al ser sometido aunatemperatura de aproximadamente100°C.,tanto la clara comola yemaexperimentancambiosque modificannosólosu aspectofísico,sinotambiénsucomposición.AIcomerse,cambiaotravezla composicióndel huevopor efectode lassustanciaspresentesenel organismo,denominadasenzimas.Estaacción digestivaesotro ejemplode uncambioquímico.Loque sucede durante ladigestióndependede laspropiedadesquímicas tanto de losalimentoscomode lasenzimasimplicadas.
- 4. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: ¿Qué es una sustancia? ¿Qué es una mezcla homogénea y una heterogénea? ¿Qué es una propiedad física y una propiedad química? Referencia Bibliográfica de la Lectura Previa Raymond Chang y Kenneth A. Goldsby. Química. Undécima edición McGraw-Hill Educación 2015. Capítulo 1 http://www.quimica.ucr.ac.cr/LQG1/laboratorio_quimica_general.pdf, Normas de seguridad de laboratorio Químico: LABORATORIOS DE QUÍMICA GENERAL. Universidad de Costa rica. Guía de experimentos. Pp 1-4.
- 5. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº2: Estructura atómica Descripciónde la Sesión: Estructura del átomo.Teoría cuántica.Modelocuánticode Bohr. Nivelesde energía,transiciones,número cuántico. Lectura Previa Durante el sigloXIX,el descubrimientode laelectrolisisdel agua(1800, NicolsonyCarlisle) yde lasleyesde Faraday (1832) sugierenque lasunidadesde carga eléctricaestán asociadas con los átomos. Peronoes hasta finalesdel sigloXIXyprincipiosdelXXque se identificanlaspartículascargadasque componenel átomo. El protón y el electrónfueronidentificadosestudiandolaconductividadde los gasesa bajas presionespor Goldsteinen1886 y por Thomson en1897, respectivamente. Estudiandoel comportamiento de las partículasfrente a camposeléctricosymagnéticos,se determinóque el protónesuna partícula de carga positiva con una relaciónmasa/carga de 1,04 10-8 kg/C, mientras que el electrónesuna partícula de carga negativa con una relación masa/carga de 5,69 10-12 kg/C. En 1909, Millikanestudialacarga adquirida por una gota de aceite al ser irradiadaconrayos X y propone que launidadelemental de cargaasociadaal electrónyal protónvale 1,60 10-19 C. A partir de este valorde carga y de susrelacionesmasa/carga,se determinaronlasmasasdel electrónyladel protón,siendoésta1835 mayor que aquella(tabla1.1).Al bombardearberilioconpartículasde altaenergía,Chadwickdemostróen1932 que los átomos están constituidostambiénpor partículas sincarga llamadas neutrones,de masa similara la del protón. TEORÍA ATÓMICA DE BOHR. El trabajo de Bohr, girósobre el modelonucleardel átomode Rutherford,enel que el átomose ve como un núcleocompactorodeadoporun enjambre de electronesmásligeros.El modelo de Bohr establece que unátomoemite radiaciónelectromagnéticasólocuandounelectróndel átomosalta de un nivel cuánticoaotro (átomo excitado). NielsBohr impulsolosconceptosde: -Loselectronesse encuentranencapasyque losde laúltimacapa determinanlaspropiedadesquímicasde un átomo. -Loselectronesgiranalrededordel núcleoenestadofísicoyde determinadaenergía,porlocual,al desplazarse atravésde una órbita,noemitenni absorbenenergía. -Un electrónpuede saltarde unnivel de energíaaotro,siempre ycuandoabsorba o desprendalaenergía necesaria. TEORÍA ATÓMICA DE SOMMERFIELD En 1916, ArnoldSommerfieldexpusociertasmodificacionesalateoría de Bohr diciendoque loselectronespodíanviajarenórbitaselípticasycirculares.Ensuteoría, introdujoun parámetro( ℓ ) ℓ=n-1,agregadoal parámetroseñaladoporBohr ( n ).En el modeloatómicode Sommerfield ( n ) esigual a 1, 2, 3, etc.,y laestructura“ele” ( ℓ ) indicael gradoen laque la circunferenciasufre desviaciones.Losvaloresde nyl estáníntimamente relacionados. Reydbergestablecióunareglaconla cual determinael númerode electronesque hayenunórbital “2n2 “, perodespuésdel cuartonivel yanose cumple lareglani tampococon lospolielectrónicos.Enel último orbital solo puede habercomomáximo8electrones. Nivel n = 1 2 ( 1 )2 = 2 Nivel n = 2 2 ( 2 )2 = 8 Nivel n = 3 2 ( 3 )2 = 18 Nivel n = 4 2 ( 4 )2 = 32 El estadoenergéticode unelectrónquedadefinidopordosnúmeros,“n ” y “ ℓ ”. Los términosespectrales s, p,d, f que provienendel espectrodel hidrógeno.Tambiénsugirióque loselectronesenlosmetalesse encuentranenunadisposicióncuánticaenlaque losnivelesde bajaenergíadisponiblesparaloselectrones se hallancasi completamente ocupados. E r Q N M L K .......
- 6. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: ¿Qué esun átomo y comoestá compuesto? ¿Qué esel espectrode emisiónycómose genera? ¿Qué dice la leyde Bohr? ReferenciaBibliográficade la Lectura Previa RaymondChangy KennethA.Goldsby. Química.UndécimaediciónMcGraw-Hill Educación,2015. Capítulo1. La EstructuraElectrónicade losÁtomos.Disponible en: www3.uah.es/edejesus/resumenes/EQEM/tema_193.pdf Instalaciónde laboratorioQuímico. LABORATORIOSDEQUÍMICA GENERAL. Universidadde Costa Rica. Guía de experimentos. Pp1-5.Disponible en: http://www.quimica.ucr.ac.cr/LQG1/laboratorio_quimica_general.pdf
- 7. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº3: Onda-partícula Descripción de la Sesión: Descripciónde lasteoríasde SchrodingeryHeisenberg.Átomode Hidrogeno.Modelocuántico.Números cuánticos Lectura Previa PRINCIPIOO TEORÍA DE LA DUALIDAD El físicofrancés Louis de Broglie en 1924, consideró,que laluznosoloesun efectocorpuscularsinotambién ondulatorio.Ladualidadonda-corpúsculoeslaposesiónde propiedadestantoondulatoriascomo corpuscularesporparte de losobjetossubatómicos. Lateoría de la dualidadde la materia consideraque la materiatiene uncomportamientocorpúsculo-ondaópartícula-onda. = longitudde onda h = constante de Planck m = masa del electrón v = velocidadde lapartícula-onda PRINCIPIODE INCERTIDUMBRE DE HEISENBERG El físicoalemán WernerHeisenbergen1926, expresóque esimposible conocerconpresióny simultáneamentelaposiciónyvelocidaddel electrón,yaque al determinarlavelocidadse alterael valorreal de su posición. ECUACIÓNDE ONDA DE SCHRÖDINGER El físicoaustriaco Erwin Schrödinger en1927, establece larelaciónentrelaenergíade unelectrónyla distribuciónde este enel espaciode acuerdoconsuspropiedadesondulatorias.Propusounaecuaciónque no señalaórbitasdiscretas,sinolaondaasociadaal electrón. Suecuaciónes: ² ² ² ² x² y² z² h² = Derivaciónparcial de lafunciónde onda = (psi) Amplitudde lafunciónde ondadel electrón E = Energía total del sistema v = Energía potencial del sistema m = Masa del electrón h = Constante de Planck (x,y,z) = Coordenadascartesianas Al resolverlaecuaciónde Schrödingerse encontrósoluciónalossiguientesnúmeroscuánticos,con excepcióndel cuartoparámetroque fue agregadopor Dirac: Núm.Cuánt.Principal ( n ).-Define el tamañode lanube electrónica. Núm.Cuánt.Secundarioóazimutal ( ℓ ).-Determinalaformadel órbital. Núm.Cuánt.Magnético ( m ).-Señalalasorientacionesdel órbital. Núm.Cuánt. Spin ( s ).- Indicael girodel electrónylaposición. Si ℓ = 0, n=1 su órbital es s, m es igual 0 y s esigual a +½, -½con 2 e- comomáximo. Si ℓ = 0,1, n=2 su órbital es p, es igual –1,0,+1 y s esigual a +½,-½ con 6 e- como máximo. Si ℓ = 0,1,2, n=3 su órbital es d, es igual –2,-1,0,1,2 y s es igual a +½,-½con 10 e- como máximo. Si ℓ = 0,1,2,3, n=4 su órbital es f,es igual –3,-2,-1,0,1,2,3 y s esigual a +½,-½ con 14 e- comomáximo. Cuandon=5,6,7 son losmismosorbítalesque n=4. TEORÍA CUANTICAYCONFIGURACIÓNELECTRÓNICA La teoríafísica basadaen lautilizacióndel concepto de unidadcuánticaparadescribirlaspropiedades dinámicasde laspartículassubatómicasy lasinteraccionesentre lamateriaylaradiacióny laconfiguración electrónicaesladistribuciónde loselectronesenel átomo,segúnsunúmerocuánticoyatómico,ypor tanto, esla más probable de loselectronesentornoal núcleo.Otradefiniciónpodríaserla organizaciónde los electronesenunátomo,que determinalaspropiedadesquímicasdel mismo. Ej. 22Ti ---1s2 ,2s2 ,2p6 ,3s2 , 3p6 , 4s2 , 3d2 h mV = + + + (E – v) = 0
- 8. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: ¿Qué señala el principio de la incertidumbre? ¿Qué entiende por teoría de la dualidad? ¿En qué se basa la teoría cuántica para definir las propiedades dinámicas de las partículas? Referencia Bibliográfica de la Lectura Previa CHANG, Raymond y GOLDSBY, Kenneth A. Química. Undécima edición. McGraw-Hill Educación 2015. Capítulo 1. La EstructuraElectrónicade losÁtomos.Disponible en: www3.uah.es/edejesus/resumenes/EQEM/tema_193.pdf LABORATORIOS DE QUÍMICA GENERAL. Universidad de Costa rica. Guía de experimentos. Pp. 14-17.
- 9. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº4: Átomos Descripción de la Sesión: Átomos polielectrónicos. Configuración electrónica de los elementos Lectura Previa Los átomos polielectrónicos.La ecuaciónde Schrodingeresirresoluble de formaexactapara átomos de más de un electrón, y no es por su complejidad, pues lo son siempre las ecuaciones, por sencillas que sean, de cualquier sistema físico de más de dos partículas interaccionando entre sí, por ejemplo, Sol -Tierra-Luna. Situando el Sol en el centro de coordenadas, la irresolubilidad es debida a que no es posible separar las coordenadasque definenlatrayectoriade laTierrade aquéllasquedefinenlade laLuna,puesambasse afectan mutuamente.Enotraspalabras,no se puede conocerlatrayectoriade la Tierrasinconocer previamentelade laLuna y viceversa.Unaformade obtenerunasolución,aunqueaproximada,esdespreciaralgunainteracción. Así se puede obteneruna trayectoriaaproximadade la Tierra alrededordel Sol despreciandolainfluenciade la Luna, y la de la Luna alrededor de la Tierra despreciando la del Sol.Obsérvese que se ha transformado un problema irresoluble de tres partículas (Sol-Tierra-Luna) en dos problemas resolubles, pero aproximados, de dos partículas (Sol-Tierra y Tierra-Luna). La aproximación orbital.Enunátomopolielectrónico,el segundoelectrónysiguientesintroducenlarepulsión entre electrones,ausente enel átomode hidrógeno.Laaproximaciónorbital esunmétodode resoluciónque consiste en despreciar las repulsiones interelectrónicas (recuadro 1.8), con lo que los el ectrones se independizan unos de otros, comportándose cada uno de ellos tal como lo haría en un sistema monoelectrónico de carga nuclear Z. Por esta vía, el problema irresoluble de un átomo con n electronesse convierte en n problemas resolubles de 1 sólo electrón, cuyas soluciones conocemos ya, son los orbitales atómicos hidrogenoides. El resultado es que el estado de un átomo polielectrónico se aproxima mediante la superposición de estados individuales de los electrones u orbitales atómicos, y la energía total mediante la suma de las energías de cada uno de dichos estados monoelectrónicos. El nombre de aproximación orbital procede, por tanto, de que introduce en los átomos polielectrónicos la idea de orbital como estado de un electrón en el átomo. Ahora bien, un orbital atómico del hidrógeno es una solución exacta de la ecuación de ondasque representaunode losestadosde energíaen que puede estarel átomo debidoasu único electrón. Un orbital en un átomo polielectrónico representa el estado de energía de uno de sus electrones, y es el resultado de una aproximación,que desprecia las repulsiones interelectrónicas y permite hablar en términos de electrones independientes. Configuraciones electrónicas de los átomos polielectrónicos en su estado fundamental. Orden de llenadode orbitales.Para cada tipode orbital y como consecuenciade sudiferente penetración,la carga nuclearefectivaque sobreél ejerceel núcleoysuenergíavaríande formadistintaal aumentarel número atómico (figura 1.19). A veces, se altera el orden relativo de sus energías y, por tanto, el de su llenado. Generalmente, pero no siempre, los orbitales se llenan en el orden 1 s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p <7s < 5f < 6d <7p ... Regla de Hund(primeraversión)."Para unaconfiguracióndada,el estadomásestableesaquél conel máximo número de electrones desapareados" Configuraciones electrónicas. Las reglas anteriores predicen correctamente las configuraciones electrónicas experimentales de los átomos polielectrónicos en su estado fundamental (tabla 1.10), salvo las excepciones entre los metales de transición detalladas a continuación: • Muchos casos se pueden justificar por la pequeña diferencia de energía entre los orbitales (n-1)d y ns: • El trasvase de electrones del orbital ns al (n-1)d puede verse favorecido por la estabilidad de las configuraciones esféricas (estados con todos los subniveles completos, completos a mitad o vacíos): • Razonamientossimilaresse puedenhaceren lantánidosyactínidosparaexcepcionesanálogascon orbitales (n —2)f y (n —1)d. • Al formar cationes, los electrones se sacan primero de los orbitales np, luego ns y finalmente (n —1)d.
- 10. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: ¿Cómo se puede resolver los problemas de interacciones múltiples? ¿En qué se basa la aproximación orbital de interacciones entre átomos? ¿Cómo se llenan las distintas capas de orbitales electrónicos? Referencia Bibliográfica de la Lectura Previa CHANG, Raymond y GOLDSBY, Kenneth A. Química. Undécima edición. McGraw-Hill Educación 2015. Capítulo 1. La EstructuraElectrónicade losÁtomos.Disponible en: www3.uah.es/edejesus/resumenes/EQEM/tema_193.pdf LABORATORIOS DE QUÍMICA GENERAL. Universidad de Costa rica. Guía de experimentos. Pp. 13-17; 23.
- 11. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº5: Teoría atómica Descripción de la Sesión: Leyesponderalesde laquímica.Leyde proporcionesdefinidas,leyde proporciones múltiples. Lectura Previa Un primeraspectodel conocimientoquímicofue conocerlarelaciónentre lascantidadesde loscuerposque intervienenenunareacciónpasandode lomeramente cualitativoalocuantitativo.El descubrimientode la balanzay su aplicaciónsistemáticaal estudiode lastransformacionesquímicaspor LAVOISIERdiolugaral descubrimientode lasleyesde lascombinacionesquímicasyal establecimientode laquímicacomociencia. Ley de la conservaciónde la masa (o de Lavoisier).:La masade un sistema permanece invariablecualquiera que sea la transformaciónqueocurra dentro de él; estoes,en términosquímicos, lamasade loscuerpos reaccionanteses igual a la masade losproductosde la reacción. Esta leyse consideraenunciada por LAVOISIER.Unensayorigurosode estaleyfue realizadopor LANDOLTen1893-1908, no encontrándose diferenciaalgunaenel pesodel sistemaantesydespuésde verificarse lareacción,siempre que se controlen todoslosreactivosy productos (Fig1:inicioreacción;Fig2: ocurre reacción;Fig3 terminode reacción). La leyde laconservaciónde la materiano esabsolutamenteexacta.Lateoría de la relatividaddebida a EINSTEIN ha eliminadoel dualismoexistente enlafísicaclásicaentre lamateriaponderable ylaenergía imponderable.Enlafísicaactual,la materiay la energíasonde lamismaesencia,puesnosólolaenergía tiene unpeso,ypor tanto unamasa, sinoque lamateriaes unaforma de energíaque puede transformarse enotra forma distintade energía.La energíaunidaa una masamaterial esE = mc2 endonde E es laenergía, m la masa y c la velocidadde laluz.Enuna transformaciónde masaenenergíao recíprocamente,larelación entre ambasvariacioneses,análogamente, ΔE=Δm.c2 . La relaciónentre masay energíada lugar a que la ley de la conservaciónde lamateriay laleyde la conservaciónde laenergíano seanleyesindependientes,sino que debenreunirse enunaleyúnicade laconservaciónde lamasa-energía. Ley de las proporciones definidas (o de Proust). Cuando dos o más elementos se combinan para formar un determinado compuesto lo hacen en una relación en peso constante independientemente del proceso seguidoparaformarlo. Estaleytambiénse puedeenunciardesde otropuntode vista:Paracualquiermuestra pura de undeterminadocompuestoloselementos que loconforman mantienenunaproporciónfijaen peso, es decir,unaproporciónponderal constante. Así,porejemplo,enel agualosgramosde hidrógenoylosgramos de oxígenoestánsiempre enla proporción1/8, independientemente del origendel agua. El francés PROUST, en 1801, quien generalice el resultado enunciando la ley a la que da nombre. Ley de las proporcionesmúltiples (ode Dalton). Las cantidadesde un mismoelemento que se unen conuna cantidadfijade otro elemento para formaren cadacaso un compuestodistintoestánen larelaciónde númerosenteros sencillos. La leyde Proustnoimpide que dosomás elementosse unanenvariasproporcionespara formar varios compuestos.Así,porejemplo,el oxígenoyel cobre se unenendosproporcionesyformandos óxidos de cobre que contienen79,90 % y88,83 % de cobre.Si calculamoslacantidadde cobre combinado con un mismopesode oxígeno,tal como1g, se obtiene encadacaso: Las dos cantidadesde cobre son,muyaproximadamente,unadoble de laotray,por tanto, lospesosde cobre que se unencon un mismopesode oxígenoparaformar losdosóxidosestánenlarelaciónde 1 esa 2.
- 12. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: ¿Qué dice la primera ley de Lavoisier? ¿A qué se refiere la ley de proporciones definidas? ¿Cómo explica la ley de proporciones mútiples? ReferenciaBibliográficade la Lectura Previa Las Leyesy PonduralesVolumétricas.Disponible en:encina.pntic.mec.es/jsaf0002/p31.htm LABORATORIOSDE QUÍMICA GENERAL. Universidadde Costarica.Guía de experimentos.Pp18-19
- 13. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº6: SistemaPeriódico Descripción de la Sesión: Fundamentosde laclasificaciónperiódicade loselementos Lectura Previa La tablao sistemaperiódico,esel esquemade todosloselementosquímicosdispuestosporordende númeroatómicocreciente yenunaforma que reflejalaestructurade loselementos.Subase esla"Ley Periódica", lacual establece que laspropiedadesfísicasy químicas de los elementostiendenarepetirse de forma sistemática conforme aumenta el número atómico. Todos loselementosde un grupo presentanuna gran semejanzay,por lo general,difierende loselementosde losdemásgrupos. JohnA. R. Newlandsintentóclasificarloselementosporordende masasatómicascrecientes,observandoque después de cada intervalo de siete reaparecían las mismas propiedades químicas (es decir que el octavo elementoteníapropiedadessimilaresalas del primero). Porsu analogía con la escala musical,laclasificación fue llamada "ley de las octavas" Li 6,9 Be 9,01 B 10,81 C 12,01 N 14 O 15.99 F 18,99 Na 22,98 Mg 24,31 Al 26,98 Si 28,08 P 30,97 S 32 Cl 35,45 K 39,01 Ca 40,08 En las columnas que resultan de la clasificación de Newlands se observa la presencia de los elementos pertenecientesaunamismatríada (Li,Na y K).Se deduce que a partir del Li,el elementode númerode orden igual a 8 es el Na que tiene propiedades similares. Lo mismo ocurre con el Be (berilio), que presenta propiedades químicas similares al Mg (magnesio); con el B (boro) y el Al (aluminio), y así sucesivamente. TABLA PERIÓDICA DE MENDELEIEV La leyquímica que afirmaque laspropiedadesde todoslos elementossonfuncionesperiódicasde susmasas atómicasfue desarrolladaindependientemente pordosquímicos: por el ruso Dimitri Mendeléievyel alemán Julius Lothar Meyer. En 1869, Mendeleievse propusohallaruna"leyde lanaturaleza",válidaparatodaclasificaciónsistemáticade loselementos.Clasificótodosloselementosconocidosensuépocaenordencreciente de suspesosatómicos, estableciendounarelaciónentre ellosysuspropiedadesquímicas. Ensuclasificación,Mendeleievnoconsideró el hidrogeno ni lade los gasesnobles,porquenohabíansidodescubiertosaun.Laleyperiódicade Mendeleiev puede ser enunciada del siguiente modo: "Las propiedades químicas y la mayoría de las propiedades físicas de los elementos son función periódica de sus pesos atómicos". El alemán Lothar Meyer propuso una clasificación de los elementos relacionando los pesos atómicos con las propiedades físicas, tales como el punto de fusión, de ebullición, etc. La clave del éxitode losesfuerzosde MendeléievyMeyerfue comprenderque losintentosanterioreshabían falladoporque todavía quedaba un cierto número de elementospordescubrir, y había que dejarlos huecos para esoselementosenlatabla.Porejemplo,aunque noexistíaningúnelementoconocidohastaentoncescon unamasaatómicaentre ladel calcioyladeltitanio,Mendeléievledejóunsitiovacante ensusistemaperiódico. Este lugarfue asignadomástarde al elementoescandio,descubiertoen1879,que tiene unaspropiedadesque justifican su posición en esa secuencia. El descubrimiento del escandio sólo fue parte de una serie de verificaciones de las prediccionesbasadas en la ley periódica, y la validación del sistema periódico aceleró el desarrollo de la química inorgánica. La primerarevisión de latabla extendióel sistemaparaincluirelementoscuyaexistenciaeracompletamente insospechadaenel sigloXIX.Este grupocomprendíalostresprimeroselementosde losgasesnoblesoinertes, argón, helioyneón,descubiertosenlaatmósferaentre 1894 y 1898 por el físicobritánicoJohnWilliamStrutt y el químicobritánicoWilliamRamsay.El segundoavance fue la interpretaciónde lacausa de la periodicidad de los elementos en términos de la teoría de Bohr (1913) sobre la estructura electrónica del átomo. A esta teoría se la llamó: TEORÍA DE LA CAPA ELECTRÓNICA.
- 14. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: ¿En qué se basa la “Ley periódica”? ¿Qué predice la Ley de Mendeleiev? ¿Por qué había que dejar espacios en la tabla periódica de acuerdo a Mendeleiev y Meyer? Referencia Bibliográfica de la Lectura Previa LABORATORIOS DE QUÍMICA GENERAL. Universidad de Costa rica. Guía de experimentos. Pp 38-44
- 15. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº 7: Tablas Periódicas Descripción de la Sesión: Tabla periódicasegún Mendeleiev.Períodos,gruposy familias.Elementosrepresentativos,elementosde transiciónyde transicióninterna. Lectura Previa TEORÍA DE LA CAPA ELECTRÓNICA En la clasificaciónperiódica, los gases nobles, que no son reactivos en la mayoría de los casos (valencia = 0), estáninterpuestosentre ungrupode metalesaltamente reactivosque formancompuestosconvalencia+1 y un grupo de no metales también muy reactivos que forman compuestos con valencia -1. Este fenómeno condujo a la teoría de que la periodicidad de las propiedades resulta de la disposición de los electronesen capas alrededordel núcleoatómico.Segúnlamismateoría,losgasesnoblessonporlogeneral inertesporque sus capas electrónicas están completas; por lo tanto, otros elementos deben tener algunas capas que están sóloparcialmente ocupadas,ysusreactividadesquímicasestánrelacionadasconloselectronesde esascapas incompletas. Por ejemplo, todos los elementos que ocupan una posición en el sistema inmediatamente anteriora ungas inerte,tienenunelectrónmenosdelnúmeronecesarioparacompletarlascapasypresentan una valencia -1 y tienden a ganar un electrón en las reacciones. Loselementosquesiguenalosgasesinertesenlatablatienenunelectrónenlaúltimacapa,ypuedenperderlo en las reacciones, presentando por tanto una valencia + 1. Un análisis del sistema periódico, basado en esta teoría, indica que la primera capa de electrones puede contener un máximo de 2 electrones, la segunda un máximo de 8, la tercera de 18, y así sucesivamente. El número total de elementos de cualquier periodo corresponde al número de electrones necesarios para conseguir una configuración estable. La diferencia entre los subgrupos A y B de un grupo dado también se puede explicar sobre la base de la teoría de la capa de electrones. Ambos subgrupos son igualmente incompletos en la capa exterior, pero difieren entre ellos en las estructuras de las capas subyacentes. Este modelo del átomo proporciona una buena explicación de los enlaces químicos. TEORÍA CUÁNTICA El desarrollo de la teoría cuántica y su aplicación a la estructura atómica, enunciada por el físico danés Niels Bohr y otros científicos, ha aportado una explicación fácil a la mayoría de las características detalladas del sistema periódico. Cada electrón se caracteriza por cuatro números cuánticos que designan su movimiento orbital enel espacio.Pormediodelasreglasde selecciónquegobiernanesosnúmeroscuánticos,ydelprincipio de exclusión de Wolfgang Pauli, que establece que dos electrones del mismo átomo no pueden tener los mismos números cuánticos, los físicos pueden determinar teóricamente el número máximo de electrones necesario para completar cada capa, confirmando las conclusiones que se infieren del sistema periódico. TIPOS DE TABLA Cada autor siente la tentación de dibujar una tabla donde, según él, se manejan mejor los conceptos de periodicidadquímica. Las tablas más importantes son las que comúnmente se conocen como: “Tabla corta”, “Tabla larga” y “Tabla larga extendida”, sin embargo es la tabla larga la que más se conoce Tabla larga Modificaciónmuyútil,quetambiénsueleserconocidacomo tablade Both.Se construye de tal forma que reflejalateoría de Both sobre la distribuciónelectrónica.Enlas verticalesse encuentran los elementos cuya distribución electrónica final es coincidente, en esencia la tabla larga deriva de la original de Mendeleiev, extendiendo los períodos largos (cuarto, quintoysexto) ycortandoendoslosperíodoscortosparaacomodarenel medioalasseries de loselementosde transición.Asíse generanperíodoslargosperosoloa partirdel cuarto período. En el sistemaperiódicolargo,cadaperiodocorresponde ala formaciónde una nuevacapa de electrones.Los elementos alineados tienen estructuras electrónicas estrictamente análogas. El principio y el final de un periodo largo representan la adición de electrones en una capa de valencia; en la parte central aumenta el número de electrones de una capa subyacente.
- 16. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: Según la teoría de capa electrónica, ¿qué característica especial poseen los gases inertes? ¿Qué ventajas posee la teoría cuántica con respecto a la de capas? ¿Por qué nace la tabla larga? Referencia Bibliográfica de la Lectura Previa LABORATORIOS DE QUÍMICA GENERAL. Universidad de Costa rica. Guía de experimentos. Pp 53-57; 63-68
- 17. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº8: Propiedades Periódicas de loselementos Descripción de la Sesión: Radioatómico,iónicoycovalente,volumen,numerode oxidaciónpotencial de ionización, electronegatividad,electroafinidadyserieselectrónicas. Lectura Previa La tablaperiódicaconstade sub-partesque nosayudana entenderlasdistintaspropiedades que posee cada unode suselementos. Podemosencontrarymedirladistanciaentre losnúcleosenunamolécula.Se pude deducirel radiode un catióno un anión.Podemosdeducirlahabilidaddelátomode cadaelementopara atraer loselectronesde unenlace químico.Se puede sacarel cambiode energíacuandoun átomoacepta un electrónenestadogaseoso.Ylamínima energíaque se requiere paraquitarunátomo gaseosoensu estado fundamental. I.- Radio Atómico: El radio atómico de un metal es la mitad de la distancia entre dos núcleos de dos átomos adyacentes Para elementos que existen como moléculas diatómicas simples, el radio atómico es la mitad de la distancia entre los núcleos de los dos átomos en una molécula especifica A mayor carga nuclear efectiva,los electrones estarán más fuertemente enlazadosal núcleo y menor será el radioatómico.Considérese elsegundoperíodode elementosdel Li al F.Al desplazarsede izquierdaaderecha, se encuentra que el número de electrones de la carga interna permanece constante, mientras que la carga nuclear aumenta. Los electrones que se agregan para balancear la creciente carga nuclear efectiva aumenta constantemente mientras que el número cuántico principal permanece constante. (n= 2). A medida que aumentalacarga nuclearefectiva,el radioatómicodisminuye constantementedel litioal flúor. A medidaque se desciendeenungrupo- por ej.,el grupo 1A- se encuentraque el radioatómico aumentasegúnaumentael número atómico. II.- Radio Iónico: El Radio iónico es el radio de un catión o de un anión. El radio iónicoafectalas propiedadesfísicasyquímicas de un compuesto iónico. Por ej., la estructura tridimensional de un compuesto iónico depende del tamaño relativode suscationesyaniones. Cuandounátomoneutrose convierte enunion,se esperaun cambioenel tamaño. Si el átomo forma un anión, su tamaño (o radio) aumenta, dado que la carga nuclear permanece constante perolarepulsiónresultantede laadiciónde electrón(es)extiendeel dominiode lanube electrónica. Por otro lado,un catión es más pequeñoque suátomo neutro,dadoque quitaruno o más electronesreduce la repulsión electrón-electrón y se contrae la nube electrónica. III.- Electronegatividad:La electronegatividadnos permite distinguir entre elementos covalentes e iónicos. Un enlace covalente,esel compartimientode unpar de electronesentre dosátomos.Enuna moléculacomo el H donde losátomossonidénticos,se esperaque loselectronesseanigualmente compartidos;estoes,los electronespasanlamismacantidadde tiempoenla vecindadde cada átomo.A pesarde que losátomosde H y F también están unidos por un enlace, el compartimiento del par de electrones pasa más tiempo en la vecindad de un átomo que del otro. En tal caso, el enlace covalente se denomina enlace covalente polar, o simplemente un enlace polar. Una propiedad que ayuda a distinguir el enlace covalente puro del polar es la electronegatividad de los elementos, es decir, la habilidad de un átomo para atraer hacia sí los electrones de un enlace químico. La electronegatividadde unelemento estárelacionadaconunaafinidadysuenergíade ionización(queveremos más adelante). En cada grupo,la electronegatividaddisminuye al aumentarel númeroatómico,indicandoun aumento en el carácter metálico. Nótese que los metales de transición no siguen estas tendencias. Los elementos más electronegativos (los halógenos, oxigeno, nitrógeno y azufre) están ubicados en el ángulo superiorderechode latablaperiódica,ylosmenoselectronegativos(losmetalesalcalinosyalcalinoterreos) se encuentran el ángulo inferior izquierdo. IV.- Electroafinidad (Afinidad electrónica) Otra de las propiedades de los átomos que influye en su comportamiento químico es su habilidad para aceptar uno o más electrones. Esta habilidad se mide por la AfinidadelectrónicaoElectroafinidad,lacual esel cambio de energía cuando un átomo acepta un electrón en estado gaseoso.
- 18. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio ¿Qué entiende por radio atómico? ¿Explique lo que entiende por radio iónico ¿Qué entiende por electronegatividad de los átomos? Referencia Bibliográfica de la Lectura Previa LABORATORIOS DE QUÍMICA GENERAL. Universidad de Costa rica. Guía de experimentos. PP. 6-12.
- 19. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº10: Enlace Químico Descripción de la Sesión: Teorías sobre naturalezade enlace químico.Enlace covalente,covalentecoordinado,yenlace iónico Lectura Previa Enlace covalente Los primerosconceptosde launióncovalente surgieronde este tipode imagende la moléculade carbonoe hidrógeno.El enlace covalenteestáimplícitoenla estructurade Lewisindicandoelectronescompartidosentre losátomos. Un enlace covalente entre dosátomos se produce cuandoestosátomosse unen,para alcanzar el octetoestable,compartiendo electrones delúltimonivel1 (excepto el Hidrógeno que alcanzalaestabilidadcuandotiene2electrones).Ladiferencia de electronegatividad entre losátomosnoeslosuficientementegrande comoparaque se produzcauna uniónde tipoiónica.Para que unenlace covalente se genereesnecesarioque ladiferenciade electronegatividadentre átomosseamenora1,7. De estaforma,losdos átomoscompartenunoo más pareselectrónicos enunnuevotipode orbital, denominado orbital molecular.Losenlacescovalentesse producenentre átomosde unmismoelementono metal y entre distintoselementosnometales. Cuandoátomosdistintosde nometalesse unenenunaformacovalente, unode ellosresultarámás electronegativoque el otro,porloque tenderáaatraer la nube electrónicadel enlace haciasunúcleo, generandoun dipoloeléctrico.Estapolarizaciónpermiteque lasmoléculasdel mismocompuestose atraigan entre sí por fuerzaselectrostáticasde distintaintensidad. En síntesis,enun enlace iónico,se produce latransferenciade electronesde unátomoa otro y enel enlace covalente,loselectronesde enlace soncompartidosporambosátomos.Enel enlace covalente, losdos átomosno metálicoscompartenunoomás electrones,esdecir,se unenatravésde sus electronesenel últimoorbital,el cual depende del númeroatómico encuestión.Entre losdosátomospuedencompartirse uno,dos o tresparesde electrones,locual dará lugara la formaciónde un enlace simple,doble otriple respectivamente.Enlaestructurade Lewis,estosenlacespuedenrepresentarse porunapequeñalíneaentre losátomos. Distintostipos de enlacescovalentes Enlace covalente simple. Enlace simple:esunpar electrónicocompartidoformadoporun electrónpertenecienteal últimonivel de energíade cadaátomoy se representaconuna línea.Ejemplos:H-H,Cl-Cl Enlace doble:Formadopor dospareselectrónicoscompartidos,esdecirpordos electrones pertenecientesal últimonivel de energíade cada átomoy se representacondoslíneas paralelas.Ejemplo:O=O Enlace triple:Formadopor trespareselectrónicoscompartidos,esdecirportreselectrones pertenecientesal últimonivel de energíade cada átomoy se representacontreslíneas paralelas.Ejemplo:N≡N Enlace covalente dativo o de coordinación: Es un par electrónicocompartidopordosátomosperoambos electronessonaportadosporel mismoátomo.Se suele representar conuna flecha(→). Un ejemplode unaespecie químicaque poseeunenlace coordinado,el cual esel ion amonio(NH4 1+ ).El Ion amonioestáconstituidoporunprotóny amoniaco.Los compuestosenlosque se encuentraunenlace coordinadose conocencon el nombre de compuestosde coordinación.LosCompuestosde coordinacióno tambiéndenominadoscomplejos,loscualesensumayoríade loscasos estánunidosa variosaniones circundantes conocidoscomo ligandos. Preguntas de inicio: ¿Qué entiende por enlace covalente? ¿Qué es enlace simple, doble o triple? ¿Qué es un enlace de coordinación?
- 20. [Escriba aquí] [Escriba aquí] [Escribaaquí] Referencia Bibliográfica de la Lectura Previa PUERTAS, Ana Alejandra. Enlaces químicos. Documento de la Organización de Estados Iberoamericanos. Disponible en: campus-oei.org/fpciencia/art08.htm LABORATORIOSDE QUÍMICA GENERAL. Universidadde Costarica.Guía de experimentos. PP.20-26.
- 21. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº11: Teoría de enlacesde valencia Descripción de la Sesión: Notaciónde Lewis,formaciónde enlacessimplesymúltiples.Regladel duetoyocteto.Excepcionesde moléculas. Lectura Previa ESTRUCTURAS DE LEWIS, REGLA DEL OCTETO. Lewisfue unode losprimerosenintentarproponerunateoría para explicarel enlace covalente,porellocreonotacionesabreviadasparaunadescripciónmásfácil de las unionesatómicas,que fueronlasestructurasde Lewis. Regladel octeto:“Cuandose formaun enlace químico losátomosreciben,cedenocompartenelectronesde tal formaque la capa más externade cada átomo contenga ocho electrones,yasí adquiere laestructuraelectrónicadel gasnoble máscercanoen el sistema periódico”. Ideas básicas: 1) Los electrones, especialmente los que están en la capa más externa (capa de valencia), jueganun papel fundamental en el enlace químico. 2) En algunoscasosse transfieren electronesde unátomoaotro,formándose ionespositivosynegativosque se atraen entre sí mediante fuerzas electrostáticas denominadas enlaces iónicos. 3) En otros casos se comparten entre los átomos uno o más pares de electrones, esta compartición de electrones se denomina enlace covalente. 4) Los electrones se transfieren o se comparten de manera que los átomos adquieren una configuración electrónica especialmente estable. Generalmente se trata de una configuración de gas noble con ocho electrones más externos que constituyen un octeto. Símbolos de Lewis y estructuras de Lewis. Un símbolo de Lewis consiste de unsímbolo químicoque representael núcleoyloselectronesinternosde un átomo, junto con puntos situados alrededor del símbolo representando a los electrones más externos (electronesde lacapa de valencia).Asíel símbolo de Lewisparael silicioque tienelaconfiguración[Ne]3s2 3p2 es: para escribir los símbolos de Lewis se sitúan puntos solitarios en los lados del símbolo hasta un máximo de cuatro y luegose vanpareandohastaformarun octeto.Lossímbolosde Lewisse escribenhabitualmentepara los elementos de los grupos principales y en raras ocasiones para los elementos de transición. Para los elementos de los grupos principales el número de electrones de valencia y por ende el número de puntos que aparecen en un símbolo de Lewis es igual al número del grupo en la tabla periódica. Una Estructura de Lewis es una combinación de símbolos de Lewis que representa la transferencia o compartición de electrones en un enlace químico. Método para escribir estructuras de Lewis: ENLACE COVALENTE SIMPLE, DOBLE Y TRIPLE La comparticiónde un parde electronesentre átomosenlazadosdalugara un enlace covalente simple. Par enlazante ↓ Formaciónde una moléculade H2 La compartición de dos pares de electrones entre átomos enlazados da lugar a un enlace covalente enlace covalente doble. Dos paresenlazantes ↓ Formaciónde una moléculade O2
- 22. [Escriba aquí] [Escriba aquí] [Escribaaquí] Cada átomo de O tiene 6 electrones, la única manera de que cada átomo cumpla octeto es que cada átomo comparta dos pares de electrones con el otro átomo, lo que da origen a un enlace covalente doble. La comparticiónde tres pares de electronesentre átomos enlazadosdalugara un enlace covalente triple. Tres pares enlazantes ↓ Formación de una molécula de N2 El enlace covalentetripledelN2 esunenlace muyfuerte,difícil de romperen una reacciónquímica.La excepcional fuerzade este enlace hace que el N2 (g) seabastante inerte.Debidoaello,el N2 (g) coexiste conel O2 enlaatmósfera y solamente se formanóxidosde nitrógenoencantidadesde trazas a altas temperaturas. La falta de reactividad del N2 hacia el O2 es una condición esencial para la vida en la tierra. Enlace covalente coordinado: El par electrónico compartido es aportado sólo por uno de los átomos. El átomo que aporta el par electrónico se denomina “dador” y el que lo recibe “aceptor”. Formación del ion amonio Preguntas de inicio: ¿Cuáles son las ideas básicas de la notación de Lewis? ¿Cómo explica la notación de Lewis para los elementos? ¿Cómo explica la formación de los enlaces de coordinación? Referencia Bibliográfica de la Lectura Previa GARCÍA, Begoña. PRÁCTICA 5: Extracción líquido-líquido. Separación, purificación e identificación de mezclas binarias de especies orgánicas desconocidas. Cromatografía de capa fina (CCF). Disponible en: https://capitanswingysanlamuerte.files.wordpress.com/2015/04/extraccion-liquido-liquido.pdf
- 23. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº12: Característicasdel enlace Descripción de la Sesión: Energía, longitud,polaridadde enlace yde lamolécula,momentodipolar,modelopariónico,ordende enlace,propiedadesmagnéticas,cargaformal,resonancia Lectura Previa Las fuerzasde atracción que unena losátomosen loscompuestos,se llamanenlacesquímicos.Al acercarse dos átomos,suselectronesse redistribuyenminimizandoel potencialenlanuevasituación:losátomosse enlazansi laenergíaalcanzada esinferiorala que teníanpor separado.Losdos modelosextremosde redistribuciónde electronessonel iónicoyel covalente,perolamayoríade enlacesse describenmejor considerandounamezclade ambos. El enlace iónicose estabilizaporlaatracción entre lascargas opuestasde cationesyaniones.Ningúnenlace espuramente iónico.Enloscompuestosiónicos(aquellosformadosporenlacesprincipalmente jónicos)cada iontiende arodearse del mayornúmeroposible de ionesde cargacontraria,resultandoque,encondiciones normales,son sólidosconcationesyanionesalternándose enunaredtridimensional.Estudiaremosel enlace iónicomediante parescónicos,unmodelosimple,aunque ficticio,formadoporatracciónentre uncatión y un anión.La formaciónde un enlace iónicoesfavorablesi laenergíanecesariaparaionizarlosátomoses compensadaporla energíaliberadaporlasatraccioneselectrostáticasentre catiónyanión,loque esmás fácil cuandoreaccionanátomosde bajas energíasde ionizaciónconátomosde altasafinidadeselectrónicas. Carga formal.La carga formal de unátomo enuna moléculase asignaasumiendoque cadaátomove compensadasucarga nuclearporuno de loselectronesde cadaunode susparesde enlace (de acuerdocon un igual compartimiento) yporlosdoselectronesde cadaunode susparessolitarios(que sólole pertenecen a él).La experienciaindicaque lasestructurasde Lewismásestablessonnormalmente:*lasque poseen cargas formalesmáspequeñas,y• colocanlascargas negativaspreferentementesobre losátomosmás electronegativos.De acuerdoaeste criterio,laestructurade Lewismásadecuadapara el trifluorurode boro esla A: El criterio de las cargas formales,juntoa la regladel octeto,permite estimarcuál ocuálessonlas estructurasde Lewismásrazonablesparauna moléculadeterminada.Enocasiones,comoesel caso del BF3,cada criteriopredice,paraunamisma molécula,unaestructuradiferente.Nosiempre esfácil señalarcuál eslamás adecuada,aunque algunas ideasse dan a continuación. Resonancia. A veceslaspropiedadesde unamoléculase interpretanmejorsuponiendoque sudistribución electrónicaesintermediaentre variasestructurasde Lewis.El casomás evidenteescuandotenernosdos estructurasidénticasenenergía: Los experimentosmuestranque laestructurareal esunainediade lasdosestructurasde Lewis(así,por ejemplo,losdosenlacesN-0sonidénticos).A estamediase le llamaresonanciayala estructuraresultante de la mediase le llamahíbridode resonancia.Lasestructurasde resonanciasólose diferen-cianenla asignaciónde laposiciónde lospareselectrónicos,nuncaenlasposicionesde losátomos.El híbridode resonanciatiene unaenergíamenorque cadauna de las formasresonantes.Estadiferenciade energíarecibe el nombre de energíade resonancia. Preguntas de inicio: ¿Qué entiende por enlace iónico? ¿Qué es la carga formal ¿Qué entiende por resonancia? Referencia Bibliográfica de la Lectura Previa CHANG, Raymond y GOLDSBY, Kenneth A. Química. Undécima edición. México, McGraw-Hill Educación, 2015. El Enlace en las Moléculas. Disponible en: www3.uah.es/edejesus/resumenes/EQEM/tema_2.pdf
- 24. [Escriba aquí] [Escriba aquí] [Escribaaquí] LABORATORIOSDE QUÍMICA GENERAL. Universidadde Costarica.Guía de experimentos.Pp21-22-25 Práctica 6: Destilación.Disponible en: https://www.upo.es/depa/webdex/quimfis/docencia/quimbiotec/FQpractica6.pdf
- 25. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº13: Enlace covalente Descripción de la Sesión: Enlace covalente coordinado,formaciónde aductos.Expansiónde capade valencia Lectura Previa El enlace covalente se formacuandolosátomosque estánenlazándose tiendenarecibirelectrones. Enlace Covalente Molecular:Ese tipode enlace se formacuando losátomosinvolucradostiendenarecibir electrones.Lospareselectrónicossonunidosdebidoal compartimientode suselectrones,unavezque es imposibleatodoslosátomoscederelectronesorecibirlos. El par electrónicoesformadoporun electrónde cada átomoy pertenece simultáneamenteadosátomos. Las moléculas sonestructuras eléctricamenteneutras constituidas porlano ocurrenciatantode ganocuanto de perdidade electrones,formandoasíestructuraelectrónicamenteneutra. Poresarazón,ese enlace tambiénesdesignadomolecular. El agua (H2O) es uncompuestomoleculardeterminadoporel enlace de dosátomosde hidrógenoyunode oxígeno. H − O – H Enlace Covalente Coordinado.Este enlace esrepresentadoporunpequeñovectoryocurre cuandounode losátomospresentasuoctetocompletoyel otro necesitaadquirirdoselectronesparacompletarlo. Este enlace obedece alaTeoría del Octeto:Los átomosse unenintentandoadquirir ochoelectronesenla capa de valenciaosea,laconfiguraciónelectrónicade losgasesnobles. Siendoasí,un átomoque ya alcanzóla estabilidadelectrónicase une aotro que necesitaelectronespara completarsucapa de valencia.Unejemplode este enlace escuandoun átomode azufre (S) se ligaa dosde oxígeno(O) para formardióxidode azufre (SO2). O = S —> O La ligase formaporque esestablecidoundoble enlace del azufreconunode losoxígenosque necesita alcanzar laestabilidad electrónica,osea,ochoelectronesenlacapade valencia(regladel octeto).El enlace coordinadoesrepresentadoporlaseta,donde el azufre comparte unparde suselectronesconel otro oxígeno. Estructuras deLewis para especies químicas que presentan expansióndela capa devalencia Para especiesquímicascomoel ion, IO53-o lamolécula, XeO,2F2,el procedimientoestándarparala obtenciónde lasestructurasde Lewisfalla.Estose debe aque cuando se hace el cálculopara determinarel númerode electronesacompartir(S),se consigue unnúmeroque esmenoral númerode enlacesnecesarios para que todoslos átomosesténunidosatravés de un enlace sencillo(estose puede constatarhaciendoel cálculopara las especiesindicadas arriba).Enestoscasosse hace necesariomodificarlamaneraenque se determinan Lasestructuras de Lewis. Preguntas de inicio: ¿Qué es la expansión de capa de valencia? ¿Qué es un enlace covalente coordinado? ¿Qué es una propiedad física y una propiedad química? Referencia Bibliográfica de la Lectura Previa CHANG,Raymondy GOLDSBY, KennethA.Química. Undécimaedición.México,McGraw-Hill Educación,2015. Capítulo 1.
- 26. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº14: Estequiometría Descripción de la Sesión: Conceptode mol, fórmulaempírica,formulamolecular.Relaciónycálculosestequiométricos.Reactivosen exceso,limitante,rendimiento. Lectura Previa Antecedentesestequiométricos: En la cinéticaquímicaque estudialasvelocidadesde losprocesosquímicossiendofunciónlaconcentración de las especiesque reaccionan,losproductosde reacción,catalizadorese inhibidores,de losdiferentes mediosdisolventes,variablescomotemperatura,presiónque puedenafectarala velocidadde unareacción. La cinéticaquímicabuscala relaciónentre laformaprecisaenque varía la velocidadde reacciónconel tiempo,ylanaturalezade las colisionesintermoleculares(que influyenlavelocidad) implicadasenla generaciónde losproductosde reacción.La mayoría de lasreacciones implicanunaserie de procesosetapaa etapa,cuya sumacorresponde ala Estequiometríaenlaque se combinanlosreactivosyse formanlos productos.Sinembargo,sólounade ellasesgeneralmente laetapadeterminantede lavelocidad (generalmenteenlaformaciónde productos),muchomásrápidasque otras. Una vez analizados los diversos tipos de reacciones se pueden estudiar los aspectos cuantitativos de las reacciones químicas, (la cantidad en las que estas reacciones forman productos). Las relaciones ponderales (o de masa) entre reactivos y productos en una reacción química representan la Estequiometría de la reacción. Para interpretar una reacción cuantitativamente, se requiera aplicar el conocimiento de las masas molares y el concepto de mol. Molaridad, Normalidad,Molalidad,Fracción molar, porcentajesMasa enMasa, masa en volumen,volumen en volumen. Molaridad (M): Existendistintasformasde expresarlaconcentraciónde unadisolución,perolasdosmásutilizadasson:gramos por litro(g/l) yMolaridad(M).Losgramos por litroindicanlamasade soluto,expresadaengramos,contenida enundeterminadovolumende disolución,expresadoenlitros.Así,unadisoluciónde clorurode sodioconuna concentración de 40 g/l contiene 40 g de cloruro de sodio en un litro de disolución. La Molaridad se define como la cantidad de sustancia de soluto, expresada en moles,contenida en un cierto volumen de disolución, expresado en litros, es decir: M = n/V.El número de moles de soluto equivale al cociente entre la masa de soluto y la masa de un mol (masa molar) de soluto. Molalidad(m): La molalidad se define como el número de moles de solutodisueltos en 1kg de disolvente esto quiere decir: Molalidad= Moles de soluto /masa de disolvente (Kg) Por ejemplo, para preparar una disolución acuosa 1 molal o 1m de sulfato de sodio (Na2SO4) es necesario disolver1mol(142.0g) de lasustanciaen1000g de agua.Dependiendode lanaturalezade lainteracciónsoluto disolvente,el volumenfinal de ladisoluciónserámayoromenorde 1000ml. Tambiénesposible,aunque muy improbable que el volumen final sea de 1000ml Cabe hacer la aclaraciónque para expresar Molaridad se utiliza (M) y para expresar Molalidad se utiliza (m) Porcentajes: Ejemplo.- El ácidofosfórico (H3PO4) se usaenlosdetergentes,fertilizantes,dentífricosybebidasgaseosas. Calcúlese lacomposiciónporcentual enmasade H,P,yO en este compuesto. La masamolar del H3PO4 estádada por 3(1.008g) + 30.97g + 4(16g)= 97.99 g La composiciónporcentual es: %H= %P= %O= Peroeste procesotambiénse puede realizarde formainversa,esdecir;si tenemosel porcentajeque existe de cada elementoenlamoléculaanalizadapodremosobtenerlafórmulaempíricade lamolécula. Trate de realizarlo.
- 27. [Escriba aquí] [Escriba aquí] [Escribaaquí] Preguntas de inicio: ¿Qué es la estequiometría? ¿Qué es Molaridad y Molalidad? ¿Cómo prepara una solución molar? Referencia Bibliográfica de la Lectura Previa CHANG, Raymond y GOLDSBY, Kenneth A. Química. Undécima edición. México, McGraw-Hill Educación, 2015. Capítulo 1. LABORATORIOSDE QUÍMICA GENERAL. Universidadde Costarica.Guía de experimentos.Pp53-57
- 28. [Escriba aquí] [Escriba aquí] [Escribaaquí] Semana Nº15: Soluciones Descripción de la Sesión: Expresiónde soluciones.%p/p,%p/v,molaridad,molalidad.Soluto,solvente,densidad.Propiedades coligativas. Lectura Previa Unidadesde concentración El estudiocuantitativode unadisoluciónrequiere que se conozcasu concentración,esdecir, lacantidadde solutopresente endeterminadacantidadde unadisolución.Losquímicosutilizan variasunidadesde concentracióndiferentes;cadauna de ellastiene ciertasventajas,así comoalgunaslimitaciones. Examinaremoslascuatrounidadesde concentraciónmáscomunes: porcentaje enmasa,fracciónmolar, molaridadymolalidad. Tipos de unidadesde concentración Porcentaje en masa: El porcentaje en masa (tambiénllamado porcentajeen peso o peso porcentual) esla relación de la masa de un soluto en la masa de la disolucion,multiplicado por100%: El porcentaje enmasano tiene unidadesporque esunarelaciónde cantidadessemejantes. Fracción molar (X): La fracción molarde un componente de unadisolución,el componenteA,se representa como XA y se define como : La fracciónmolarno tiene unidades,debidoaque tambiénrepresentaunarelaciónde dos cantidades semejantes. Molaridad (M): La molaridadesel númerode molesde solutoen1L de disolución,esdecir, Por tanto,lasunidadesde lamolaridadsonmoles/L. Molalidad(m):La molalidad esel número demoles desoluto disueltosen 1 kg (1 000 g) de un disolvente, esdecir, Por ejemplo,paraprepararuna disoluciónacuosade sulfatode sodio(Na2SO4) 1molal,o1 m, es necesario disolver1mol (142.0 g) de la sustanciaen1 000 g (1 kg) de agua.Dependiendo de lanaturalezade la interacciónsoluto-disolvente,el volumenfinal de ladisoluciónserámayor omenorque 1 000 mL. Tambiénes posible,aunquepocoprobable,que el volumenfinal seaigual a1 000 mL. Comparación entre las unidadesde concentración La elecciónde unaunidadde concentracióndependedel propósitodel experimento.Porejemplo, lafracción molarno se utilizaparaexpresarlaconcentraciónde lasdisoluciones paravaloracionesoparaanálisis gravimétricos,peroesapropiadaparael cálculode presiones parcialesde losgasesypara trabajar con presionesde vaporde lasdisoluciones. Laventajade lamolaridadradicaen que,porlo general,esmásfácil medirel volumen de unadisolución,utilizandomatracesvolumétricoscalibradosconprecisión,que pesarel disolvente. Porestarazón,engeneral se prefiere lamolaridad sobre lamolalidad. Pero,lamolalidades independientede latemperatura,yaque la concentraciónse expresaennúmerode molesde solutoymasa de disolvente(porej.el volumende unadisolución incrementaconla temperatura, yporende cambiala molaridad). Debidoaésto,enalgunasocasionesespreferible utilizarmolalidad envezde molaridad. Algunasvecesesnecesarioconvertirunaunidadde concentraciónde unadisoluciónen otra;por ejemplo, cuandose emplealamismadisoluciónendiferentesexperimentosque requierendiferentesunidadesde concentraciónparalos cálculos.Suponga que se quiere expresarlaconcentraciónde unadisoluciónde glucosa(C6H12O6) 0.396 m en molaridad.Sabemos que hay0.396 molesde glucosaen1 000 g del disolvente y necesitamosdeterminarel volumende estadisolución.Primero,calculamoslamasade la disoluciónapartir de la masa molarde la glucosa:
- 29. [Escriba aquí] [Escriba aquí] [Escribaaquí] La siguienteetapaesladeterminaciónexperimental de la densidadde ladisolución,lacual esde 1.16 g/mL.Ahora podemosexpresarel volumende ladisolución,enlitros,de la siguiente manera Por último,lamolaridadde ladisoluciónestádadapor: Comose observa,ladensidadde ladisoluciónse utilizacomo factor de conversiónentre molalidad ymolaridad. Preguntas de inicio: Una muestra de 0.892 g de cloruro de potasio (KCl) se disuelve en 54.6 g de agua. ¿Cuál es el porcentaje en masa de KCl en la disolución? ¿Qué ventajas tiene el usar molalidad por sobre molaridad? Si se preparauna disolucióna20°C y su concentraciónse expresaen:porcentaje enmasa,molalidady molaridad.Ladisoluciónse calientaa88°C. ¿Cambiaránlasunidadesconcentración? ¿Cuáles? Referencia Bibliográfica de la Lectura Previa CHANG, Raymond y GOLDSBY, Kenneth A. Química. Undécima edición. México, McGraw-Hill Educación, 2015. Unidadesde Concentración.Disponibleen: http://depa.fquim.unam.mx/amyd/archivero/Expresiones_Concentracion_31504.pdf
- 30. [Escriba aquí] [Escriba aquí] [Escribaaquí] SesiónNº16: Descripción de la Sesión: Lectura Previa Preguntas de inicio: Referencia Bibliográfica de la Lectura Previa
- 31. [Escriba aquí] [Escriba aquí] [Escribaaquí] SesiónNº17: Descripción de la Sesión: Lectura Previa Preguntas de inicio: Referencia Bibliográfica de la Lectura Previa