Acevedo baudilio quimica i_grupo 8 _ii-2010_
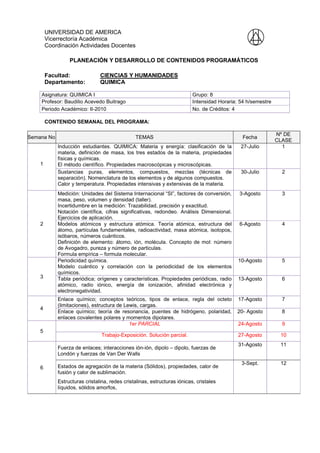
- 1. UNIVERSIDAD DE AMERICA Vicerrectoría Académica Coordinación Actividades Docentes PLANEACIÓN Y DESARROLLO DE CONTENIDOS PROGRAMÁTICOS Facultad: CIENCIAS Y HUMANIDADES Departamento: QUIMICA Asignatura: QUIMICA I Grupo: 8 Profesor: Baudilio Acevedo Buitrago Intensidad Horaria: 54 h/semestre Periodo Académico: II-2010 No. de Créditos: 4 CONTENIDO SEMANAL DEL PROGRAMA: Semana No. TEMAS Fecha Nº DE CLASE 1 Inducción estudiantes. QUIMICA: Materia y energía: clasificación de la materia, definición de masa, los tres estados de la materia, propiedades físicas y químicas. El método científico. Propiedades macroscópicas y microscópicas. 27-Julio 1 Sustancias puras, elementos, compuestos, mezclas (técnicas de separación). Nomenclatura de los elementos y de algunos compuestos. Calor y temperatura. Propiedades intensivas y extensivas de la materia. 30-Julio 2 2 Medición: Unidades del Sistema Internacional “SI”, factores de conversión, masa, peso, volumen y densidad (taller). Incertidumbre en la medición: Trazabilidad, precisión y exactitud. Notación científica, cifras significativas, redondeo. Análisis Dimensional. Ejercicios de aplicación. 3-Agosto 3 Modelos atómicos y estructura atómica. Teoría atómica, estructura del átomo, partículas fundamentales, radioactividad, masa atómica, isotopos, isóbaros, números cuánticos. Definición de elemento: átomo, ión, molécula. Concepto de mol: número de Avogadro, pureza y número de particulas. Formula empírica – formula molecular. 6-Agosto 4 3 Periodicidad química. Modelo cuántico y correlación con la periodicidad de los elementos químicos. 10-Agosto 5 Tabla periódica; orígenes y características. Propiedades periódicas, radio atómico, radio iónico, energía de ionización, afinidad electrónica y electronegatividad. 13-Agosto 6 4 Enlace químico; conceptos teóricos, tipos de enlace, regla del octeto (limitaciones), estructura de Lewis, cargas. 17-Agosto 7 Enlace químico; teoría de resonancia, puentes de hidrógeno, polaridad, enlaces covalentes polares y momentos dipolares. 20- Agosto 8 5 1er PARCIAL 24-Agosto 9 Trabajo-Exposición. Solución parcial. 27-Agosto 10 6 Fuerza de enlaces; interacciones ión-ión, dipolo – dipolo, fuerzas de Londón y fuerzas de Van Der Walls 31-Agosto 11 Estados de agregación de la materia (Sólidos), propiedades, calor de fusión y calor de sublimación. Estructuras cristalina, redes cristalinas, estructuras iónicas, cristales líquidos, sólidos amorfos, 3-Sept. 12
- 2. UNIVERSIDAD DE AMERICA Vicerrectoría Académica Coordinación Actividades Docentes Semana No. TEMAS Fecha Nº DE CLASE 7 Difracción de rayos X. 7-Sept. 13 Estados de agregación de la materia (Líquidos), propiedades, fuerzas intermoleculares, tensión superficial, viscosidad, presión de vapor, punto de ebullición. Propiedades del agua. 10-Sept. 14 8 Estados de agregación de la materia (gases); composición de la atmósfera, propiedades de los gases, presión de un gas, presión atmosférica, leyes de los gases. Ejercicios. 14-Sept. 15 Teoría cinética molecular; difusión de los gases, gases reales. Taller: leyes de los gases. 17-Sept. 16 9 Laboratorio 1. Normas de seguridad y reconocimiento del material del laboratorio. 21-Sept. 17 Definiciones, óxidos, ácidos, bases y sales; propiedades físicas y químicas, y aplicaciones industriales Nomenclatura Química Inorgánica; tipos de nomenclatura, 24-Sept. 18 10 Laboratorio 2. Punto de fusión y de ebullición y propiedades electrolíticas de las disoluciones acuosas. 28-Sept. 19 Reacciones Químicas y Estequiometria; definición, clases de reacciones, balanceo. Reactante límite, reactante en exceso. Ejercicios de aplicación. 1-Oct. 20 11 Laboratorio 3. Elementos del grupo IA y IIA. 5-Oct. 21 2º PARCIAL. 8-Oct. 22 12 Laboratorio 4. Reacciones química. 12-Oct. 23 Trabajo-Exposición- Solución del parcial. 15-Oct.. 24 13 Laboratorio 5. Reacciones de oxido - reducción. 19-Oct. 25 Tipos de balanceo, oxido reducción y ión electrón. Ejercicios de aplicación. 22-Oct. 26 14 Laboratorio 6. Estequiometria. 26-Oct. 26 Ecuación de estado, peso molecular, densidad, presiones parciales. Ejercicios de aplicación. 29-Oct. 27 15 Estequiometria de gases y disoluciones. Ejercicios de aplicación 2-Nov. 28 Taller estequiometria. 5-Nov. 29 16 Exposiciones del trabajo en laboratorio. 9-Nov. Reacciones químicas y estequiometria – Ejercicios de aplicación industrial. Exposiciones del trabajo en laboratorio. 12-Nov. 30
- 3. UNIVERSIDAD DE AMERICA Vicerrectoría Académica Coordinación Actividades Docentes EVALUACIÓN: Corte Evaluación Fecha Actividad Porcent. 100% Primero Parcial 1 (P1) 24-Agosto Evaluación escrita (15%) 30%Especificar otras actividades como: Quizes, talleres, trabajos en grupo, exposiciones C/clase Tareas (5%), Quizes- Talleres (5%) 25-Agosto Trabajo/exposición (5%) Segundo Parcial 2 (P2) 8-Octubre Evaluación escrita (15%) 30%Especificar otras actividades como: Quizes, talleres, trabajos en grupo, exposiciones C/clase Tareas (5%), Quizes- Talleres (5%) 15-Octubre Trabajo/exposición (5%) Tercero Examen Final (16-27 Nov.) Programado por la facultad Evaluación escrita (25 %) 40% Especificar tipo prueba: oral, escrita, exposición. Semanal c/clase Laboratorio: Informes 5% Exp. 5% Quizes 5% METODOLOGÍA: (Actividades - recursos – otras ayudas didácticas) El estudiante debe leer, analizar, y trabajar aplicaciones con anterioridad, los temas de la clase, de acuerdo al programa académico recibido (PRESENTAR TAREAS). Debe asistir a las clases para aclarar dudas sobre el correspondiente tema, y ampliar sus conocimientos sobre aplicaciones prácticas Debe asistir a las explicaciones y trabajar en clase y extra clase desarrollando talleres y guías en grupo e individual. (TALLERES EN CLASE) Debe realizar y presentar trabajo extraclase como complemento a las explicaciones dadas por el profesor. Debe presentar pruebas escritas como exámenes parciales, quices y examen final. Deben asistir a los laboratorios con las guías leídas y portando los elementos de seguridad industrial. BIBLIOGRAFÍA BRADY, J.E.: Química Básica. Principios y Estructura. Ed. Limusa Weley. México, 1999. BROWN, L. Química: La ciencia central, tercera edición, editorial Prentice –Hall Hispanoamericana S.A. Mexico 1999. EN BIBLIOTECA.. CHANG, R.: Química. McGraw-Hill. México, etc. 2002. EN BIBLIOTECA DICKERSON, R.E.; GRAY H.R.; DARENSBOURG, M.Y. y DARENSBOURG, D.J.: Principios de Química. Ed. Reverté, S.A. Barcelona, 1992. HEIN, M. y ARENA, S.: Fundamentos de Química, 10.a edición. Internacional Thomson Editores. México, etc., 2001. MAHAN, B.H. y MYERS, R.J.: Química. Curso Universitario. Addison-Wesley iberoamericana. Argentina, etc., 1990.
- 4. UNIVERSIDAD DE AMERICA Vicerrectoría Académica Coordinación Actividades Docentes PETRUCCI, R.H.; HARWOOD, W.S. y HERRING, F.G.: Química General. 8ª Edición. Ed. Prentice Hall. Madrid, etc., 2002. UMLAND, J. B. y BELLAMA, J. M.: Química General, 3.a edición. Internacional Thomson Editores. México, etc., 2000. WHITTEN, K.W.; DAVIS, R.E. y PECK, M.L.: Química General Superior. Mc Graw Hill. México, etc., 1998. EN BIBLIOTECA INTERNET: www.chemtutor.com (Principios básicos, ecuaciones y ejercicios de practica) www.eduteca.com (Practicas de laboratorio) www.scirus.com www.edu.aytolacoruna.es/aula/química www.educaplus.org/sp2002/index_sp.php www.geocities.com/erkflores/Tabla.htm www.ciencianet.com Journal of Chemical Education Online. http://www.ur.mx/cursos/diya/quimica/jescobed/estados.htm GUIAS: Guía de laboratorio de química I. Fundación Universidad de América. TRABAJOS DE EXPOSICION GRUPAL EN CLASE. Temas de exposición primer corte: Grupo Nº Tema Fecha 1 Métodos físico químicos de separación. Taller. 30-Julio 2 Unidades del SI; ejercicios; análisis dimensional, sufijos, prefijos, factores de conversión al sistema ingles conversión de unidades de temperatura. 3-Agosto 3 Ejercicios de notación científica y cifras significativas. Ejercicios. 6-Agosto 4 Numero atómico, número de masa, Isotopos, isóbaros, sustancia pura, definición de elemento, molécula, ion y compuesto. Ejercicios. 10-Agosto 5 Concepto de mol, Formula molecular formula empírica, formulas de compuestos iónicos, y modelos moleculares. 13-Agosto 6 Modelo atómicos y estructura atómica. Taller. 17-Agosto Temas de exposición segundo corte: Grupo Nº Tema Fecha 1 Números cuánticos. Ejercicios. 31-Agosto. 2 Leyes de los gases. Ejercicios. 14-Sept 3 Estequiometria de gases. Ejercicios. 17-Sept. 4 Nomenclatura; química inorgánica. Taller. 24-Sept. 5 Reacciones Químicas, clases de reacciones, balanceo. Taller. 1-Oct. 6 Estequiometria. Reactante límite, reactante en exceso 1-Oct.
- 5. UNIVERSIDAD DE AMERICA Vicerrectoría Académica Coordinación Actividades Docentes Trabajo de exposición grupal. Tiempo de exposición: 15 a 20 min. Se debe entregar un informe de la exposición (50%) 8 días antes de la exposición. Contenido del trabajo: Titulo. Resumen. Introducción (marco teórico). Objetivos Ejercicios, y resolución. Ejemplos.( Discusión. Conclusiones. Taller y/o ejercicios propuestos Bibliografía (localizada). TRABAJO EN LABORATORIO. • EXPOSICIONES SEGURIDAD EN LABORATORIO. Grupo Nº Tema Fecha 1 Normas de seguridad para trabajo en laboratorio. 21-Sept. 2 Toxicidad. 21-Sept. 3 Reactividad química. 21-Sept. 4 Almacenamiento de reactivos químicos y hojas de seguridad. 21-Sept. 5 Materiales de laboratorio. 21-Sept. 6 Montajes; destilación, sublimación, cristalización, punto de fusión y ebullición, extracción Soxhlet, etc. 21-Sept. *10 minutos por cada exposición. • INFORMES DE LABORATORIO Contenido informes de laboratorio: Titulo. Resumen. Introducción (marco teórico). Objetivos. Procedimiento (diagrama de flujo) Análisis y discusión de resultados. Conclusiones. Taller y/o ejercicios propuestos Bibliografía (localizada). Cada grupo debe llevar para la sesión de laboratorio: Cuaderno de laboratorio, rollo de papel absorbente o trapo para limpiar, 1 caja de fósforos,