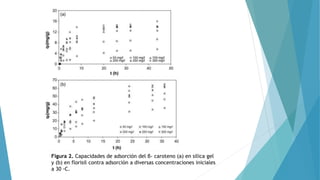
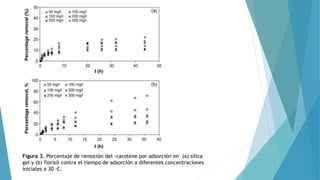
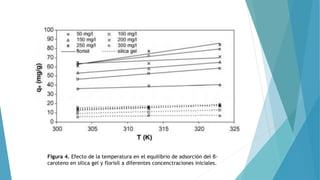
Este documento resume un estudio sobre la cinética y termodinámica de la adsorción de β-caroteno en adsorbentes a base de sílica. Los autores encontraron que la capacidad de adsorción aumenta con el tiempo, la concentración inicial y la temperatura. La adsorción en florisil fue mayor que en sílica gel y se ajustó mejor al modelo de Langmuir. El proceso fue espontáneo y endotérmico, haciendo del florisil un buen adsorbente para β-caroteno.