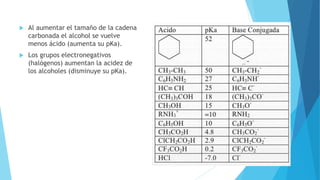
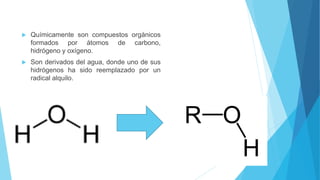
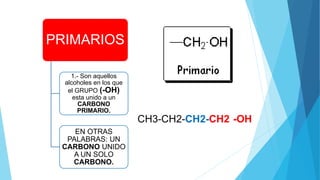
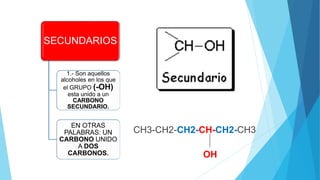
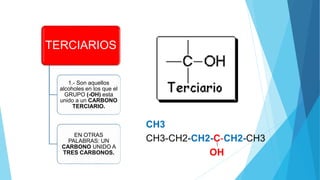
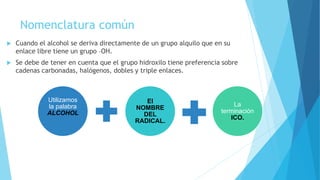
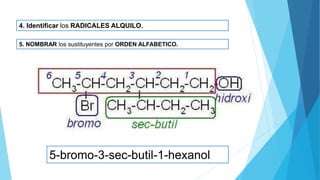
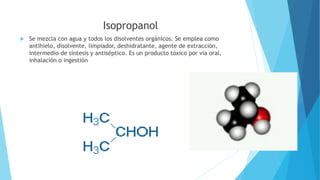
El documento resume las propiedades y clasificación de los alcoholes. Define a los alcoholes como compuestos orgánicos que contienen un grupo funcional hidroxilo. Explica que se clasifican como alcoholes primarios, secundarios o terciarios dependiendo del carbono al que esté unido el grupo hidroxilo. También describe algunas aplicaciones de los alcoholes en fármacos, cosméticos y alimentos.