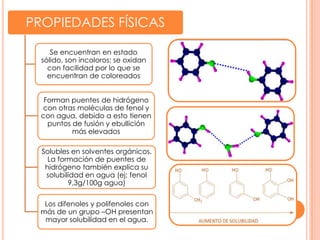
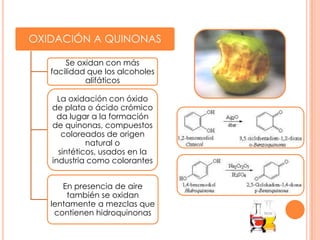
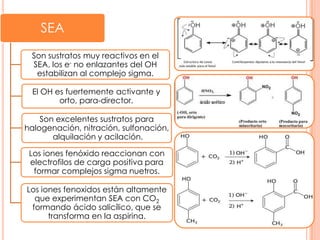
Este documento trata sobre los fenoles, compuestos orgánicos que contienen uno o más grupos hidroxilo unidos directamente al anillo aromático. Los fenoles presentan propiedades físicas y químicas similares a los alcoholes alifáticos pero también se diferencian en algunas propiedades importantes como su acidez. Dentro de las reacciones características de los fenoles se encuentran la oxidación a quinonas y las sustituciones electrófilas aromáticas. El documento también describe la nomencl