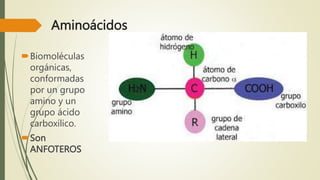
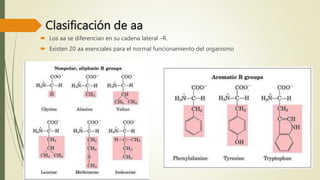
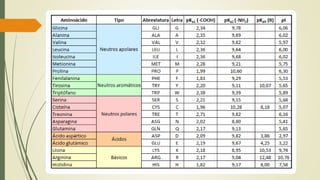
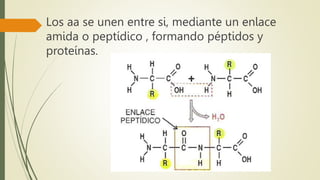
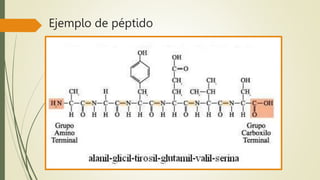
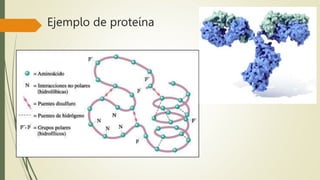
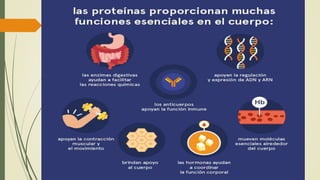
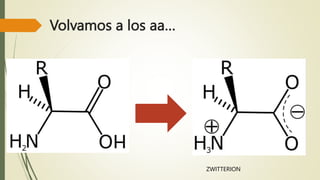
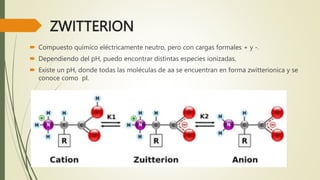
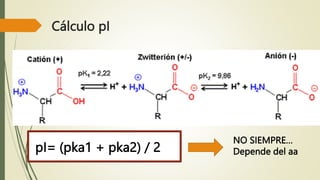
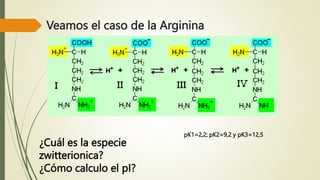
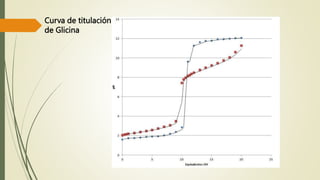
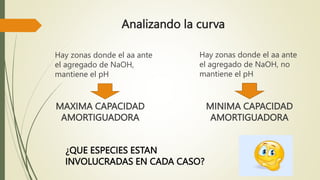
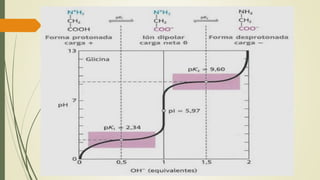
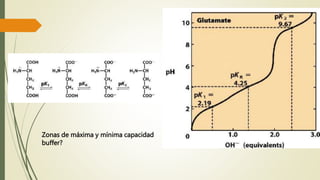
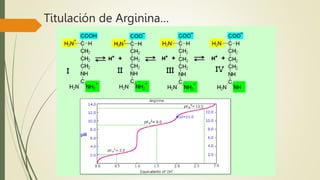
Los aminoácidos son biomoléculas orgánicas conformadas por un grupo amino y un grupo ácido carboxílico. Existen 20 aminoácidos esenciales para el organismo. Los aminoácidos se unen formando péptidos y proteínas mediante enlaces peptídicos. Las proteínas cumplen múltiples funciones importantes como estructurales, reguladoras, defensivas y de transporte. Los aminoácidos son moléculas anfóteras que tienden a estar en su forma zwitteriónica. Pueden actuar