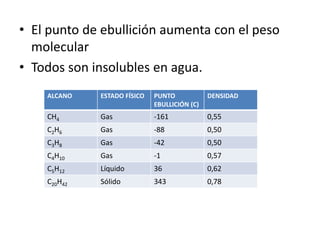
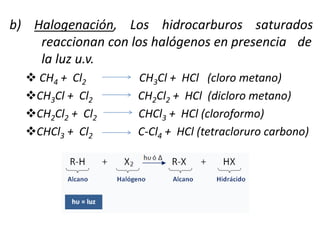
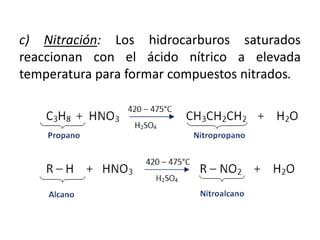
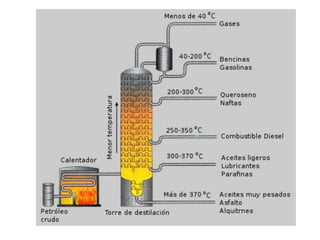
Los hidrocarburos saturados tienen propiedades físicas y químicas que dependen de su tamaño molecular. Físicamente, los de 1-4 carbonos son gases, los de 5-17 carbonos son líquidos como la gasolina y el diésel, y los de 18 o más carbonos son sólidos como grasas y alquitranes. Químicamente, pueden oxidarse o halogenarse y reaccionar con ácido nítrico o craquearse para romper moléculas grandes. Principalmente se obtienen del petróleo crudo a través de