ENLACE._TIPOS_DE_SUSTANCIAS._PROPIEDADES.pdf
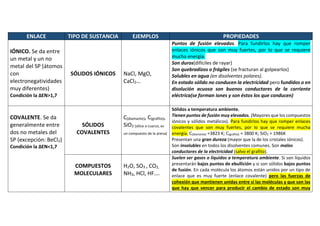
- 1. ENLACE TIPO DE SUSTANCIA EJEMPLOS PROPIEDADES IÓNICO. Se da entre un metal y un no metal del SP (átomos con electronegatividades muy diferentes) Condición la ∆EN>1,7 SÓLIDOS IÓNICOS NaCl, MgO, CaCl2… Puntos de fusión elevados. Para fundirlos hay que romper enlaces iónicos que son muy fuertes, por lo que se requiere mucha energía. Son duros(difíciles de rayar) Son quebradizos o frágiles (se fracturan al golpearlos) Solubles en agua (en disolventes polares). En estado sólido no conducen la electricidad pero fundidos o en disolución acuosa son buenos conductores de la corriente eléctrica(se forman iones y son éstos los que conducen) COVALENTE. Se da generalmente entre dos no metales del SP (excepción: BeCl2) Condición la ∆EN<1,7 SÓLIDOS COVALENTES C(diamante), C(grafito), SiO2 (sílice o cuarzo, es un compuesto de la arena) Sólidos a temperatura ambiente. Tienen puntos de fusión muy elevados. (Mayores que los compuestos iónicos y sólidos metálicos). Para fundirlos hay que romper enlaces covalentes que son muy fuertes, por lo que se requiere mucha energía. C(diamante) =3823 K; C(grafito) = 3800 K; SiO2 = 1986K Presentan una gran dureza (mayor que la de los cristales iónicos). Son insolubles en todos los disolventes comunes. Son malos conductores de la electricidad (salvo el grafito). COMPUESTOS MOLECULARES H2O, SO3 , CO2, NH3, HCl, HF…. Suelen ser gases o líquidos a temperatura ambiente. Si son líquidos presentarán bajos puntos de ebullición y si son sólidos bajos puntos de fusión. En cada molécula los átomos están unidos por un tipo de enlace que es muy fuerte (enlace covalente) pero las fuerzas de cohexión que mantienen unidas entre sí las moléculas y que son las que hay que vencer para producir el cambio de estado son muy
- 2. EN ESTE CASO HAY ENLACES INTERMOLECULARES (ENTRE MOLÉCULAS) QUE PUEDEN SER DE DOS TIPOS: - FUERZAS DE VAN DER WAALS - ENLACES POR PUENTE DE HIDRÓGENO débiles (Fuerzas de Van der Waals/ enlaces por puente de hidrógeno) por lo que se necesita poca energía para fundir o hacer hervir estas sustancias. Los enlaces por puente de hidrógeno son más fuertes que las fuerzas de Van der Waals, por lo que se requiere más energía para fundir o vaporizar aquellas sustancias que lo presenten. Solo hay tres compuestos inorgánicos donde aparece este tipo de enlace (H2O, HF, NH3), pero sí hay muchos compuestos orgánicos que lo presentan: alcoholes, ácidos carboxílicos, aminas y amidas primarias y secundarias. Por su parte, las fuerzas de Van der Waals crecen con el tamaño molecular(son mayores en compuestos con mayor masa molar) Suelen ser poco solubles en agua. En el caso de moléculas polares éstas sustancias sí se disuelven en agua. (Igual disuelve a igual. Las sustancias polares se disuelven en disolventes polares y las apolares en disolventes apolares) Son malos conductores de la corriente eléctrica. Los electrones se localizan en los enlaces. METÁLICO. Se da entre átomos con electronegatividades bajas y similares (entre átomos de elementos metálicos) SÓLIDOS METÁLICOS Fe(s), Ca(s), Cu(s)… Cualquier metal del SP Aleaciones: bronce (Cu y Sn); Latón (Cu y Zn) Son sólidos a temperatura ambiente (a excepción del mercurio). Temperaturas de fusión altas, debido a que el enlace entre los átomos es fuerte. Pero varían mucho. Por ejemplo, la del cesio es solamente 28,44ºC y la del wolframio 3422ºC Buenos conductores del calor y la electricidad, debido a la existencia de electrones libres que pueden moverse. Dúctiles y maleables, debido a la posibilidad de que las capas de iones se pueden deslizar unas sobre otras sin que se rompa la red metálica.