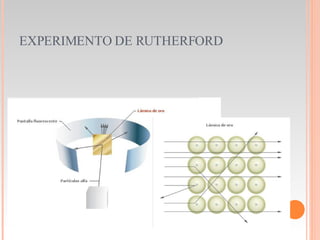
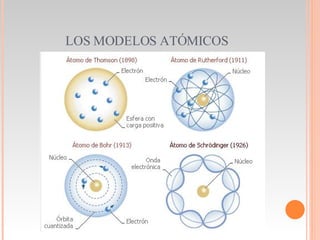
El documento resume la evolución del modelo atómico desde la antigua Grecia hasta la teoría atómica moderna. Demócrito propuso que toda materia está compuesta de átomos indivisibles. Los alquimistas intentaron transmutar elementos. Robert Boyle propuso que la materia está compuesta de partículas diminutas. Thomson propuso un modelo de átomo con electrones incrustados en materia positiva. Rutherford descubrió el núcleo atómico a través de experimentos de dispersión. Millikan midió la carga del