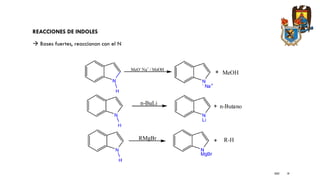
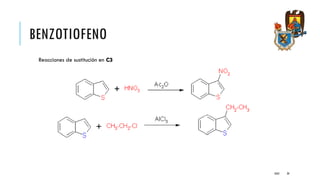
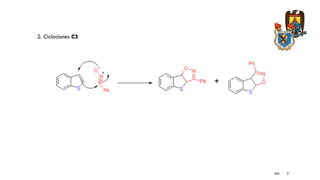
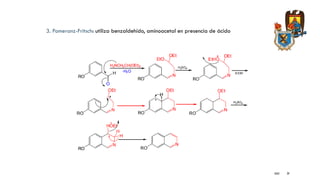
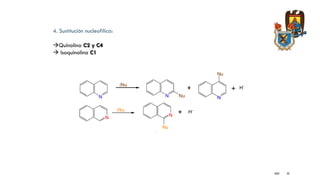
El documento presenta información sobre la síntesis y reacciones de varios heterociclos aromáticos como el pirrol, indol, benzofurano, benzotiofeno, quinolinas e isoquinolinas. Explica métodos comunes de síntesis como Paal-Knorr para pirrol, Fisher y Madelung para indol, y Skraup, Doebner-Vonmiller y Combes para quinolinas. También describe reacciones típicas como sustitución electrofílica, halogenación, oxidación y ciclaciones para estos compuest