Informe 5 - Física II
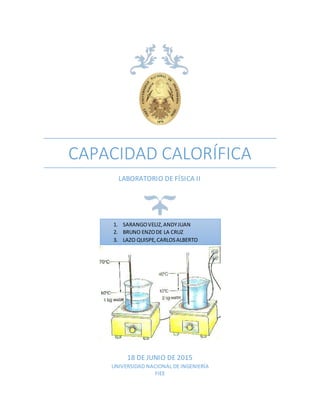
- 1. CAPACIDAD CALORÍFICA LABORATORIO DE FÍSICA II 18 DE JUNIO DE 2015 UNIVERSIDAD NACIONAL DE INGENIERÍA FIEE 1. SARANGOVELIZ,ANDYJUAN 2. BRUNO ENZODE LA CRUZ 3. LAZO QUISPE,CARLOSALBERTO
- 2. Capacidadcalorífica| UNI CAPACIDAD CALORIFICA I. OBJETIVOS Determinar el equivalente en agua de un calorímetro. Determinar el calor específico del cobre. Determinar el calor específico del aluminio.
- 3. Capacidadcalorífica| UNI II. MATERIALES Pinzas de sujeción. Cocina eléctrica o jarra eléctrica. Vaso pirex. Un thermo. Un vernier. Termómetro. Guantes de protección.
- 5. Capacidadcalorífica| UNI III. FUNDAMENTO TEÓRICO I. CAPACIDAD CALORIFICA La capacidad calorífica o capacidad térmica de un cuerpo es el cociente entre la cantidad de energía calorífica transferida a un cuerpo o sistema en un proceso cualquiera y el cambio de temperatura que experimenta. En una forma más rigurosa, es la energía necesaria para aumentar la temperatura COCIN A
- 6. Capacidadcalorífica| UNI de una determinada sustancia en una unidad de temperatura.1 Indica la mayor o menor dificultad que presenta dicho cuerpo para experimentar cambios de temperatura bajo el suministro de calor. Puede interpretarse como una medida de inercia térmica. Es una propiedad extensiva, ya que su magnitud depende, no solo de la sustancia, sino también de la cantidad de materia del cuerpo o sistema; por ello, es característica de un cuerpo o sistema particular. Por ejemplo, la capacidad calorífica del agua de una piscina olímpica será mayor que la de un
- 7. Capacidadcalorífica| UNI vaso de agua. En general, la capacidad calorífica depende además de la temperatura y de la presión. II. EQUILIBRIO TERMICO El equilibrio térmico es aquel estado en el cual se igualan las temperaturas de dos cuerpos, las cuales, en sus condiciones iniciales presentaban
- 8. Capacidadcalorífica| UNI diferentes temperaturas. Una vez que las temperaturas se equiparan se suspende el flujo de calor, llegando ambos cuerpos al mencionado equilibrio término. III. CALORÍMETRO El calorímetro es un instrumento que sirve para medir las cantidades de calor
- 9. Capacidadcalorífica| UNI suministradas o recibidas por los cuerpos. En un caso ideal de transferencia de calor se puede hacer una simplificación: que únicamente se consideren como sustancias intervinientes a las sustancias calientes y frías entre las que se produce la transferencia de calor y no los recipientes, que se considerarían
- 10. Capacidadcalorífica| UNI recipientes adiabáticos ideales, cuyas paredes con el exterior serían perfectos aislantes térmicos (calorímetro); el caso real más parecido sería un termo o un saco de dormir con relleno de plumas. IV. EQUIVALENTE EN AGUA Cuando un líquido contenido en un calorímetro recibe calor (energía) la absorbe, pero también la absorben las paredes del calorímetro. Lo mismo sucede cuando pierde energía. Esta intervención del calorímetro en el proceso se representa por su
- 11. Capacidadcalorífica| UNI equivalente en agua: su presencia equivale a añadir al líquido que contiene los gramos de agua que asignamos a la influencia del calorímetro y que llamamos "equivalente en agua". El "equivalente en agua" viene a ser "la cantidad de agua que absorbe o desprende el mismo calor que el calorímetro". IV. PROCEDIMIENTO EXPERIMENTAL PARTE I Tome la temperatura ambiente
- 12. Capacidadcalorífica| UNI Mida 300 ml de agua y caliéntala a 80 °C. Anote la temperatura exacta del agua. Agregue a su termo (calorímetro) el agua caliente espere unos minutos hasta que alcance la temperatura de equilibrio. Anote la temperatura de equilibrio. b) PARTE II PARTE 2a Utilizando agua a mayor de temperatura que el cuerpo metálico. Determine la masa del metal.
- 13. Capacidadcalorífica| UNI Vuelva a calentar el agua y mida exactamente la temperatura del agua del calorímetro Determine la temperatura del metal. Coloque el metal en el recipiente y determine la temperatura de equilibrio. Vuelve a repetir el experimento para el segundo metal. PARTE 2b
- 14. Capacidadcalorífica| UNI Utilizando agua a menor temperatura que el cuerpo metálico Caliente el metal, utilizando un recipiente y agua caliente a unos 80 °C. Anote exactamente la temperatura del mental. Mida 300 ml de agua a temperatura ambiente. Anote la temperatura exacta del agua. Coloque el metal en el recipiente y determine la temperatura de equilibrio.
- 15. Capacidadcalorífica| UNI Vuelva a repetir el experimento para el segundo metal. VI. CALCULO Y RESULTADOS DETERMINE LA EXPRESIÓN PARA CALCULAR EL EQUIVALENTE EN AGUA DEL CALORÍMETRO. Primero para hallar la expresión del equivalente gramo pondremos la siguiente expresión al interactuar dos
- 16. Capacidadcalorífica| UNI cuerpos que en este caso serían el agua y el calorímetro. ECUACIÓN NUMERO 1 𝑄 𝑎𝑔𝑢𝑎 + 𝑄 𝑐𝑎𝑙𝑜𝑟𝑖𝑚𝑒𝑡𝑟𝑜 = 0 … (1) Pero ambos calores que tienes cada cuerpo mencionado se calculan a través de las siguientes 2 ecuaciones: ECUACIÓN NUMERO 2 𝑄 𝑎𝑔𝑢𝑎 = 𝑚 𝑎𝑔𝑢𝑎 ∗ 𝑐𝑒 𝑎𝑔𝑢𝑎 ∗ ∆𝑇𝑎𝑔𝑢𝑎 … (2) ECUACIÓN NÚMERO 3
- 17. Capacidadcalorífica| UNI 𝑄 𝑐𝑎𝑙𝑜𝑟𝑖𝑚𝑒𝑡𝑟𝑜 = 𝑚 𝑒𝑞 ∗ 𝑐𝑒 𝑎𝑔𝑢𝑎 ∗ ∆𝑇𝑐𝑎𝑙𝑜𝑟𝑖𝑚𝑒𝑡𝑟𝑜 … (3) De la ecuaciones (1), (2) y (3) obtenemos la expresión en donde calcularemos la expresión equivalente en agua para el calorímetro: 𝒎 𝒆𝒒 = − 𝒎 𝒂𝒈𝒖𝒂 ∗ ∆𝑻 𝒂𝒈𝒖𝒂 ∆𝑻 𝒄𝒂𝒍𝒐𝒓𝒊𝒎𝒆𝒕𝒓𝒐 UTILIZANDO SUS DATOS CALCULE EL EQUIVALENTE EN AGUA DEL CALORÍMETRO.
- 18. Capacidadcalorífica| UNI En el cuadro que se presenta están los datos obtenidos en el laboratorio que nos permitirán hallar el equivalente de agua del calorímetro. 𝑻 𝒂𝒎𝒃𝒊𝒆𝒏𝒕𝒆(℃) 26℃ 𝒎 𝒂𝒈𝒖𝒂(g) 277g 𝑻 𝟎(℃) 80℃ 𝑻 𝒆𝒒(℃) 53℃
- 19. Capacidadcalorífica| UNI En la ecuación encontrada del enunciado anterior procedemos a reemplazar los datos: 𝒎 𝒆𝒒 = 𝟐𝟕𝟕×𝟐𝟕 𝟐𝟕 Con los datos obtenemos que equivalente en gramo del agua es 277 g. DETERMINE LA EXPRESIÓN PARA CALCULAR LA CAPACIDAD CALORÍFICA DEL METAL Ahora para obtener la capacidad calorífica de cada metal formamos la ecuación como en el caso anterior en
- 20. Capacidadcalorífica| UNI función de los calores que obtiene el agua, el metal y el calorímetro ECUACIÓN NUMERO 5 𝑄 𝑎𝑔𝑢𝑎 + 𝑄 𝑐𝑎𝑙𝑜𝑟𝑖𝑚𝑒𝑡𝑟𝑜 + 𝑄 𝑚𝑒𝑡𝑎𝑙 = 0 … (5) Ahora para cada calor tiene su expresión para hallarlo ECUACIÓN NUMERO 6 𝑄 𝑎𝑔𝑢𝑎 = 𝑚 𝑎𝑔𝑢𝑎 ∗ 𝑐𝑒 𝑎𝑔𝑢𝑎 ∗ ∆𝑇𝑎𝑔𝑢𝑎 … (6) ECUACIÓN NUMERO 7 𝑄 𝑐𝑎𝑙𝑜𝑟𝑖𝑚𝑒𝑡𝑟𝑜 = 𝑚 𝑒𝑞 ∗ 𝑐𝑒 𝑎𝑔𝑢𝑎 ∗ ∆𝑇𝑐𝑎𝑙𝑜𝑟𝑖𝑚𝑒𝑡𝑟𝑜 … (7) ECUACIÓN NUMERO 8
- 21. Capacidadcalorífica| UNI 𝑄 𝑚𝑒𝑡𝑎𝑙 = 𝐶 𝑚𝑒𝑡𝑎𝑙 ∗ ∆𝑇 𝑚𝑒𝑡𝑎𝑙 … (8) Ahora de las ecuaciones (5), (6), (7) y (8) obtenemos la ecuación que nos permitirá hallar la capacidad calorífica de un metal. 𝑪 𝒎𝒆𝒕𝒂𝒍 = − (𝒎 𝒂𝒈𝒖𝒂 ∗ ∆𝑻 𝒂𝒈𝒖𝒂 + 𝒎 𝒆𝒒 ∗ ∆𝑻 𝒄𝒂𝒍𝒐𝒓𝒊𝒎𝒆𝒕𝒓𝒐) ∗ 𝒄𝒆 𝒂𝒈𝒖𝒂 ∆𝑻 𝒎𝒆𝒕𝒂𝒍 UTILICE SUS DATOS EXPERIMENTALES PARA DETERMINAR LA CAPACIDAD CALORÍFICA DEL METAL, EN LOS PROCESOS 2A Y 2B PARA DADA METAL.
- 22. Capacidadcalorífica| UNI De la tabla 2a que se muestra procedemos hallar la capacidad calorífica del cobre. 𝑻 𝒂𝒎𝒃𝒊𝒆𝒏𝒕𝒆 (℃) 𝟐𝟔℃ 𝒎 𝑪𝒖(𝒈) 95g 𝑻 𝑪𝒖(℃) 26℃ 𝑻 𝒂𝒈𝒖𝒂(℃) 80℃ 𝒎 𝒂𝒈𝒖𝒂(g) 351g 𝑻 𝒆𝒒(℃) 73℃ Con los datos obtenidos reemplazamos en la ecuación encontrada en el enunciado 3; Q (calorímetro)=0 𝑪 𝑪𝒖 = − 𝟑𝟓𝟏∗( 𝟕𝟑−𝟖𝟎) 𝟕𝟑−𝟐𝟔 = 𝟓𝟐 ( 𝒄𝒂𝒍 °𝑪 ) 𝒂𝒑𝒓𝒐𝒙.
- 23. Capacidadcalorífica| UNI De la tabla 2b que se muestra procedemos hallar la capacidad calorífica del aluminio. 𝑻 𝒂𝒎𝒃𝒊𝒆𝒏𝒕𝒆 (℃) 26℃ 𝒎 𝑨𝒍(𝒈) 137g 𝑻 𝑨𝒍(℃) 70℃ 𝑻 𝒂𝒈𝒖𝒂(℃) 26℃ 𝒎 𝒂𝒈𝒖𝒂(g) 373g 𝑻 𝒆𝒒(℃) 34℃ Con los datos obtenidos reemplazamos en la ecuación encontrada en el enunciado 3; Q (calorímetro)=0
- 24. Capacidadcalorífica| UNI 𝑪 𝑨𝒍== − 𝟑𝟕𝟑∗( 𝟑𝟒−𝟐𝟔) 𝟑𝟒−𝟕𝟎 = 𝟖𝟐 ( 𝒄𝒂𝒍 °𝑪 ) 𝒂𝒑𝒓𝒐𝒙. DETERMINE EL CALOR ESPECÍFICO DE CADA CUERPO METÁLICO QUE HA UTILIZADO. 𝒄𝒆 𝒎𝒆𝒕𝒂𝒍 = 𝑪 𝒎𝒆𝒕𝒂𝒍 𝒎 𝒎𝒆𝒕𝒂𝒍 ENTONCES PARA 2A 𝑪 𝑪𝒖 = 𝟓𝟐 = 𝟗𝟓 ∗ 𝑪 𝒆(𝑪𝒖) 𝑪 𝒆(𝑪𝒖) = 𝟎. 𝟓𝟒( 𝒄𝒂𝒍 𝒈°𝑪 ) ENTONCES PARA 2B 𝑪 𝑨𝒍 = 𝟖𝟐 = 𝟏𝟑𝟕 ∗ 𝑪 𝒆(𝑨𝒍)
- 25. Capacidadcalorífica| UNI 𝑪 𝒆(𝑨𝒍) = 𝟎. 𝟓𝟗( 𝒄𝒂𝒍 𝒈°𝑪 ) COMPARE EL VALOR OBTENIDO EN EL PASO 5 CON EL VALOR ESPERADO PARA ESTOS MATERIALES. ENTONCES PARA 2A 𝑪 𝒆(𝑪𝒖) = 𝟎. 𝟓𝟒( 𝒄𝒂𝒍 𝒈°𝑪 ) Experimental 𝑪 𝒆(𝑪𝒖) = 𝟎. 𝟎𝟗𝟑( 𝒄𝒂𝒍 𝒈°𝑪 ) Tablas %error= 480% aprox. (muy alto) ENTONCES PARA 2B 𝑪 𝒆(𝑨𝒍) = 𝟎. 𝟓𝟗( 𝒄𝒂𝒍 𝒈°𝑪 ) Experimental
- 26. Capacidadcalorífica| UNI 𝑪 𝒆(𝑨𝒍) = 𝟎. 𝟐𝟏𝟕( 𝒄𝒂𝒍 𝒈°𝑪 ) Tablas %error= 171% aprox. (muy alto) VII. CONCLUSIONES Y OBSERVACIONES Vemos que el error es muy alto, deducimos que es por el termómetro, ya que no puede medir de forma exacta la temperatura del metal, esto es ya que está involucrado el factor tiempo y el factor de irradiación de calor infrarroja mayormente. Se
- 27. Capacidadcalorífica| UNI recomienda para este experimento usar otro tipo de termómetro para los metales así será más efectivo el cálculo.
- 28. Capacidadcalorífica| UNI VIII. BIBLIOGRAFÍA SEARS – SEMANSKY: Física universitaria, tomo I - 12ava edición. Cap. 15 TIPLER, MOSCA: Física para la ciencia y la tecnología Vol. 1 5ta Edición.
- 29. Capacidadcalorífica| UNI SERWAY: Física para las ciencias y la ingeniería volumen I-5ta edición. Cap. 16 HUGO MEDINA GUZMAN: Física II. HUMBERTO LEYVA: Física II – Tomo 2
