Leishmaniasis Expocision curso Extraccion y Recoleccion de Muestras Biologicas Humanas II.pptx
- 1. • Curso : Extracción y Recolección de Muestras Biológicas Humanas II • Profesor: Josue Bravo Medina • Aula : 2MLA51-08 • Integrantes Mejía Muñoz Rosaura Ravelo Simón Mirella Talaverano Ugarte Jennifer Ventura Mancilla Ashley Verdi Pulido Josué Fabricio Vega Vega Jesús
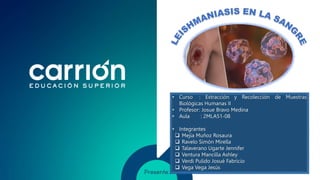
- 2. INTRODUCCIÓN La leishmaniasis (o leishmaniosis) es causada por más de 20 especies del género de parásitos protozoarios Leishmania. Se transmiten por la picadura de flebótomos hembra infectados, que necesitan ingerir sangre para producir huevos. Hay unas 70 especies animales, entre ellas el ser humano, que pueden ser fuente de transmisión del parásito. Existen 3 tipos; Cutánea y Mucosa son enfermedades infecciosas que afectan a la piel y las mucosas causadas por protozoos del género Leishmania y transmitidas a los animales y humanos por vectores de la familia Psychodidae y la leishmaniasis Visceral es una enfermedad crónica, sistémica que afecta principalmente a niños menores de cinco años; puede estar asociada a la desnutrición y a otras condiciones. La leishmaniasis en el Perú es una enfermedad que afecta predominantemente a población andina y selvática, la distribución de casos se extiende a 21 departamentos del Perú donde se encuentra presente el vector de la enfermedad. En esta exposición desarrollaremos los siguientes puntos para una buena toma de muestra y brindar un resultado confiable; indicaciones preanaliticas, materiales y la conservación y transporte de la muestra.
- 3. INDICACIONES PRE-ANALÍTICAS DE LA LEISHMANIOSIS: La ficha Epidemiológica debe estar debidamente llenada Corroborar la identificación del paciente, es decir, los nombres y apellidos completos, fecha de nacimiento, DNI, edad, localidad, entre otros. La muestra será marcada con un código creado con los datos del paciente. Adjuntar la orden del médico tratante para realizar la toma indicada. Solicite al paciente que le muestre la lesión. Explique el procedimiento al paciente. Observar la o las lesiones presentes en el cuerpo del paciente. Escoger la lesión que tenga menor tiempo de evolución o en caso de existir infección secundaria obtener la muestra de la menos infectada.
- 4. Leishmaniosis Cutánea Frotis (raspado) del borde interno de la úlcera • Materiales: 1. Guantes de cirugía 2. Alcohol 70° 3. Algodón 4. Solución salina 5. Jabón quirúrgico 6. Gasa estéril 7. Láminas porta-objetos 8. Lancetas u hojas de bisturí 9. Colorante de giemsa o wright 10.Microscopio óptico 11.Aceite de inmersión. MATERIALES:
- 5. Leishmaniasis Mucosa: Biopsia de piel • Materiales: 1. Guantes de cirugía 2. Agua destilada o solución salina fisiológica estéril 3. Jabón quirúrgico 4. Alcohol 5. Agujas estériles 6. Gasas estériles 7. Jeringas de 1c.C. 8. Xilocaína al 2% sin epinefrina 9. Mango y hojas de bisturí nos. 11 y 15 10.Frasco con formol tamponado al 10 %. 11.Si se dispone de sacabocados de 4mm se puede tomar la biopsia con él. MATERIALES:
- 6. Leishmaniasis Visceral: Examen parasitológico directo de médula ósea: • Materiales: 1. Xilocaína simple al 2% 2. Jeringa heparinizada 3. Aguja de grueso calibre o trocar 4. Láminas porta-objeto 5. Colorante giemsa o Wright 6. Microscopio MATERIALES:
- 7. TOMA DE MUESTRA PARA EL DIAGNÓSTICO PARASITOLÓGICO DE LEISHMANIASIS, ZONAS ENDÉMICAS: Frotis Directo 1. Registrar datos del paciente. 2. Realizar limpieza del área de trabajo (OH 70%) 3. Disponer material necesario. 4. Lavarse las manos y colocarse los guantes. 5. Explicar procedimiento. 6. Rotular las láminas en uno de sus extremos. 7. Seleccionar la lesión con menor tiempo de evolución y buscar los bordes más indurados que indiquen que la lesión está activa. 8. Limpiar la lesión con desinfectante con movimientos circulares del centro hacia la periferia de la lesión. 9. Si la lesión presenta costra, humedecerla y retirarla. Luego limpiar nuevamente la lesión.
- 8. Frotis Directo 10. Seleccionar el área para la incisión alrededor del borde más activo con los dedos índice y pulgar. Hacer presión durante 20 seg. Para lograr una buena hemostasia. Sin dejar de hacer presión, realizar con el bisturí una incisión superficial paralela al borde de la lesión de 5 mm de longitud por 3 mm de profundidad. 11. Realizar un total de 3 láminas por paciente con 3 impresiones por lámina portaobjetos y cada impresión de 8 a 10 mm de diámetro aprox. 12. Descartar la hoja de bisturí. 13. Aplicar crema antibiótica en la lesión con un bajalenguas y cubrirla con gasa estéril y esparadrapo. 14. Dejar secar las láminas horizontalmente sobre la mesa de trabajo a T° ambiente durante 15 minutos. 15. Fijar las láminas cubriéndolas en su totalidad con metanol absoluto. Dejarlas en posición vertical para escurrir el exceso de metanol y dejar secar entre 15 y 20 minutos. 16. En el envío debe realizarse en porta láminas o envueltas en papel absorbente.
- 9. TOMA DE MUESTRA PARA EL DIAGNÓSTICO PARASITOLÓGICO DE LEISHMANIASIS, ZONAS ENDÉMICAS: Aspirado de lesión 1. Registrar datos del paciente 2. Limpiar zona de trabajo (OH 70%) 3. Disponer material necesario 4. Lavado de manos y colocación de guantes 5. Explicar procedimiento al paciente 6. Seleccionar la lesión con menor tiempo de evolución y buscar los bordes más indurados que indiquen que la lesión está activa 7. Limpiar la zona de lesión del centro hacia la periferia 8. Si hay lesiones costrosas humedecerlas y retirarlas. Luego hacer nuevamente la limpieza de la lesión 9. Tener preparada una solución de PBS con antibiótico 10. Preparar 3 ó 4 jeringas de insulina y envasar 0.1 de la mezcla anterior en cada una de ellas 11. Introducir la aguja de 3 a 4 mm en el borde exterior de la lesión de manera que se forme un ángulo de 45°. Luego aspirar para obtener líquido tisular (evitar aspirar sangre) 12. Repetir el procedimiento con las jeringas restantes en distintos sitios del borde de la lesión 13. Al terminar la toma de muestra hacer presión sobre la lesión con gasa estéril hasta que se controle el sangrado. Luego cubrir con crema antibiótica y gasa estéril.
- 10. CONSERVACIÓN Y TRANSPORTE DE MUESTRAS Raspado • Refrigeración (4°C - 8°C) hasta 48 horas. • A largo plazo se conserva en Buffer de lisis (-20°C a -80°C) • Evitar la congelación y descongelación Aspirado • Refrigeración (4°C a 8°C) hasta 48 horas a largo plazo se conserva en buffer de lisis a (-20°C a -80°C) • Evitar la congelación y descongelación.
- 11. CASO CLÍNICO Paciente de sexo masculino de 33 años Consultó por úlcera de cinco centímetros, localizada en cara interna de maléolo izquierdo, poco profunda, de bordes netos, sobreelevados he indurados, de fondo seroso, dolorosa, de más de seis meses de evolución con el antecedente de haber viajado a zona tropical de Bolivia previo a la aparición de dicha lesión. Con la confirmación histológica de leishmaniasis cutánea, había sido tratado en otro centro de salud con anfotericina B liposomal en dosis y tiempos correctos sin respuesta, y posteriormente con imipenem, sin ninguna mejoría. Un nuevo estudio histopatológico (Figura 2) efectuado en nuestro nosocomio arrojó el mismo diagnóstico y ante la falta de disponibilidad de antimoniales en nuestro medio se inició tratamiento con itraconazol (400 mg/día) vía oral, por 30 días y luego 200 mg/día vía oral durante tres meses más, con curación completa de la lesión. El paciente ha sido controlado durante seis meses luego de finalizado el tratamiento y se mantiene en remisión completa.
- 12. Muchas gracias