Mapa Menta Lectrua #1 ¿En que difieren los óxidos metálicos de los óxidos no metálicos?
•Descargar como PPTX, PDF•
0 recomendaciones•240 vistas
Los óxidos metálicos son sólidos mientras que los óxidos no metálicos pueden ser sólidos, líquidos o gaseosos. Los átomos requieren energía para unirse y formar compuestos, adoptando configuraciones electrónicas que cumplen la regla del octeto y alcanzan mayor estabilidad.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...schizophrenia_candy_blue
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...schizophrenia_candy_blue
Recomendados
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...schizophrenia_candy_blue
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...schizophrenia_candy_blue
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
ELECTRONES DE VALENCIA, ESTRUCTURA DE LEWIS Y REGLA DEL OCTETO

ELECTRONES DE VALENCIA, ESTRUCTURA DE LEWIS Y REGLA DEL OCTETO
Fis quiweb. formulación química inorgánica. fórmulas e información

Fis quiweb. formulación química inorgánica. fórmulas e información
Lectura 1 mapa mental:¿En que difieren los óxidos metálicos y no metálicos?

Lectura 1 mapa mental:¿En que difieren los óxidos metálicos y no metálicos?
Similar a Mapa Menta Lectrua #1 ¿En que difieren los óxidos metálicos de los óxidos no metálicos?
Similar a Mapa Menta Lectrua #1 ¿En que difieren los óxidos metálicos de los óxidos no metálicos? (20)
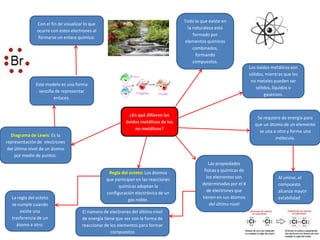
Mapa Menta Lectrua #1 ¿En que difieren los óxidos metálicos de los óxidos no metálicos?
- 1. Todo lo que existe en la naturaleza está formado por elementos químicos combinados, formando compuestos. Con el fin de visualizar lo que ocurre con estos electrones al formarse un enlace químico. Los óxidos metálicos son sólidos, mientras que los no metales pueden ser sólidos, líquidos o gaseosos. Este modelo es una forma sencilla de representar enlaces. ¿En qué difieren los óxidos metálicos de los no metálicos? Se requiere de energía para que un átomo de un elemento se una a otro y forme una mólecula. Diagrama de Lewis: Es la representación de electrones del último nivel de un átomo por medio de puntos. La regla del octeto se cumple cuando existe una trasferencia de un átomo a otro. Regla del octeto: Los átomos que participan en las reacciones químicas adoptan la configuración electrónica de un gas noble. El número de electrones del último nivel de energía tiene que ver con la forma de reaccionar de los elementos para formar compuestos Las propiedades físicas y químicas de los elementos son determinadas por el # de electrones que tienen en sus átomos del último nivel Al unirse, el compuesto alcanza mayor estabilidad