Dif. entre óx. metálicos y no metálicos: estructura y propiedades
•
0 recomendaciones•292 vistas
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...schizophrenia_candy_blue
Recomendados
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...schizophrenia_candy_blue
Más contenido relacionado
La actualidad más candente
La actualidad más candente (19)
ELECTRONES DE VALENCIA, ESTRUCTURA DE LEWIS Y REGLA DEL OCTETO

ELECTRONES DE VALENCIA, ESTRUCTURA DE LEWIS Y REGLA DEL OCTETO
Destacado
Destacado (14)
Encuentro Empresario - Transferencia Tecnológica y Talento Humano

Encuentro Empresario - Transferencia Tecnológica y Talento Humano
LASER ALEJANDRITA En ELIANA L VALENCIA. Listado De Empresas De LASER ALEJANDR...

LASER ALEJANDRITA En ELIANA L VALENCIA. Listado De Empresas De LASER ALEJANDR...
Similar a Dif. entre óx. metálicos y no metálicos: estructura y propiedades
Similar a Dif. entre óx. metálicos y no metálicos: estructura y propiedades (20)
REVISTA DE QUIMICA, ENLACES QUIMICOS Laura Marapacuto

REVISTA DE QUIMICA, ENLACES QUIMICOS Laura Marapacuto
Más de batiquimos (17)
Mapa mental de lectura #1 en que difieren los oxidos metalicos de los no meta...

Mapa mental de lectura #1 en que difieren los oxidos metalicos de los no meta...
Dif. entre óx. metálicos y no metálicos: estructura y propiedades
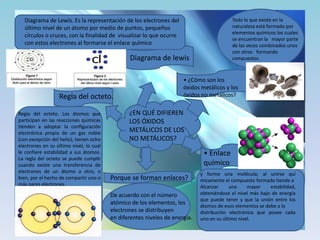
- 1. Todo lo que existe en la naturaleza está formado por elementos químicos los cuales se encuentran la mayor parte de las veces combinados unos con otros formando compuestos. Diagrama de Lewis. Es la representación de los electrones del último nivel de un átomo por medio de puntos, pequeños círculos o cruces, con la finalidad de visualizar lo que ocurre con estos electrones al formarse el enlace químico Diagrama de lewis Regla del octeto. Regla del octeto. Los átomos que participan en las reacciones químicas tienden a adoptar la configuración electrónica propia de un gas noble (con excepción del helio), tienen ocho electrones en su último nivel, lo cual le confiere estabilidad a sus átomos. La regla del octeto se puede cumplir cuando existe una transferencia de electrones de un átomo a otro, o bien, por el hecho de compartir uno o más pares electrones. • ¿Cómo son los óxidos metálicos y los óxidos no metálicos? ¿EN QUÉ DIFIEREN LOS ÓXIDOS METÁLICOS DE LOS NO METÁLICOS? • Enlace químico Porque se forman enlaces? De acuerdo con el número atómico de los elementos, los electrones se distribuyen en diferentes niveles de energía. y forme una molécula; al unirse quí micamente el compuesto formado tiende a Alcanzar una mayor estabilidad, obteniéndose el nivel más bajo de energía que puede tener y que la unión entre los átomos de esos elementos se debe a la distribución electrónica que posee cada uno en su último nivel.