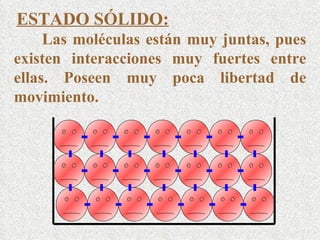
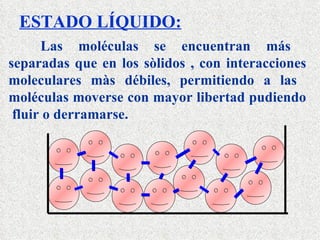
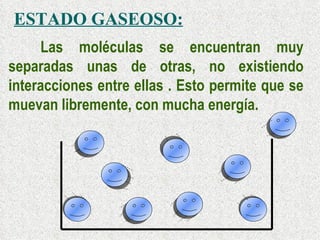
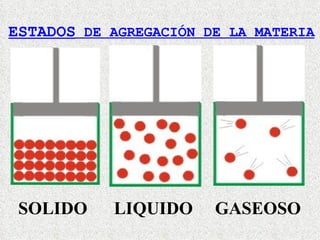
Este documento describe la clasificación de la materia según su estado de agregación y composición. La materia puede encontrarse en estado sólido, líquido o gaseoso dependiendo de la interacción entre sus moléculas. Según su composición, la materia puede ser una sustancia pura, compuesta por un solo elemento o compuesto, o una mezcla formada por dos o más sustancias que mantienen sus propiedades individuales. Las mezclas pueden ser homogéneas o heterogéneas.