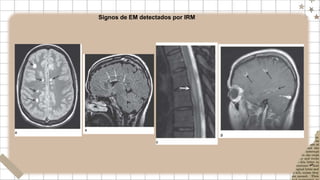
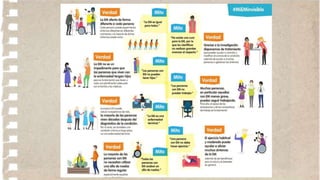
La esclerosis múltiple (EM) es una enfermedad crónica del sistema nervioso central caracterizada por la inflamación, desmielinización y cicatrización del tejido que conduce a pérdida neuronal. Afecta a 350,000 estadounidenses y 2.5 millones de personas en el mundo. La EM ocurre más en mujeres que en hombres y generalmente comienza entre los 20-40 años. Las lesiones ocurren en diferentes áreas y tiempos en el sistema nervioso central causando síntomas que varían dependiendo de la localización de las lesiones