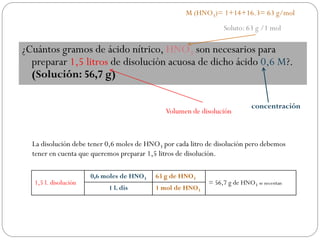
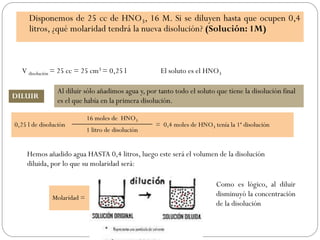
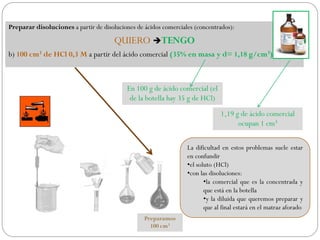
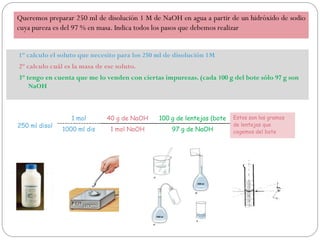
Este documento presenta varios problemas relacionados con la preparación y cálculo de concentraciones de disoluciones. Explica cómo determinar la concentración de una disolución expresada de diferentes formas, preparar disoluciones a partir de solutos sólidos o concentrados, diluir disoluciones y calcular la concentración resultante de mezclar disoluciones. También cubre cálculos para determinar la cantidad de soluto necesaria para una reacción química.