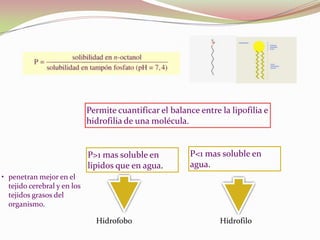
El documento describe el coeficiente de distribución y sus aplicaciones. El coeficiente de distribución permite definir el grado de disociación o asociación de sustancias, las constantes de equilibrio, y se utiliza para procesos de extracción y en farmacología para diseñar fármacos.