Aquí están los pasos para resolver este problema:
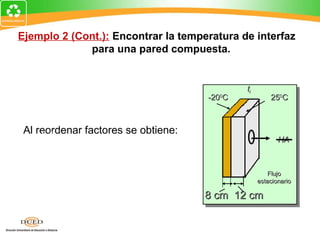
1. Dibuje un diagrama del proceso.
2. Identifique la información dada: mv = 4 g, tf = 600C
3. Identifique lo que se debe encontrar: mi
4. Escriba la ecuación de conservación de energía para el sistema:
Qhielo = Qvapor
5. Resuelva la ecuación para encontrar mi
La ecuación de conservación de energía es:
mi(Lf + c∆T) = mvLv
Donde:
Lf = fusión del hielo
c



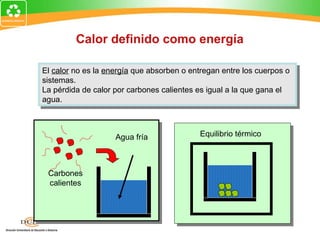












![Ejemplo 2: Un puñado de perdigones
de cobre se calienta a 900C y luego se
sueltan en 80 g de agua en un vaso a
100C. Si la temperatura de equilibrio es
180C, ¿cuál fue la masa del cobre? te= 180C
cw = 4186 J/kg C0; cs = 390 J/kg C0
aislador
mw = 80 g; tw= 100C; ts = 900C a 900C
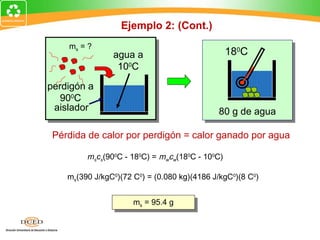
Pérdida de calor por perdigón = calor perdigón
ganado por agua 100C
mscs(900C - 180C) = mwcw(180C - 100C) agua a
Nota: las diferencias de temperatura son [alto - bajo] para asegurar valores
absolutos (+) perdido y ganado.](https://image.slidesharecdn.com/semana5-calor-120919124925-phpapp02/85/Semana-5-calor-17-320.jpg)




![Ejemplo 3 (Cont.): El paso uno es Q1 para convertir 10 g de hielo a
-200C a hielo a 00C (no agua todavía).
Q1 para elevar hielo a 00C: Q1 = mc∆t
-200C 00C
t
1000 Q1 = (10 g)(0.5 cal/gC0)[0 - (-200C)]
C
Q1 = (10 g)(0.5 cal/gC0)(20 C0)
Q1 = 100 cal
Q1 = 100 cal
00C
chielo= 0.5 cal/gC0
-200C hiel
Q
o](https://image.slidesharecdn.com/semana5-calor-120919124925-phpapp02/85/Semana-5-calor-23-320.jpg)






![Ejemplo 5 (Cont.):
Ganancia = 4000 cal + (50 cal/g)te
Pérdida de calor = mwcw∆t 00C 700C
∆t = 700C - te [alto - bajo] 50 g 200 g
te = ?
Pérdida = (200 g)(1 cal/gC0)(700C- te )
Pérdida = 14,000 cal - (200 cal/C0) te
El calor ganado debe ser igual al calor perdido:
4000 cal + (50 cal/g)te = 14,000 cal - (200 cal/C0) te](https://image.slidesharecdn.com/semana5-calor-120919124925-phpapp02/85/Semana-5-calor-30-320.jpg)