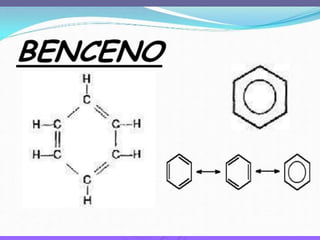
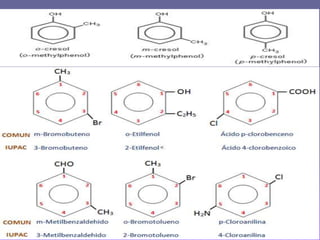
La molécula de benceno consiste en un anillo cerrado de seis átomos de carbono unidos por enlaces que resuenan entre uniones simples y dobles. Cada átomo de carbono está a su vez unido a un átomo de hidrógeno. En 1864-1865, Kekulé propuso la estructura de resonancia del benceno, en la que los electrones se deslocalizan entre enlaces simples y dobles de forma continua. Los hidrocarburos aromáticos policlíclicos como el benzopireno pueden ser cancerígenos