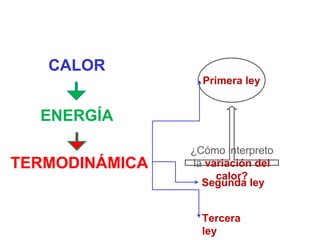
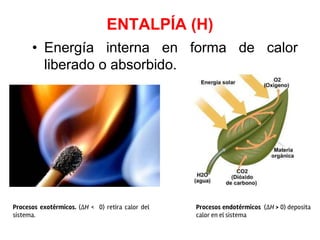
El documento trata sobre conceptos básicos de termodinámica. Explica que la termodinámica estudia los cambios de energía que acompañan procesos físicos y químicos y permite predecir si una reacción puede ocurrir bajo ciertas condiciones. Define conceptos clave como calor, trabajo, energía cinética y potencial. También describe las primeras leyes de la termodinámica sobre la conservación de la energía y que el interés principal es el cambio de energía que acompaña un cambio en el