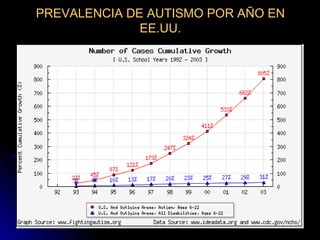
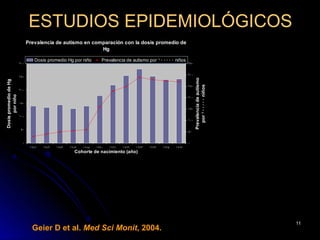
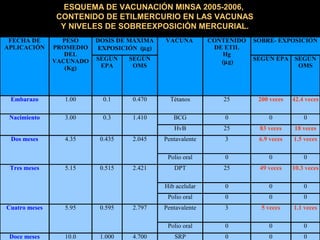
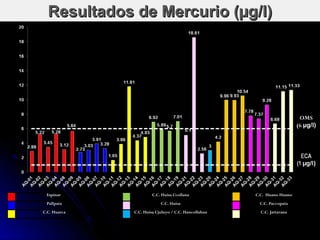
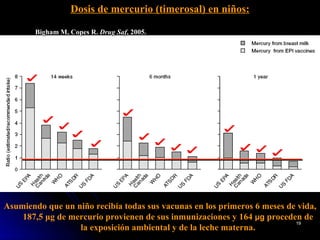
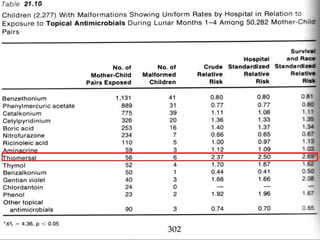
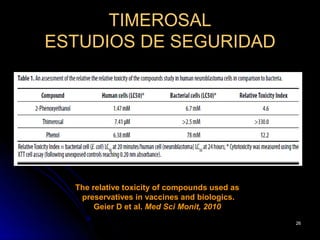
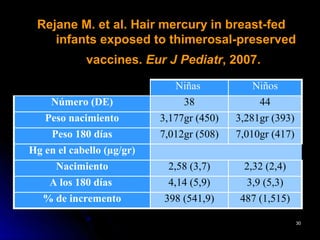
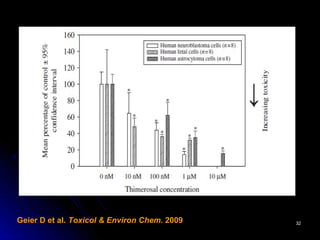
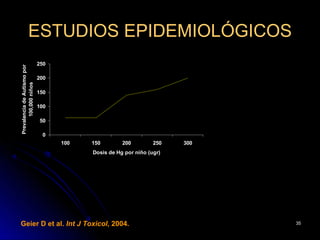
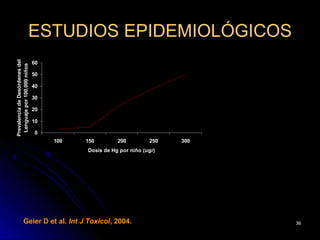
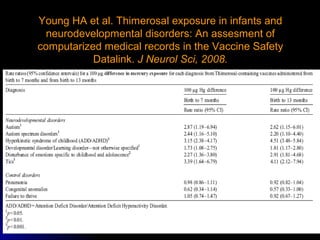
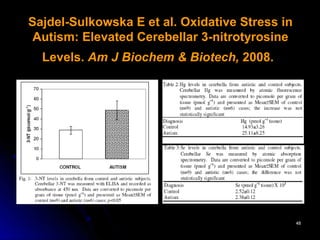
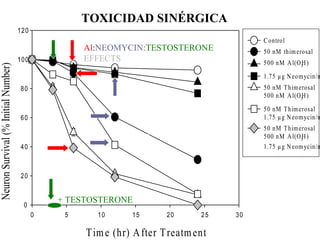
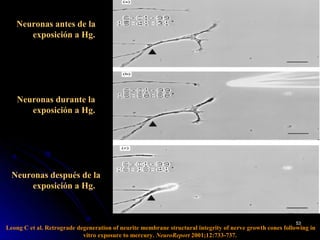
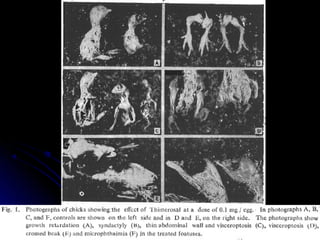
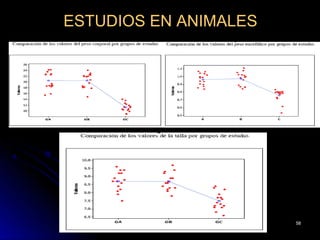
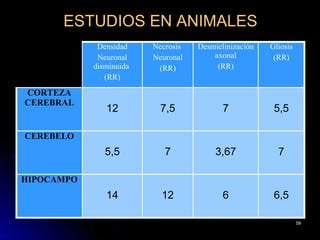
El documento habla sobre el mercurio en las vacunas. Explica que el timerosal, un preservante usado en algunas vacunas, contiene etilmercurio, una neurotoxina. Las dosis de mercurio que recibían los niños de las vacunas en EE.UU. han ido aumentando desde 1950 hasta 1992. Estudios epidemiológicos muestran que a medida que aumentaban las dosis de mercurio también lo hacía la prevalencia de autismo. El esquema de vacunación en el Perú expone a los niños a niveles de mer