_ISOMERIA_.pdf
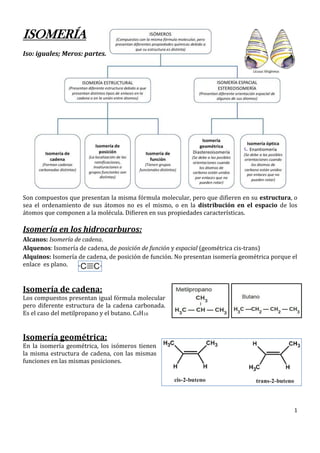
- 1. 1 ISOMERÍA Iso: iguales; Meros: partes. Son compuestos que presentan la misma fórmula molecular, pero que difieren en su estructura, o sea el ordenamiento de sus átomos no es el mismo, o en la distribución en el espacio de los átomos que componen a la molécula. Difieren en sus propiedades características. Isomería en los hidrocarburos: Alcanos: Isomería de cadena. Alquenos: Isomería de cadena, de posición de función y espacial (geométrica cis-trans) Alquinos: Isomería de cadena, de posición de función. No presentan isomería geométrica porque el enlace es plano. Isomería de cadena: Los compuestos presentan igual fórmula molecular pero diferente estructura de la cadena carbonada. Es el caso del metilpropano y el butano. C4H10 Isomería geométrica: En la isomería geométrica, los isómeros tienen la misma estructura de cadena, con las mismas funciones en las mismas posiciones.
- 2. 2 Pero como la molécula es rígida debido a la presencia del doble enlace (o de un anillo), los dos grupos funcionales estén próximos (isómero cis) o alejados (isómeros trans) si miramos desde el doble enlace Isomería de posición: Los isómeros de posición tienen el grupo funcional en distinta posición de la cadena carbonada. Por ejemplo el 1-buteno y el 2-buteno: Isomería de función: En compuestos oxigenados (entre otros): En esta tipo de isomería, los compuestos se caracterizan por tener distintos grupos funcionales, con la misma fórmula molecular. A continuación, un hidroxiácido, un ácido carboxílico y un éster comparten la misma fórmula: C2H4O2 Isómería óptica o estereoisomería: 1. ¿Qué es la actividad óptica? Existen moléculas que coinciden en todas sus propiedades excepto en su capacidad de desviar el plano de luz polarizada (en solución acuosa). Son los llamados isómeros ópticos. Uno de ellos desvía la luz polarizada hacia la derecha, y se designa (+), o dextrógiro, mientas que el otro la desvía en igual magnitud pero hacia la izquierda, y se designa (-) o levógiro. La propiedad se llama actividad óptica. 2. ¿Qué es la luz polarizada? Su comportamiento frente a la luz polarizada se debe a que la molécula carece de plano de simetría, y se pueden distinguir dos isómeros que son cada uno la imagen especular del otro, como la mano derecha lo es de la izquierda.
- 3. 3 3. .¿Qué son los isómeros ópticos? Ambas manos no son superponibles, pero son simétricas: la imagen especular de la mano derecha es la mano izquierda. Los isómeros ópticos se llaman enantiómeros. El caso más frecuente de ausencia de plano de simetría se debe a que algún carbono tetraédrico está unido a cuatro radicales distintos. Este carbono recibe el nombre de carbono asimétrico o carbono quiral. Representación genérica de un aminoácido, con un átomo de carbono quiral, lo que genera el par de enantiómeros. 4. ¿Siempre que hay átomos de carbono quiral hay actividad óptica? No. La presencia de átomos de carbono quiral es una condición necesaria pero no suficiente. Esto se da, por ejemplo en las formas meso y en las mezclas racémicas. Por otra parte, cuando dos compuestos tienen la misma fórmula molecular(son isómeros), presentan uno o más átomos de CARBONO quirales o asimétricos, puede que NO sean enantiómeros (imágenes especulares entre sí).No son superponibles pero tampoco son imágenes especulares uno de otro. A estos compuestos, se les llama DIASTERÓMEROS O DIASTEROISÓMEROS. Los vamos a ver en los glúcidos...estas estructuras que aparecen a continuación!!! 5. ¿Esta isomería, aparece solamente en compuestos orgánicos? NO, solamente se precisa un centro quiral, en el caso que está a continuación, ese centro quiral es el átomo de platino.
- 4. 4 Por si quieren profundizar: http://organica1.org/qo1/MO-CAP4.htm Material compilado de fuentes varias. Basado en: Biomoléculas. Lecciones de Bioquímica Estructural. Macarulla-Goñi. LUZ POLARIZADA: https://www.youtube.com/watch?v=Y4WChJwZNN4 ENANTIÓMEROS: https://www.youtube.com/watch?v=4yDIoDXUapM https://www.youtube.com/watch?v=VlnGB9EF3Zk http://www.quimicaorganica.net/estereoquimica.html https://www.slideserve.com/oleg/isomer-a-y-reactividad-de-los-compuestos-org-nicos Prof. Ximena Porley