iicristalografia-131209141419-phpapp01.pdf
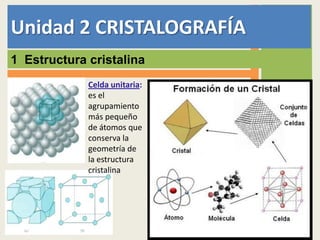
- 1. Unidad 2 CRISTALOGRAFÍA 1 Estructura cristalina Celda unitaria: es el agrupamiento más pequeño de átomos que conserva la geometría de la estructura cristalina
- 2. Unidad 2 CRISTALOGRAFÍA Que es un Cristal? Un cristal debe ser definido como un compuesto solidó de átomos, dispuestos en un patrón periódico en tres dimensiones No todos los sólidos son cristalinos, algunos son amorfos como el vidrio, y no tienen ningún arreglo regular de átomos.
- 3. 2 Estructuras cristalinas de los metales Factor de empaquetamiento atómico (FEA), es la fracción de volumen en una celda unidad que está ocupada por átomos. Este factor es adimensional y siempre menor que la unidad Índice de Coordinación (IC), se define como el número de átomos de su misma naturaleza que equidistan de él y que son sus vecinos más próximos. Cuanto más alto el IC, más estable Estructura cúbica de cuerpo centrado BCC
- 4. Cromo Un trozo de pirita, mineral rico en hierro. Tungsteno El cromo, el hierro y el tungsteno son BCC.
- 5. Ejemplo: Determinar el FEA para una estructura cúbica centrada en el cuerpo BCC D d a a a a a a a a a a d La celda para la estructura BCC, contiene 2 átomos. Si r es el radio de un átomo: El volumen de una esfera es: El FEA es: de donde
- 6. Estructura cúbica centrada en las caras FCC
- 7. Cristal de sulfato de cobre Cristal de oro Nitrato de niquel Plomo El aluminio, el cobre, el oro, el níquel, el platino, la plata y el plomo son FCC
- 8. Estructura hexagonal de empaquetamiento cerrado
- 9. Son metales HC el cadmio, magnesio, titanio y zinc. Cadmio Magnecio Titanio Zinc
- 10. La longitud de un lado del hexágono es a, y su altura es c Ejemplo: Detrerminar el FEA para una estructura exagonal El mineral berilo es un cristal hexagonal
- 11. Cálculo de la densidad El conocimiento de la estructura cristalina de un sólido metálico permite el cálculo de su densidad mediante la siguiente relación:
- 12. Ejemplo El Cu posee una estructura FCC y un radio atómico de 0.1278 nm. Considerando que los átomos son esferas sólidas que contactan a lo largo de las diagonales de la celdilla unidad FCC. ¿ Cuál es el valor teórico de la densidad del Cu ? Masa atómica del cobre: Volumen de la celda Densidad volumétrica Densidad real
- 13. Ejemplo.- El aluminio tiene una masa atómica de 26.97 (g/mol). Sabiendo que cristaliza en el sistema FCC y que la dimensión de su celda unidad es 4.049 A. ¿Cuál será su densidad? Densidad Densidad para BCC El radio es: Ejemplo.- La densidad de wolframio es 19,3 g/cm3 con masa atómica de 183,9 g/mol. Si cristaliza en una red de tipo BCC, calcular su radio atómico.
- 14. Densidad para BCC Para FCC Corresponde a BCC Ejemplo.- La masa atómica de un determinado elemento es 55,8 (g/mol). Sabiendo que su radio atómico es 1,24 A y su densidad, 7,9 g/cm. En qué red cristaliza en una BCC o FCC?
- 15. Ejemplo.- ¿Cual es el Factor de empaquetamiento atómico en el sistema cristalino hexagonal simple? Total de átomos 3 Altura = 2r EL volumen es: El FEA es:
- 16. Para plantearse el problema tenemos que pensar en el número de celdas que hay en 1 mm3 . Para un cristal BCC, el volumen de una celdilla es: El número de celdillas es: En cada celdilla hay 2 atomos Ejemplo.- Un metal cristaliza en la red cúbica centrada en el cuerpo BCC. Si su radio atómico es 1.24 manómetros. ¿Cuántos átomos existirán en 1 cm3?
- 17. Algunos metales y no metales pueden tener más de una estructura cristalina: un fenómeno conocido como polimorfismo. Si este fenómeno ocurre en un sólido elemental se denomina alotropía. La existencia de una estructura cristalina depende de la presión y de la temperatura exterior. El ejemplo más familiar es el carbono: el grafito es estable en condiciones ambientales, mientras que el diamante se forma a presiones extremadamente elevadas 4 Polimorfismo y alotropía
- 18. 5 Imperfecciones en sólidos Defectos de punto Puntuales Vacantes Intersticiales Impurezas Se fomentan por la acción de: Calentamiento Radiación con partículas Deformación plástica Desviación de la composición química
- 19. 5 Imperfecciones en sólidos Defectos de línea. Dislocaciones y disclinaciones El deslizamiento proporciona ductilidad al material
- 20. 5 Imperfecciones en sólidos Defectos superficiales Límites de grano Maclas Paredes de dominio Defectos superficiales
- 21. 5 Imperfecciones en sólidos Defectos de volumen Vacíos microscópicos Inclusiones de otras fases Defectos de apilamiento Defectos de volumen Porosidad
- 22. 6 Difución Importancia tecnológica en: Tratamientos térmicos: cementación, nitruración de aceros, control microestructura Homogenización de impurezas Microelectrónica: Dopado de semiconductores Modificación de vidrios y cerámicas Sinterización