3 d ciencias-profa_guadalupe
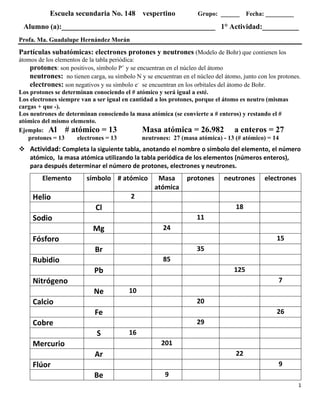
- 1. 1 Escuela secundaria No. 148 vespertino Grupo: ______ Fecha: _________ Alumno (a):__________________________________________ 1° Actividad:__________ Profa. Ma. Guadalupe Hernández Morán Partículas subatómicas: electrones protones y neutrones (Modelo de Bohr) que contienen los átomos de los elementos de la tabla periódica: protones: son positivos, símbolo P+ y se encuentran en el núcleo del átomo neutrones: no tienen carga, su símbolo N y se encuentran en el núcleo del átomo, junto con los protones. electrones: son negativos y su símbolo e- se encuentran en los orbitales del átomo de Bohr. Los protones se determinan conociendo el # atómico y será igual a esté. Los electrones siempre van a ser igual en cantidad a los protones, porque el átomo es neutro (mismas cargas + que -). Los neutrones de determinan conociendo la masa atómica (se convierte a # enteros) y restando el # atómico del mismo elemento. Ejemplo: Al # atómico = 13 Masa atómica = 26.982 a enteros = 27 protones = 13 electrones = 13 neutrones: 27 (masa atómica) - 13 (# atómico) = 14 ❖ Actividad: Completa la siguiente tabla, anotando el nombre o símbolo del elemento, el número atómico, la masa atómica utilizando la tabla periódica de los elementos (números enteros), para después determinar el número de protones, electrones y neutrones. Elemento símbolo # atómico Masa atómica protones neutrones electrones Helio 2 Cl 18 Sodio 11 Mg 24 Fósforo 15 Br 35 Rubidio 85 Pb 125 Nitrógeno 7 Ne 10 Calcio 20 Fe 26 Cobre 29 S 16 Mercurio 201 Ar 22 Flúor 9 Be 9
- 2. 2 Escuela secundaria No. 148 vespertino Grupo: ______ Fecha: _________ Alumno(a): ___________________________________________ 2° Actividad:__________ Profa. Ma. Guadalupe Hernández Morán Modelo de Bohr: costa de un núcleo donde se encuentran los protones más los neutrones (masa atómica) y de orbitales donde se colocan los electrones, los orbitales pueden ser de uno a varios, dependiendo el átomo del elemento que se quiera representar. El # atómico, determina el # de protones que será igualmente al # de electrones, porque el átomo es neutro (mismas cargas + que -). La masa atómica (se convierte a # enteros) y se resta el # atómico, nos dará el total de neutrones. FORMA DE LLENAR LOS ORBILALES Gases Nobles Número atómico 1° Orbital K 2° Orbital L 3° Orbital M 4° Orbital N 5° Orbital O 6° Orbital P Helio He 2 2 Neón Ne 10 2 8 Argón Ar 18 2 8 8 Critón Kr 36 2 8 18 8 Xenón Xe 54 2 8 18 18 8 Radón Ra 86 2 8 18 32 18 8 Modelos atómicos de Bohr Ejemplos: Helio He Flúor F Núcleo Núcleo 2° orbita Masa atómica = 4 electrón Masa atómica = 19 # atómico = 2 Se llena con solo 2 electrones # atómico = 9 1° orbita ❖Actividad: elabora el modelo de Bohr de los siguientes elementos, seguir el cuadro anterior para llenar los orbitales. Elemento Modelo de Bohr Elemento Modelo de Bohr Al Cl Ca Ne P+ = 2 N = 2 P+ = 9 N = 10
- 3. 3 Elemento Modelo de Bohr Elemento Modelo de Bohr K O Li C Na Br
- 4. 4 Escuela secundaria No. 148 vespertino Grupo: ______ Fecha: _________ Alumno (a):_____________________________________________ 3° Actividad:________ Profa. Ma. Guadalupe Hernández Morán Modelo de Lewis (cumpliendo la regla del octeto, no más de 8 electrones): reduerda primero colorar el símbolo del elemento y después sus electrones, que corresponde en número al grupo al que pertenese (tabla periódica), igual corresponden al # de átomos de la ultima orbita del modelo de Bohr, por ejemplo el Carbono que pertenese al grupo IV A, el número de puntos es 4, luego de colocar el simbolo, dibujar 4 puntos alrededor en forma de cruz, si son más, formar pares. ❖ Completa la tabla siguíente: Apóyate en la página 98 de tu libro de texto. Nombre del elemento Símbolo Grupo Modelo de Lewis Litio Magnesio Boro Silicio Oxígeno Flúor Neón Potasio Azufre Cloro C
- 5. 5 Escuela secundaria No. 148 vespertino Grupo: ______ Fecha: _________ Alumno (a):___________________________________________ 4° Actividad __________ Profa. Ma. Guadalupe Hernández Morán Formación de compuestos: enlace iónico y covalente (modelo de Lewis). Enlace Iónico es aquel en que se transfieren sus electrones de valencia (ultima orbita de modelo de Bohr), del de menor cantidad de electrones al de mayor (del menor al mayor elemento electronegativo), Además casi siempre se da entre un metal y un no metal (tabla periódica). Enlace Covalente es aquel que sus electrones de valencia se comparten, y se da principalmente entre no metales (tabla periódica). ❖ Actividad: completa la siguiente tabla. Sustancias Nombre Tipo Enlace Modelo de Lewis HCl H2O O2 NaCl CH4 MgCl2 AlCl3 H2 CO2 CaF2
- 6. 6 Escuela secundaria No. 148 vespertino Grupo: ______ Fecha: _________ Alumno (a):_____________________________________________ 5° Actividad: _______ Profa. Ma. Guadalupe Hernández Morán Definición de numero de oxidación El número de oxidaciónes unnúmero entero que representa el númerode electrones que unátomo pone enjuego cuandoformaun compuesto determinado • Elnúmerode oxidación es positivo sielátomo pierde electrones (se les llama cationes), o loscomparte con un átomo que tenga tendencia a captarlos. • Elnúmerode oxidación es negativo cuando elátomo gana electrones(se le llama aniones), o loscomparta con un átomo que tenga tendencia a ceder suselectrones. • El número de oxidación se coloca en la parte superior derecha de cada elemento, con su signo correspondiente. Ejemplos: H1+ Cl1- Ca2+ O2- K2 1+ O-2 O2 La comprobación de que está correcto el Número de Oxidación, si suma algebraica es igual a cero, recuerda que hay que multiplicar el número de oxidación, por el número de átomos presentes. Normas que se aplican para la determinación del número de oxidación de los átomos de un compuesto. El número de oxidación de un elemento libre es cero. Por ejemplo, los metales no disueltos (Cu, Zn, Al…) o los gases diatómicos (O2, Cl2, F2…). 1. En los iones de un único átomo, el estado de oxidación o número de oxidación de dicho átomo coincide con la carga del ion. Por ejemplo, en el caso de los alcalinos catiónicos el estado de oxidación es +1 (Li+ , Na+ , K+ …) y en el caso de los alcalinotérreos +2 (Ca+2 , Mg+2 …). Del mismo modo será para los demás metales, por ejemplo, en el Fe(II) el estado de oxidación es +2 y en el Fe(III) +3. 2. El número de oxidación del flúor, F, es siempre -1, por ser el átomo más electronegativo que existe. 3. El número de oxidación del oxígeno es siempre -2, con dos excepciones: 1. Cuando el oxígeno se combina con flúor, su número de oxidación es +2. 2. Cuando el oxígeno se halla formando un peróxido, como el peróxido de hidrógeno o agua oxigenada, H2O2, su número de oxidación es -1. 4. El número de oxidación del hidrógeno es siempre +1, excepto en los hidruros metálicos que es -1 (por ejemplo, hidruro sódico, Na H). 5. Algunos elementos tienen distinto estado de oxidación en función del compuesto que están formando. Por ejemplo, el estado de oxidación del nitrógeno en el monóxido de nitrógeno, NO, es +2, mientras que el estado de oxidación del nitrógeno en el dióxido de nitrógeno, NO2, es +4. 6. La suma algebraica de los números de oxidación de los elementos de un compuesto ha de ser igual a su carga, es decir: 1. Si es un compuesto neutro, la suma algebraica de sus números de oxidación será cero. 2..Si es un catión o un anión será igual a la carga del ion. Por ejemplo, en el caso del anión perclorato, ClO3 – la suma algebraica de los números de oxidación será -1. En este caso, el oxígeno tiene estado de oxidación -2, por lo que (-2)·3 = -6. De este modo, para que la suma algebraica sea -1, el estado de oxidación del cloro ha de ser +5. 7. Si el compuesto está formado por tres elementos diferente, se coloca primero el número de oxidación, de elementos presentes en los extremos siguiendo las reglas anteriores. Ejemplo; Ca+2 CO3 -2 y el número de
- 7. 7 oxidación del elemento de medio, será la cantidad y carga que falte, para que su suma algebraica sea cero, quedando el ejemplo Ca+2 C+4 O3 -2 Comprobación algebraica hay + 6 y -6 como hay 3 átomos de oxígeno, y estos se multiplican por el número de oxidación del oxígeno es -2, resultando un total de -6. La suma es igual a cero (significa que no hay cargas, es neutro) y esto es correcto. Apoyo: revisa la página de tu libro de texto página 223 a 225. ¿Quieres comprobar si has entendido estas normas y eres capaz de aplicarlas? Te sugiero ver YouTube el video de teoría y ejercicios relacionados con el número de oxidación. ❖ Actividad determina los números de oxidación de los siguientes compuestos, con su comprobación algebraica de cargas (igual a cero). Fe O C O2 Fe2 O2 H2 O Al Cl3 Ca Cl2 Na Cl Sc2 O3 K Mn O4 H2 S O4
- 8. 8 Escuela secundaria No. 148 vespertino Grupo: ______ Fecha: _________ Alumno(a):___________________________________________ 6° Actividad: __________ Profa. Ma. Guadalupe Hernández Morán Tema: Materiales elásticos. Apoyo en tu libro de texto páginas 200 y 201. Consulta vía internet. ❖ Actividad: contesta el siguiente cuestionario. 1. ¿Qué es un Polímero (resumen)? 2. ¿Qué es un monómero (lo más breve posible)? 3. ¿Qué es un plástico? 4. ¿Qué significa sintetizar un material elástico? 5. ¿Qué tipos de materiales elásticos encontramos en la naturaleza? 6. ¿Qué beneficios brinda a la sociedad sintetizar estos materiales? 7. ¿Qué objetos elásticos encontramos en nuestra vida cotidiana? 8. ¿Cuáles son las ventajas y desventajas de utilizar dichos materiales? 9. ¿Qué estado físico tienen los materiales elásticos? 10. ¿Cómo elaborar un material aláctico? Observación: anota tus respuestas en una hoja mínimo y máximo dos. _____________________________________________________________________________ Escuela secundaria No. 148 vespertino Grupo: ______ Fecha: _________ Alumno(a):___________________________________________ 7° Actividad: __________ Profa. Ma. Guadalupe Hernández Morán Tema: ¿Cuáles son los beneficios y riesgos del uso de fertilizantes y plaguicidas? Apoyo en tu libro de texto páginas 252. Consulta vía internet. ❖ Actividad • Utiliza media cuartilla de la hoja para escribir qué son los fertilizantes ¿cuáles son los beneficios y los perjuicios que ocasionas? • En la otra cuartilla de la misma hoja anotar qué son los plaguicidas, beneficios y los riesgos o perjuicios que ocasionan los plaguicidas.
