05 Enlace2009
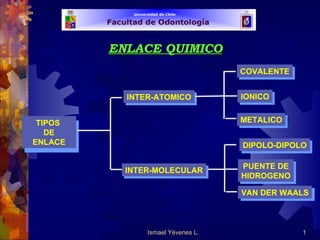
- 1. Ismael Yévenes L. TIPOS DE ENLACE INTER-MOLECULAR INTER-ATOMICO ENLACE QUIMICO DIPOLO-DIPOLO PUENTE DE HIDROGENO VAN DER WAALS COVALENTE IONICO METALICO
- 2. Ismael Yévenes L. ENLACE COVALENTE ENLACE COVALENTE: Los átomos que forman el enlace aportan un orbital atómico y un electrón formando un orbital molecular con un par de electrones compartidos. Descrito por Gilbert Newton Lewis. O 2 ; N 2 ; CH 4 : Moléculas fuertemente unidas y estables. ENLACE COVALENTE PURO ENLACE QUELATOS ENLACE COVALENTE COORDINADO
- 3. Ismael Yévenes L. Configuración Electrónica y Notación de Lewis .. .. . . . . . . . . . . . . . .
- 4. Ismael Yévenes L. Formación de Enlace Apareamiento de espines de orbitales atómicos a medio llenar. Electrones con espines apareados no participan en el enlace Molécula de Hidrógeno: H : H H 2 Molécula de Agua: H : Ö : H 2 O H Molécula de Amoníaco: H : N : H NH 3 H .. .. ..
- 5. Ismael Yévenes L. Covalencia. El número máximo de enlaces covalentes que puede formar un átomo es igual al número de orbitales a medio llenar que posee. Hidrógeno: 1 Boro: 3 Carbono: 4 Nitrógeno: 3 Interpretación Mecanocuántica de Formación de H 2 Componentes: 2 protones, 2 electrones y 2 núcleos. Núcleos: Repulsión. Electrones: Atracción con espines opuestos (M s = + 1/2 ; - 1/2) Núcleo - Nube Electrónica: Atracción. Resolución Energética: Ecuación de Schröedinger Representación de Lewis: Nube de electrones apareados entre los núcleos. - h H + V = E 8 · · m
- 6. Ismael Yévenes L. Los orbitales 1s se traslapan formando un orbital molecular, un orbital simétrico, el cual se designa con la letra griega H Cl . . . . Cl Cl 1s 3p 3p 3p
- 7. Ismael Yévenes L. Hibridación Configuración Basal C: 1s 2 2s 2 2p x 1 2p y 1 2p z 0 = Covalencia 2. Configuración Excitada C: 1s 2 2s 1 2p x 1 2p y 1 2p z 1 = Covalencia 4. Orientación Espacial: los orbitales p se orientan perpendicularmente entre sí, formando ángulos de 90°, los orbitales s no tienen orientación. . . . .
- 8. Ismael Yévenes L. Reorganización de Orbitales s + p + p + p sp 3 + sp 3 + sp 3 + sp 3 = 4 sp 3 Orbital híbrido, ángulo de enlace de 109° y orientación tetraédrica regular. Representación de la Molécula de Metano. H H H H 109º . C : H . . . H . . H H c H H H H
- 9. Ismael Yévenes L. Hibridación Tetraédrica: El átomo de carbono presenta hibridación sp 3 , el hidrógeno tiene un orbital s, luego se forman cuatro enlaces moleculares sigma sp 3 . Hibridación Trigonal: Este orbital esta compuesto por un orbital s y 2 orbitales p. S + p + p sp 2 + sp 2 + sp 2 = 3 sp 2 Los orbitales híbridos son coplanares, se ubican formando ángulos de 120° y orientados hacia los vértices de un triángulo equilátero. El orbital p libre se orienta perpendicularmente al plano de los orbitales sp 2 .
- 10. Ismael Yévenes L. H H s s C = sp 2 sp 2 sp 2 p z C = sp 2 sp 2 sp 2 p z s s H H Representación de la Molécula de Eteno. El eteno presenta: 5 enlaces sigma : 4 s - sp 2 (C-H) y 1 sp 2 - sp 2 (C-C); 1 enlace pi ( p) : superposición de orbitales p, densidad electrónica por encima y por debajo del eje de núcleos, mas débil que s. 120º C C H H H H
- 11. Ismael Yévenes L. Hibridación Digonal: Participación de un orbital s y un orbital p s + p sp + sp = 2 sp La orientación del orbital híbrido es lineal, con un ángulo de enlace de 180°. Los orbitales p libres se orientan perpendicularmente entre sí y con el orbital sp. Representación de la Molécula de Etino: CH = CH H --C ---------------C-- H Tipos de Enlace: Tres enlaces sigma, dos sp-s (C-H) y uno sp-sp (C-C). Dos enlaces pi. H s C = sp sp py pz C = sp sp py pz s H
- 12. Ismael Yévenes L. Enlace Covalente Coordinado. El enlace está formado por electrones aportados por un átomo y por otro átomo que aporta su orbital vacío. H 3 N : + H + NH 4 + Quelantes: Moléculas con varios átomos capaces de ceder pares de electrones. Quelato: Molécula formada por un catión y un quelante. H H : N : H H .. ..
- 13. Ismael Yévenes L. H 2 N - CH 2 - CH 2 - NH 2 : Etilendiamina; ésta molécula forma dos enlaces covalentes coordinados con átomos metálicos, siendo el átomo dador de electrones el agente de quelación. H 2 C - H 2 N: :NH 2 - CH 2 Cu 2+ H 2 C - H 2 N: :NH 2 - CH 2 Nomenclatura de Enlaces. Enlace covalente no polar u homopolar entre átomos iguales. Enlace covalente semipolar entre átomos diferentes. Enlace iónico o heteropolar entre átomos diferentes con transferencia de electrones y formación de iones. El grado de polaridad lo determina la electronegatividad de los átomos.
- 14. Ismael Yévenes L. H 2,1 Li Be B C N O F 1,0 1,5 2,0 2,5 3,0 3,5 4,0 Na Mg Al P S Cl 0,9 1,2 1,5 2,1 2,5 3,0 K Ca Br 0,8 1,0 2,8 Escala de Electronegatividades (E.N.) Cuanto mayor sea la diferencia de E.N., mayor será el carácter polar de la molécula, diferencias mayores a 1,6 se considera iónico.
- 15. Ismael Yévenes L. Uniones Intermoleculares. Atracción Dipolar: Asociación de moléculas por interacción de cargas, inducción de cargas parciales por diferencia de E.N. A + --- B - Enlace de Hidrógeno: Enlace dipolar entre un átomo de hidrógeno de una molécula y un átomo de F, O o N de otra molécula. Factores en la formación del enlace: la diferencia de E.N. Entre el H y otros átomos desplaza electrones hacia el H. El tamaño del H permite a otros átomos acercarse al átomo de H de otra molécula. H -- O- - - H H- - - O -- H O O O O C H C H C O O O
- 16. Ismael Yévenes L. Este enlace explica las propiedades del agua, alcoholes, fenoles, ácidos carboxílicos. Enlace de Van der Waals Son dipolos temporales o de inducción de carga temporal. Tendencia de moléculas a inducir dipolos por deformación del orbital molecular. + - Dipolo temporal Las moléculas grandes se polarizan más fácilmente que las pequeñas, las fuerzas de Van der Waals aumentan con el peso molecular.
