Alquinos y dienos reloaded
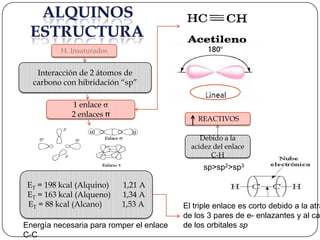
- 1. H. Insaturados Interacción de 2 átomos de carbono con hibridación “sp” 1 enlace 2 enlaces REACTIVOS Debido a la acidez del enlace C-H sp>sp2>sp3 ET = 198 kcal (Alquino) 1,21 A ET = 163 kcal (Alqueno) 1,34 A ET = 88 kcal (Alcano) 1,53 A El triple enlace es corto debido a la atra de los 3 pares de e- enlazantes y al ca Energía necesaria para romper el enlace de los orbitales sp C-C
- 2. Generación de un triple enlace Deshidrohalogenación de Dihalogenuros Vecinales Br 2 H3C KOH (alc) NaNH2 H3C Br H3C H3C CH CH2 Br Propino Br 1,2-dibromopropano 1-Bromo - 1- Propeno Bromuro de Propileno Reacción de Acetiluros Metálicos con Halogenuros de alquilo R C C Na + R' Br R C C R' + NaBr R = R' o R distinto a R'
- 3. Son compuestos APOLARES Molécula Fuerzas de Van Der Waals s unidas Insolubles en agua Solubles en disolventes orgánicos de baja polaridad: éter, benceno, tetracloruro de carbono Pto. De Fusión # de C Pto. De Ebullición # de ramificaciones Densidad
- 4. ALQUINOS REACTIVIDAD Electrofílica “Carbocatión” ADICIÓN ÁCIDO-BASE Hidrogenaci Formación de ón Acetiluros Metálicos Halogenació n A. ½ ácido Halogenuros de Hidrógeno Tautomeros Adición de Agua Cuando más pequeño el pKa + ácido
- 5. UV-VIS (400-800 nm) π-π* Absorción final cerca de 200nm RMN Tipo de Desplazamiento Tipo de Carbono Desplazamie Hidrogeno Químico nto Químico Alquino RC≡CH 1,7 – 3,1 65 – 85
- 6. INFRARROJO Vibraciones Moleculares Grupo (Cromóforo Intensida Rango (cm-1) Hidrocarbonado) d C-H (tensión) s ~3300 C-H (enlace) s ~630 C-C (tension del enlace multiple) Alquino Monosustutido m 2140-2100 Alquino Disustituido v,m 2260-2190
- 7. Un hidrocarburo con dos dobles enlaces es un dieno: Este tipo de compuestos pueden ser aislados, conjugados o acumulados. Propiedades físicas El 1,3 – butadieno o divinilo es un gas fácilmente licuable (a – 5°C). El – 2 – metil – 1,3 – butadieno, o isopreno es un líquido de fácil ebullición. Propiedades químicas Los hidrocarburos diénicos, disponiendo de dobles enlaces en las moléculas, causan reacciones de adición corrientes, por ejemplo, decoloran el agua de bromo, adicionan haluros de hidrógeno, etc.
- 8. CALOR DE HIDROGENACIÓN DE LOS ENLACES CONJUGADOS. Cuanto menos calor se libera durante la hidrogenación, se considera que el compuesto es más estable. Los dobles enlaces conjugados tienen una estabilidad extra. Obtención de los dienos Por deshidrogenación del alcanos. Mediante el cracking de hidrocarburos. Por el proceso de deshidratación y desdidrogenación de alcohol etílico.
- 9. LA REACCIÓN DE DIELS-ALDER. También recibe el nombre de cicloadición [4+2] porque se forma un anillo por la interacción de cuatro electrones pi del alqueno con dos electrones pi del alqueno o del alquino.
- 10. TRASLAPAMIENTO DEL ORBITAL DE LA REACCIÓN DE DIELS-ALDER. El mecanismo de la reacción de Diels-Alder es concertado, todos los enlaces se rompen y se forman en un solo paso. Se mueven simultáneamente tres pares de electrones, lo que requiere un estado de transición con traslapamiento entre los orbitales p extremos del dieno y los del dienófilo. Los requisitos del estado de transición determinarán la estequiometría del producto
- 11. ESPECTRO UV Utilizado en dienos, gracias a sus transiciones electrónicas y a su estabilidad cuando están conjugados Espectro de UV del isopropeno en metanol muestra λmáx = 222 nm, ε = 20.000. 1 = : 217 nm isopropeno 2 = : 268 nm La altura del pico cambiará dependiendo de la concentración de la muestra y de la longitud del paso, pero la longitud de onda a la que se encuentra (I) no cambiará. Adviértase que la adición de enlaces dobles conjugados aumenta λ.
- 12. Alarg.: CSP2 – H 3600- 3300 C=C 1600- 1675 Flex: =C-H 1000- 650 Realizado por: Bibliografía: Carlos Puente Wade Jr. Química Orgánica Jhon Sucuy Carey Francis, Química Orgánica
