2. Proteinas.pdf
- 1. Estructura y propiedades físicoquímicas de las Proteínas, Péptidos y Aminoácidos Dra. Ligbel Sanchez Castillo
- 2. Niveles de organización proteica • Estructura primaria • Estructura secundaria • Estructura terciaria • Estructura cuaternaria
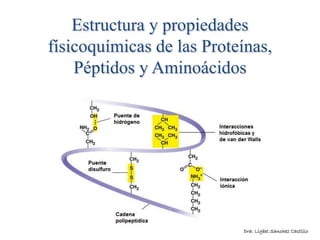
- 3. Enlaces responsables de los niveles de organización de las proteínas • Enlaces fuertes: - Enlace peptídico - Enlace disulfuro • Enlaces débiles: - Enlaces puente de hidrógeno - Interacciones hidrofóbicas - Fuerzas electrostáticas - Fuerzas de Van Der Waals
- 5. Estructura primaria • Define el orden de los aminoácidos, y la ubicación de los enlaces disulfuros en las cadenas polipeptídicas. • La secuencia de A,A de la estructura primaria puede predecirse a partir del gen que codifica a la proteína. • Se puede apreciar el A,A con el grupo amino terminal y el que contiene el grupo carboxilo terminal. • Si existen varias cadenas se identifican con las letras griegas alfa, beta, gamma,etc. 1 4 3 2 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Amino terminal Carboxilo terminal
- 7. • Está caracterizada por conformaciones regulares, que pueden encontrarse en toda o en una parte de la proteína. • La planaridad del enlace peptídico y el impedimento estérico derivado de la cadena lateral R, hace que la proteína adopte la forma de resorte. • Los enlaces puente de hidrogeno le dan la estabilidad a la estructura. • Existen varios tipos: -hélice, hoja plegada o lámina (paralela o antiparalela). Estructura secundaria
- 8. • Espiral en el mismo sentido de las manecillas del reloj. • Cada vuelta contiene de 3 a 6 residuos de A,A. • Es una configuración elástica. • La estructura secundaria es más estable y de menor energía que la cadena polipeptídica (estructura primaria).
- 10. Hoja plegada o lámina beta • Los segmentos de la cadena se disponen lado a lado en forma casi completamente extendida. • Formada por enlaces puente de hidrógeno entre los "O " carbonílicos y los " H " amídicos de dos o más cadenas polipeptídicas extendidas y adyacentes. • Disposición en zig-zag. • Pueden ser: paralelas o antiparalelas.
- 11. Lámina -paralela Lámina -antiparalela
- 12. Triple hélice • El colágeno es el ejemplo característico. • Espiral enrollado de tres subunidades polipeptídicas. • Cada unidad polipeptídica o cadena alfa está torcida en una hélice con giro a la izquierda de 3 residuos por vuelta. • La triple hélice del colágeno está estabilizado por múltiples enlaces cruzados intercatenarios entre residuos de lisina y de hidroxilisina.
- 13. • Está caracterizada por plegamientos a distancia. • Está constituída por varios “DOMINIOS". • Además de enlaces puente de hidrógeno, se anexan las interacciones hidrófobas, fuerzas de Van Der Waals y las fuerzas electrostáticas. • Ejemplo: la mioglobina. Estructura terciaria
- 14. Mioglobina
- 15. • Se refiere al ensamblaje de dos o más cadenas polipeptídicas separadas, unidas mediante interacciones o entrecruzamientos no covalentes. • El conjunto se denomina oligomero. • Las cadenas peptídicas se denominan monómeros o subunidades . • Participan todos los enlaces débiles. Estructura cuaternaria
- 19. FACTORES DE ESTABILIDAD QUE MANTIENEN A LAS PROTEÍNAS EN SOLUCIÓN (COLOIDES) • Atmósfera hidratante • Carga neta (+) ó (-) PRECIPITACIÓN • Con desnaturalización • Sin desnaturalización
- 20. Desnaturalización Desorganización de la conformación nativa o biológicamente activa de una proteína, que tiene lugar cuando se cambia el entorno. Agentes desnaturalizantes: • Cambios extremos de pH. • Calentamiento. • Úrea, detergentes, cloruro de guanidino,etc.
- 21. Hidrólisis H2O Ruptura del enlace amida (enlace peptídico) al agregar agua, con la respectiva regeneración de los A,A constituyentes.
- 22. Clasificación de las proteínas • De acuerdo a sus funciones. • De acuerdo a su solubilidad. • De acuerdo a su conformación. • De acuerdo a su composición.
- 23. De acuerdo a sus funciones • Catalíticas • Estructurales • Contráctiles • De defensa natural • Digestivas • De transporte • Hormonales • Del ADN • Cromosómicas • De la membrana- receptores • Ribosómicas • De almacenamiento • Tóxicas o de toxinas • De la visión
- 24. De acuerdo a su solubilidad Albúminas: • Son de origen animal. • Solubles en agua destilada. • Precipitan en slns. salinas saturadas. • PM: < 70.000 Daltons Globulinas: • Son de origen vegetal y animal. • Insolubles en agua destilada. • Precipitan en slns. medio saturadas de sales. • PM: > 150.000 Daltons Histonas: • Son de origen vegetal o animal. • Solubles en agua destilada y ácidos diluídos. • Precipitan por adición de amoníaco. • Están unidas al ADN en el núcleo celular. Protaminas: • Son de origen animal. • Solubles en agua destilada, slns. Salinas, ácidos y bases. • PM: 6.000 Daltons. • Están unidas a otras proteínas para formar complejos de alto PM.
- 25. De acuerdo a su conformación Proteínas fibrosas • Generalmente insolubles en agua. • Tienen formas moleculares muy alargadas. • Conjunto de cadenas polipeptídicas largas, dispuestas a manera de haz. • Resistentes a la desnaturalización. • Poseen uniones intermoleculares fuertes. • Material estructural de los tejidos • Ej.: Colágeno, elastina, queratina Proteínas globulares • Solubles en agua o slns. salinas. • Estructura compacta. • Poseen estructuras casi esféricas a elípticas. • Se desnaturalizan fácilmente. • Fuerzas intermoleculares débiles. • Regulan procesos vitales. • Ej.: Hemoglobina, enzimas, inmunoglobulinas, miosina, fibrinógeno.
- 26. De acuerdo a su composición Proteínas simples o no conjugadas • Sólo tienen material polipeptídico. • No poseen adherido ningún grupo no proteico. Proteínas conjugadas • El componente polipeptídico se encuentra asociado con un componente no peptídico, orgánico o inorgánico, llamado grupo prostético.
- 27. Clasificación de las proteínas Proteínas simples •Fibrosas •Globulares •Albúmina •Globulina Proteínas conjugadas • Glicoproteínas • Metaloproteínas • Hemoproteínas • Flavoproteínas • Fosfoproteínas • Nucleoproteínas • Lipoproteínas •Colágeno •Elastina •Queratina
- 28. PROTEÍNAS SIMPLES: PROTEÍNAS FIBROSAS COLÁGENO: - La unidad básica de la fibra del colágeno es la molécula de tropocolágeno. - Forma parte del tejido conectivo, tejido que precisa resistencia o dureza. - Es una triple hélice formada por 3 hélices polipeptídicas enrolladas entre sí. Cada hélice con aprox. 1000 residuos. - Es rico en los A,A: Glicina, lisina, prolina, hidroxiprolina. La hidroxilisina es poco frecuente. - Es más estable mientras tenga más restos de prolina y lisina.
- 30. ELASTINA: - Proteína fibrosa flexible. - Se encuentra en el tejido conectivo elástico (ligamentos, vasos sanguíneos arteriales). - Formada por los A,A: Glicina, leucina, isoleucina, prolina, y poca cantidad de hidroxiprolina. - Carece de hidroxilisina.
- 31. QUERATINA: - Proteína insoluble en los animales, derivadas de las células del ectodermo. - Están incluídas en este tipo los elementos proteicos estructurales de la piel, así como los derivados biológicos del ectodermo (pelo, plumas, lana, escamas,uñas). - Existen dos clases de queratinas con secuencia de A,A y funciones similares: -queratinas y -queratinas. - Las -queratinas son las proteínas más importantes del pelo y las uñas y forman parte importante de la piel del animal. - Las -queratinas son miembros de un gran grupo de proteínas filamentosas intermedias, que desempeñan funciones estructurales en los núcleos, citoplasmas y superficie de muchas células.
- 32. QUERATINA
- 33. • Glucoproteínas (Ej.: grupos sanguíneos). • Metaloproteínas (Ej.: enzima anhidrasa carbónica posee Zn). • Hemoproteínas (Ej.: hemoglobina, mioglobina, citocromos, catalasa). • Flavoproteínas (Ej.: succinato deshidrogenasa-FAD). • Fosfoproteínas (Ej.: caseína de la leche). • Nucleoproteínas (Ej.: cromatina). • Lipoproteínas (Ej.: quilomicrones, VLDL, LDL,HDL). PROTEÍNAS CONJUGADAS
- 34. HEMOPROTEÍNAS • GRUPO PROSTÉTICO: HEM Nucleo coloreado tetrapirrólico, formado por cuatro unidades de piorrol, conectadas a modo de anillo por puentes metenilo. La estructura es planar y en el centro tiene un átomo de hierro. Fe+2
- 35. - Hemoproteína presente en eritrocitos. - Grupo proteico: Globina (Dos cadenas alfa y dos beta). - Grupo prostético: Hem o Hemo. - Función: Transporte de oxígeno del aparato respiratorio a los tejidos, y CO2 desde los tejidos a los pulmones para ser excretado. HEMOGLOBINA
- 36. - Hemoproteína presente en tejido muscular. - Grupo proteico: Una sola cadena polipeptídica. - Grupo prostético: Hem o Hemo. - Función: Fija y almacena O2 cuando la concentración del mismo es alta, y lo libera cuando las células así lo requieran. MIOGLOBINA
- 37. - Hemoproteína con actividad enzimática. - Grupo prostético: Hem o Hemo. - Función: Actúan como agentes de transferencia de electrones en las reacciones de oxido-reducción de la cadena respiratoria. - Ejemplos: Cit b, Cit c1, Cit c, Cit aa3, Cit P450. CITOCROMOS
- 38. - Hemoproteína con actividad enzimática. - Grupo prostético: Hem o Hemo. - Función: Degrada el peróxido de hidrógeno en agua y oxígeno.. CATALASA
- 39. FLAVOPROTEÍNAS • GRUPO PROSTÉTICO: Mononucleótido de flavina (FMN) o dinucleótido de flavina y adenina (FAD). • Se forma en el cuerpo a partir de la vitamina B5 o riboflavina. • Numerosas enzimas son flavoproteínas o metaloflavoproteínas.
- 40. LIPOPROTEÍNAS • GRUPO PROTEICO: Apolipoproteína o apoproteína (Apo B48, apo B100, apo A). • GRUPO PROSTÉTICO: Nucleo lipídico. • Función: Transporte de lípidos por el torrente circulatorio. • Tipos: Quilomicrón, VLDL, LDL, HDL.
- 41. https://www.youtube.com/watch?v=qAGQvmtQEMM https://www.youtube.com/watch?v=e2OW6U3x0Vs Ver estos videos de repaso Lección Escrita