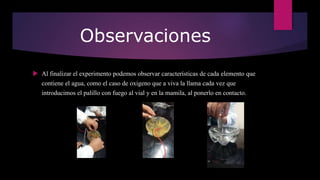
Este documento describe un experimento de laboratorio para sintetizar agua a partir de hidrógeno y oxígeno. Los estudiantes utilizaron electrodos de níquel, agua oxigenada y sal para separar el agua en sus elementos constituyentes mediante electrólisis. Luego verificaron la presencia de hidrógeno y oxígeno observando que el hidrógeno es combustible y el oxígeno aviva la llama. Al reunir ambos gases, se vuelve a formar agua, demostrando que es un compuesto de dichos elementos.