Clase de química los óxidos. Dulce y Nadiuzca
•Descargar como PPTX, PDF•
0 recomendaciones•361 vistas
Los oxidos
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Destacado
2014-10-29_La eficiencia energética y la certificación medioambiental LEED

2014-10-29_La eficiencia energética y la certificación medioambiental LEEDAlex Ciurana Fenes, CEM, CMVP
Destacado (12)
Articulo kardex, una herramienta de gestión de inventarios

Articulo kardex, una herramienta de gestión de inventarios
2014-10-29_La eficiencia energética y la certificación medioambiental LEED

2014-10-29_La eficiencia energética y la certificación medioambiental LEED
Elective Care Conference: the role of the MDT coordinator role 

Elective Care Conference: the role of the MDT coordinator role
Elective Care Conference: welcome and opening address

Elective Care Conference: welcome and opening address
Elective care conference: imaging demand and capacity 

Elective care conference: imaging demand and capacity
Similar a Clase de química los óxidos. Dulce y Nadiuzca
Similar a Clase de química los óxidos. Dulce y Nadiuzca (20)
Formulación y nomenclatura de óxidos básicos y ácidos

Formulación y nomenclatura de óxidos básicos y ácidos
Guía de compuestos binarios abril 2014 colegio san josé 3° años

Guía de compuestos binarios abril 2014 colegio san josé 3° años
Compuestos Químicos, Nomenclatura y reacciones de obtención

Compuestos Químicos, Nomenclatura y reacciones de obtención
Último
Último (20)
Clasificaciones, modalidades y tendencias de investigación educativa.

Clasificaciones, modalidades y tendencias de investigación educativa.
Resolucion de Problemas en Educacion Inicial 5 años ED-2024 Ccesa007.pdf

Resolucion de Problemas en Educacion Inicial 5 años ED-2024 Ccesa007.pdf
TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx

TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf
ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...

ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...
ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx

ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
Clase de química los óxidos. Dulce y Nadiuzca
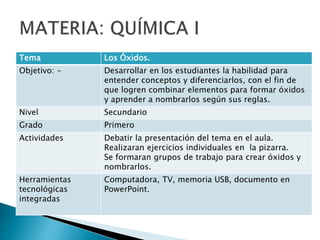
- 1. Tema Los Óxidos. Objetivo: - Desarrollar en los estudiantes la habilidad para entender conceptos y diferenciarlos, con el fin de que logren combinar elementos para formar óxidos y aprender a nombrarlos según sus reglas. Nivel Secundario Grado Primero Actividades Debatir la presentación del tema en el aula. Realizaran ejercicios individuales en la pizarra. Se formaran grupos de trabajo para crear óxidos y nombrarlos. Herramientas tecnológicas integradas Computadora, TV, memoria USB, documento en PowerPoint.
- 2. LOS ÓXIDOS SON COMPUESTOS BINARIOS FORMADOS POR LA COMBINACION DEL OXÍGENO CON OTROS ELEMENTOS (MATÁLICOS O NO METÁLICOS).
- 3. Elemento a combinar Símbolo del Oxígeno Ex Oy Estado de Oxidación Valencia del o Valencia del Oxígeno elemento en cuestión E
- 4. De acuerdo al tipo de elemento que se combine con el oxígeno, se pueden clasificar en : Óxidos Ácidos o Anhídridos. Óxidos Básicos.
- 5. Óxidos Ácidos Combinación del oxígeno con un elemento no metálico. Aquí el oxígeno actúa con valencia 2 y el no metal con algunas de sus valencias positivas.
- 6. Óxidos Básicos Están formados por la combinación del oxígeno con un elemento metálico. En éstos el oxígeno actúa con valencia 2, mientras que el metal actúa con cualquiera de sus valencias o estados de oxidación. Su nombre es porque al reaccionar con el agua se produce una base.
- 7. Para los óxidos Básicos Actualmente se utiliza la Nomenclatura de Stock, para nombrarlos. Para nombrar los óxidos ácidos Se utiliza la Nomenclatura Estequiométrica
- 8. Para nombrar a los óxidos básicos, se utiliza la siguiente regla: 1. Si el metal tiene un solo estado de oxidación: se escribe primero la palabra ÓXIDO y luego el nombre del Metal. Ej: CaO= óxido de Calcio 2 . Si el metal tiene dos (2) estados de oxidación diferentes, se escribe la palabra óxido y al metal se le agrega la terminación oso para el menor estado de oxidación e ico para el mayor. Ej. Co2 + O2 = CoO óxido cobaltoso Co3 + O2 = Co2O3 óxido cobáltico
- 9. 3. Si el metal tiene más de dos estados de oxidación diferente, se escribe la palabra oxidación el nombre del metal y al lado entre paréntesis en número romano el estado de oxidación correspondiente. Ej: FeO= Óxido de hierro (II) Fe2O3 = Óxido de hierro (III)
- 10. Para retroalimentar lo aprendido en el día de hoy, haremos lo siguiente: Un resumen del tema tratado y enviar a la maestra por E-mail o WhatsApp. Además vamos a formular y nombrar algunos óxidos básicos, utilizando una tabla periódica científica digital (utilizar google).