Este documento resume los principales conceptos del equilibrio químico, incluyendo: 1) la ley de acción de masas y la constante de equilibrio, 2) los equilibrios homogéneos y heterogéneos, 3) cómo evoluciona un sistema químico hacia el equilibrio, y 4) cómo se ven afectados los sistemas químicos en equilibrio por cambios en la concentración, temperatura y presión según el principio de Le Chatelier.



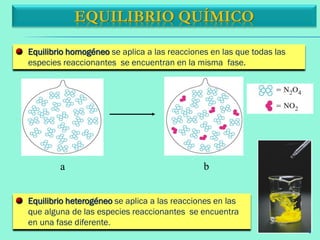
![2NO2(g) N2O4(g)
V directa
V indirecta
EQUILIBRIO QUÍMICOVelocidad
Vd = V i
[NO2]
[N2O4]
5](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-5-320.jpg)
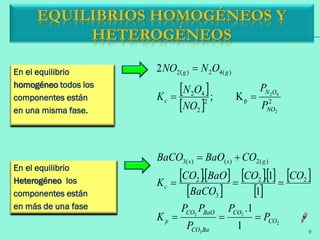
![Ley de acción de masas: Guldberg y
Waage establecieron que, cuando
un sistema alcanza el estado de
equilibrio, el cociente entre la
concentración de los productos de
la reacción y la concentración de los
reactivos, elevado cada uno a su
coeficiente estequiométrico, tenía
un valor constante, a una
temperatura determinada
CONSTANTE DE EQUILIBRIO
QUÍMICO Y LAM
A + 2 B n AB2
vd= kd [A][B]2
vr = kr [AB2]
Vd = Vr
kd[A][B]2 = kr[AB2]
2d
c 2
r
ABk
K = =
k A B
7](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-7-320.jpg)





![EQUILIBRIOS EN VARIAS ETAPAS
Hay procesos que pueden tener lugar de forma
encadenada, si se dan las circunstancias idóneas
A: N2 (g) + O2 (g) ↔ 2 NO (g) KA = 4,3 . 10 -25
B: 2 NO(g) + O2 (g) ↔ 2 NO2 (g) KB = 6,4 . 10 9
A+B: N2 (g) + 2O2 (g) ↔ 2 NO2 (g)
KA =
𝐍𝐎 𝟐
𝐍 𝟐
.[𝐎𝟐]
KB =
𝐍𝐎 𝟐
𝟐
𝐍𝐎 𝟐
.[𝐎𝟐]
KA+B =
𝐍𝐎 𝟐
𝟐
𝐍 𝟐
. 𝐎 𝟐
𝟐 =
𝐍𝐎 𝟐
𝐍 𝟐
.[𝐎𝟐]
.
𝐍𝐎 𝟐
𝟐
𝑵𝑶 𝟐
.[𝐎 𝟐
]
= KA . KB
14](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-14-320.jpg)
![
n
cp
n
cp
cp
n
cp
)mn()yx(
cmmnn
yyxx
m
B
n
A
y
D
x
C
p
i
m
B
n
A
y
D
x
C
pmn
yx
c
)RT(KK0nsi
)RT(KK0nsi
KK0nsi
)RT(KK
)RT(K
)RT(]B[)RT(A
)RT(D)RT(C
PP
PP
K
RT]c[RT
V
n
P:dondedenRTPV
PP
PP
K
BA
DC
K
yDxCmBnA
RELACIÓN ENTRE KC Y KP
15](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-15-320.jpg)







![Cuando a un sistema en equilibrio experimenta un
cambio en la concentración de alguna de las sustancias
que lo integran, evoluciona oponiéndose a la causa que
provocó esa alteración
Si agrego productos: Q > Kc ⟶ se desplazará a la
izquierda
Si agrego reactivos: Q < Kc ⟶ se desplazará a la
derecha
[reac]
[prod]
;
[reac]
[prod]
K
eq
eq
c Q
CAMBIO EN LA CONCENTRACIÓN DE
ALGUNA DE LAS SUSTANCIAS
23](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-23-320.jpg)

![ADICIÓN DE UN GAS INERTE (a T y V ctes)
No altera el equilibrio V/n
V/n
[reac]
[prod]
reac
prod
ADICIÓN DE UN REACTIVO/PRODUCTO
SÓLIDO O LÍQUIDO
No altera el equilibrio
25](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-25-320.jpg)

![ a)
b)
c)
d)
2
2
2 4
[ ]
[ ]
c
NO
K
N O
2
2
2
[ ]
[ ] [ ]
c
NOCl
K
NO Cl
2[ ]cK CO
2 2[ ] [ ]cK CO H O
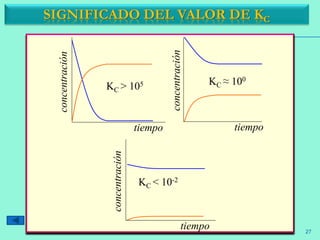
Ejemplo: Escribir las expresiones de Kc para los siguientes
equilibrios químicos:
a) N2O4(g) = 2 NO2(g)
b) 2 NO (g) + Cl2 (g) = 2 NOCl (g)
c) CaCO3 (s) = CaO (s) + CO2 (g)
d) 2 NaHCO3 (s) = Na2CO3 (s) + H2O (g) + CO2 (g)
28](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-28-320.jpg)


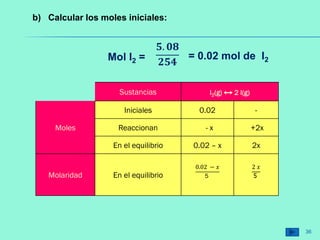
![Ejercicio 6: En un reactor de 2.5 litros se introducen 72 gramos de
SO3. Cuando se alcanza el equilibrio: SO3 (g) ↔ SO2 (g) + ½ O2 (g),
y a 200 ºC, se observa que la presión total del recipiente es de 18
atm. Calcula Kc y Kp para el equilibrio anterior a 200 ºC.
Sustancias SO3 (g) ↔ SO2 (g) + ½ O2 (g)
Moles
Iniciales 72/80 - -
Reaccionan -1x +1x +1/2x
En el equilibrio 0.9 – x +x +1/2x
Molaridad En el equilibrio
0.9 − 𝑥
2.5
𝑥
2.5
1
2
𝑥
2.5
nTotal = 0,9 –x +x +1/2 x
nTotal = 0,9 +1/2 x
Kc =
𝑺𝑶 𝟐
. 𝑶 𝟐
𝟏
/
𝟐
[𝑺𝑶 𝟑
]
P Total . V = n Total .R.T
18. 2,5 = (0,9+1/2x).0,082.(200+273) x= 0,52 mol
(sustituyendo)
0,152 0,208 0,104
31](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-31-320.jpg)

![Ejemplo: En un matraz de 5 litros se introducen 2 moles de PCl5(g) y 1 mol de de
PCl3(g) y se establece el siguiente equilibrio:
PCl5(g) ↔ PCl3(g) + Cl2(g)
Sabiendo que Kc (250 ºC) = 0,042
a) ¿cuáles son las concentraciones de cada sustancia en el equilibrio?
b) ¿cuál es el grado de disociación?
Sustancias PCl5(g) ↔ PCl3(g) + Cl2(g)
Moles
Iniciales 2 1 -
Reaccionan - x +1x +1x
En el equilibrio 2 – x 1+ x x
Molaridad En el equilibrio
2 − 𝑥
5
1 + 𝑥
5
𝑥
5
Kc =
𝑷𝑪𝒍 𝟑
. 𝑪𝒍 𝟐
[𝑷𝑪𝒍 𝟓
]
33](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-33-320.jpg)
![a) Kc =
𝑷𝑪𝒍 𝟑
. 𝑪𝒍 𝟐
[𝑷𝑪𝒍 𝟓
]
=
𝟏+𝒙 .𝒙
𝟐𝟓
[𝟐−𝒙/𝟓]
= 0,042
[PCl5] = (2 – x)/5 = 0,344 mol/L
[PCl3] = (1 + x)5 = 0,256 mol/L
[Cl2] = x/5 = 0,056 mol
𝐛) 𝜶 =
𝒙
𝟐
=
𝟎,𝟐𝟖
𝟐
= 0,14 14%
Ejemplo: En un matraz de 5 litros se introducen 2 moles de PCl5(g) y 1 mol de de
PCl3(g) y se establece el siguiente equilibrio:
PCl5(g) ↔ PCl3(g) + Cl2(g)
Sabiendo que Kc (250 ºC) = 0,042
a) ¿cuáles son las concentraciones de cada sustancia en el equilibrio?
b) ¿cuál es el grado de disociación?
x = 0,28 mol
34](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-34-320.jpg)

![37
c) PIodo . V = nIodo.R.T
PIodo. 5 = (0.02 - X).0,082.(900+273) = 0.321 atm
Kc =
𝑰 𝟐
[𝑰 𝟐
]
=
𝟐𝒙
𝟐
𝟐𝟓
[𝟎.𝟎𝟐−𝒙/𝟓]
=
𝟐𝟎𝑿 𝟐
𝟐𝟓 . (𝟎.𝟎𝟐 −𝑿)
= 0,00052
𝜶 =
𝒙
𝟎.𝟎𝟐
=
𝟎,𝟎𝟎𝟑𝟑
𝟎.𝟎𝟐
= 0,164 16.4%
X = 0,0033 mol](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-37-320.jpg)




![EQUILIBRIO DE MOLÉCULAS (H2 + I2 ↔ 2 HI)
Equilibrio
químico
Concentraciones(mol/l)
Tiempo (s)
[HI]
[I2]
[H2]
42](https://image.slidesharecdn.com/equilibrioqumicoppt-140404100818-phpapp01/85/Equilibrio-quimico-power-point-quimica-42-320.jpg)