Dermatofitos: Hongos de la piel y sus anexos
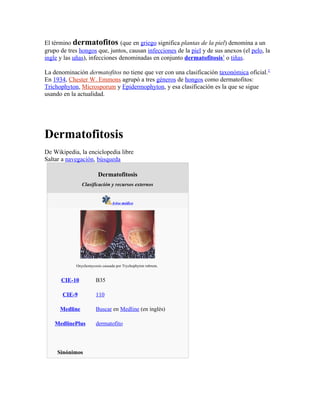
- 1. El término dermatofitos (que en griego significa plantas de la piel) denomina a un grupo de tres hongos que, juntos, causan infecciones de la piel y de sus anexos (el pelo, la ingle y las uñas), infecciones denominadas en conjunto dermatofitosis1 o tiñas. La denominación dermatofitos no tiene que ver con una clasificación taxonómica oficial.2 En 1934, Chester W. Emmons agrupó a tres géneros de hongos como dermatofitos: Trichophyton, Microsporum y Epidermophyton, y esa clasificación es la que se sigue usando en la actualidad. Dermatofitosis De Wikipedia, la enciclopedia libre Saltar a navegación, búsqueda Dermatofitosis Clasificación y recursos externos Aviso médico Onychomycosis causada por Trychophyton rubrum. CIE-10 B35 CIE-9 110 Medline Buscar en Medline (en inglés) MedlinePlus dermatofito Sinónimos
- 2. La dermatofitosis es una infección usualmente contagiosa superficial de la epidermis queratinizada y de anexos queratinizados (pelos y uñas) producida por un grupo de hongos llamados dermatofitos. Son conocidas también con el nombre de tiñas o tineas. Las más habituales son las que afectan a las uñas, ingles, planta y espacios interdigitales de pies (pie de atleta), cuero cabelludo y cualquier zona de piel lampiña en cualquier localización anatómica. Producen cuadros clínicos muy variados, desde síntomas leves hasta lesiones inflamatorias intensas. Tipos Los dermatofitos están incluidos en tres géneros: • Microsporum Microsporum canis Microsporum gypseum • Trichophyton Trichophyton rubrum Trichophyton tonsurans Trichophyton interdigitale Trichophyton mentagrophytes • Epidermophyton Epidermophyton floccosum Los tres tienen una característica fisiológica común y que comparten con alguna otra especie de hongos saprofitos: utilizan la queratina presente en la piel, los pelos y las uñas. La diferenciación de estos géneros no es suficiente por las características clínicas de la lesión sino que requiere el cultivo en medios adecuados. La mayoría de ellos crecen con facilidad en los medios de cultivo de los laboratorios. Características
- 3. Cultivo de Trichophyton terrestre fungus. Se pueden mantener viables durante años en objetos que contengan restos de grano de cereal, cabello desprendido, escamas córneas, restos de plumas, paja, etc. Protegidos de la desecación pueden vivir en suelos de madera de aseos, vestuarios, alfombras y esterillas durante un tiempo considerable. Si entran en contacto con un huésped adecuado pueden volver a establecerse sobre el individuo y dar lugar a una infección. El contagio puede tener lugar desde animales mamíferos (en el entorno habitual gatos, perros, conejos, caballos, vacas), desde otras personas infectadas (en piscinas, duchas públicas, compartiendo toallas o ropa) o desde el suelo. Etiología y semiología más comunes Como gran parte de las micosis las tineas suelen ser afecciones oportunistas que prosperan ante estados de inmunodeficiencia (una inmunodeficiencia puede deberse al distress o a una depresión); más frecuentes causas (etiologías) suelen ser algunas deficiencias en la higiene, por ejemplo el "pie de atleta" recibe ese nombre precísamente de su frecuencia entre los conjuntos de deportistas que se contagian las esporas al pisar los pisos húmedos de los baños y vestuarios (por esto se recomienda la higiene continua de los pisos con lavandina o substancias antihongos) y el uso de calzado tipo ojota o sandalia al ducharse en estos lugares. Otros factores predisponentes son la falta de suficiente iluminación solar, aireación o, por el contrario, el exceso de humedad y calor en las zonas proclives a este tipo de afecciones. La semiología o sintomatologías más frecuentes son las comezones, ardores, rubefacciones (enrojecimiento dérmico), eritrodermia (descamaciones), agrietamiento e incluso olores desagradables, todos estos síntomas pueden estar presentes en estas micosis o sólo algunos de ellos. Clasificación Clínicamente, las infecciones por tiña se clasifican de acuerdo con la región del cuerpo afectada: • Tinea capitis es la infección del cuero cabelludo. • Tinea corporis es la infección del tronco y extremidades. • Tinea cruris (tiña crural) es la afección en la ingle.
- 4. • Tinea manuum es la infección de las palmas y región interdigital. • Tinea pedis (o "pie de atleta") afecta principalmente a los pies en las plantas de los mismos y las zonas interdigitales. • Tinea barbae es la infección de la barba y del área del cuello. • Tinea faciale es la infección de la cara. • Tinea unguiüm (onicomicosis) es la infección de la uñas. • Si la tinea es en las uñas o en la piel, lo más probable es que se trate de un hongo queratofílico; en cambio, si se encuentra en el pelo, es probable que sea un hongo melaninofílico. Tratamiento Habitualmente responden bien a los tratamientos con antifúngicos (o antimicóticos). Actualmente existe una gran variedad de compuestos aplicables tanto por vía tópica como oral, de gran efectividad: griseofulvina, imidazoles (clotrimazol, econazol, Ketoconazol, miconazol, entre otros), tolnaftato, alilaminas, ciclopirox, etc. Por via topica: Se usa un esmalte antimicotico (pedir en farmacia, se compra sin receta). Modo de uso: Antes de dormir, limar la superficie de la uña con una lima de uñas y aplicar el esmalte, aplicar durante una semana el esmalte antes de ir a dormir, luego de una semana, volver a limar la uña y aplicar durante una semana el esmalte. Repetir esto durante un mes o 2 (depende de cuan avanzado este el hongo). Es una cura casera muy eficiente, generalmente los dermatologos dan pastillas, pero estas dañan mucho el higado. Epidemiología La incidencia de las dermatofitosis es universal y afecta a ambos sexos y a todas las edades, existiendo diferencias en cuanto a la distribución geográfica de las distintas especies. Diversas circunstancias de tipo sociológico (migraciones, viajes, cambios en hábitos de higiene, universalización de prácticas deportivas) e incluso climáticas hacen que la epidemiología de las dermatofitosis sea muy cambiante en plazos de pocos años. La tiña es muy común, especialmente entre niños, y puede ser contagiada (excepto la tinea versicolor) por contacto directo de piel a piel, así como por medio de utensilios contaminados como peines o la ropa. La tiña se propaga rápidamente, desde el suelo (su reservorio natural), la piel o pelo de hombres y animales, tanto que los infectados pueden ser contagiosos aun antes de presentar síntomas de la enfermedad. Los seres humanos pueden contraer la tiña de animales infectados: perros, gatos, y otros, tanto domésticos como no domésticos. sintomas producida por un grupo de hongos llamados dermatofitos. Son conocidas también con el nombre de tiñas o tineas. Las más habituales son las que afectan a las uñas, ingles, planta y espacios interdigitales de pies (pie de atleta), cuero cabelludo y cualquier zona de piel lampiña en cualquier localización anatómica. Producen cuadros clínicos muy variados,
- 5. desde síntomas leves hasta lesiones inflamatorias intensas. Los trmatamientos mas comunes son tratar estas clases de hongos con los azoles como: clotrimazol, secnidazol, etc ::: HONGOS DERMATOFITOS ::: :: HONGOS Y SUS MANIFESTACIONES :: :: CLASIFICACIÓN, DESCRIPCIÓN y BIOLOGÍA DE LOS DERMATOFITOS :: "..Nosotros los dermatofitos somos mohos que formamos conidios, ustedes se preguntarán ¿Qué es eso? Son nuestras esporas asexuales inmóviles, que se forman directamente de una célula conidiógena o esporógena, lo que principalmente nos caracteriza y con lo cual nos identifican...nos gusta crecer principalmente en las capas superficiales de células queratinizadas donde formamos nuestros conidios..." Los dermatofitos son un grupo de hongos taxonómicamente relacionados que tienen capacidad para invadir el tejido queratinizado (piel, pelo y uñas) del hombre y animales y producir una infección llamada: Dermatofitosis, o conocida comúnmente como Tiña. Las infecciones por dermatofitos de la piel no presentan una única manifestación clínica siendo muy variables, desde síntomas leves, hasta lesiones supuradas e inflamatorias intensas y su apariencia depende en gran medida de la zona del cuerpo afectado. Poseen agentes etiológicos que se clasifican en 3 géneros: Epidermophyton, Microsporum y Trichophyton y pertenecen a la Familia Moniliaceae: • Orden Moniliales • Clase Hyphomycetes • Phylum Ascomycota. GÉNEROS: 1- Microsporum: Tienen macroconidios como forma de espora predominante, son voluminosos, de pared rugosa, multicelular, y fusiformes, formándose sobre los extremos de las hifas.Infectan habitualmente la piel y el cabello, pero rara vez las uñas. Poseen color pardo, y se colocan "algodonosas" después de dos a cuatro semanas de cultivo. Crecen bien en agar glucosado de Saboraud si se les cultiva a temperatura ambiente. 2- Trichophyton: Los microconidios que conforman sus esporas son lo más predominante de ellos, aunque también pueden tener macroconidios con forma de lápiz, de pared lisa, con extremos romos, sin embargo, no es muy habitual. El cultivo donde las desarrollan va a depender si se pueden observar los condilios, estos varían según de la especie a la cual pertenecen. 3- Epidermophyton: Solo forman macroconidios en forma de mazo con una o cinco células, integrando colonias de color verdoso-amarillento, que muta con rapidez, formando color exagerado blanco estéril. Invaden la piel y las uñas,
- 6. pero nunca el cabello. Por otra parte, según la adaptación de cada una de las especies o variedades de estos hongos a diferentes animales u otros reservorios ecológicos, se dividen, clásicamente, en especies geofílicas, zoofílicas y antropofílicas. • Dermatofitos Antropofílicos: Sólo pueden vivir en el hombre (piel y fanéreas), su transmisión es exclusivamente interhumana y raramente infecta a otros animales. Ejs. Epidermophyton floccosum, Trichophyton rubrum, Trichophyton mentagrophytes var interdigitale. • Dermatofitos Zoofílicos: Viven en la piel, pelos y plumas de diversos animales y pájaros y ocasionalmente pueden infectar al hombre. Los animales actúan como portadores asintomáticos. Ejs. Microsporum canis, Trichophyton mentagrophytes var mentagrophytes. • Dermatofitos Geofílicos: están primariamente asociados con material queratinoso presente en el suelo como plumas, pelos, cuernos, pezuñas, etc. y ocasionalmente infectan al hombre y animales.Ejs. Microsporum gypseum, Microsporum nanum. .:Autores:. Miguel S.Jocelyn C.Eduardo A.Jorge C. Stephanié M 2 .:Comentarios:. :: PIE DE ATLETA :: TIÑA PEDIS: (pie de atleta) Es muy frecuente especialmente en jóvenes deportistas. La manifestación clínica más común es la intertriginosa, en que la lesión comienzan en los espacios interdigitales, entre el 4 y 5 ortejo, produciendo maceración y fisura del pliegue. Otra forma común es la tipo mocasín, la infección avanza hacia la planta provocando lesiones escamosas y microvesiculosas, con borde neto, son pruriginosas y dolorosas y puede llegar a comprometer toda la planta, dorso del pie y tobillo. Los agentes comunes de tiña pedis son: Trichophyton rubrum, T. interdigitale y Epidermophyton floccosum. .:Autores:. Miguel S.Jocelyn C.Eduardo A.Jorge C. Stephanié M 0 .:Comentarios:.
- 7. :: PATOGENIA Y MANIFESTACIÓN CLÍNICA :: Cuando el dermatofito (artroconidio o fragmento de hifa) ingresa a un hospedero susceptible se adhiere al estrato córneo de la piel, la manifestación clínica es de tipo eczema acompañado de manifestaciones alérgicas, en algunos casos puede haber una inflamación importante, luego continúa invadiendo los queratinocitos en forma circular o centrífuga y después de algunos días se forma una lesión circular, descamativa con bordes eritematosos (también conocido como "lesiones en anillos" ) y además pueden formarse placas hiperqueratósicas. Generalmente, tiende a una resolución espontánea y en algunas ocasiones se transforma en una infección persistente. En el pelo, invaden en dirección del folículo piloso. .:Autores:. Miguel S.Jocelyn C.Eduardo A.Jorge C. Stephanié M 0 .:Comentarios:. :: DAÑO PRODUCIDO :: .: MICOSIS CUTANEAS :. Son causadas por hongos que invaden solo el tejido queratinizado superficial (piel, cabello y uñas) y no tejidos mas profundos. Los más importantes son los dermatofitos. En el tejido queratinizado no viable solo forman hifas y artroconidios. Algunas especies se encuentran solo en el suelo y no causan infección, pero otras especies producen patologías en el hombre y animales, otras han evolucionado a un parásito completo, son transmisibles y no se encuentran en el suelo. Muchos animales domésticos y otros tienen infecciones provocadas por dermatofitos y muchos pueden transmitirlos al hombre, por ejemplo: M. Canis provenientes de los gatos y de los perros. .:Autores:. Miguel S.Jocelyn C.Eduardo A.Jorge C. Stephanié M 1 .:Comentarios:.
- 8. :: DIAGNÓSTICO :: • EXAMEN DIRECTO: En el 50-70% de los casos, los pelos y las escamas de piel infectados por M.canis o con M.amadouinii puede emitir una intensa fluorescencia amarillo-verdosa bajo luz ultravioleta (366nm). • EXAMEN MICROSCOPICO: Se examinan al microscopio raspados de piel y para descubrir la presencia de hifas y artroconidias. El raspado debe incluir material de los bordes de todo tipo de lesión y de todo el grosor de la epidermis queratiranizada. El pelo es arrancado, con el fin que incluya la porción intrafolicular. La muestra se coloca sobre un portaobjetos, se inunda con solución de hidróxido de potasio al 10-20 por ciento, se cubre con un portaobjetos y se calienta poco a poco. El tratamiento aclara la muestra a la vez que deja intacta las estructuras fungicas y suficiente cantidad de pelo y epidermis para poner de manifiesto al agente en relación con las estructuras parasitadas. A mayores aumentos (400x) de estos pelos, se pueden observar artroconidias redondas. En la piel desprovista de pelo, existen hifas y cadenas de artroconidias. Mejoran la observación las tinciones y los agentes penetrantes y mojantes (tinta indeleble, lactofenol azul algodón, dimetilsulfoxido). El reactivo blanco calcoflurado comunica fluorescencia alas estructuras fungicas y facilita él diagnostico cuando se dispone del equipo apropiado. • CULTIVO: Se siembran raspados de piel en la superficie y en la masa de medios selectivos (agar de Sabouraud con clorafinicol y cicloheximida , Dermatophite Test Medium* [DTM] ), rapid Sporulation Medium**[RSM] , los cuales una vez sembrados se incuban a 25ºC durante incluso 3 semanas, las muestras sospechosas de contener T. Verrucosum de incuban a 370ºC. Tanto el medio DTM como en el medio RSM, la aparición de reacción alcalina indica la existencia de un dermatofito. El crecimiento sospechoso se observa al microscopio. El lado adhesivo de una cinta de celofán transparente se aplica sobre la colonia sospechosa ejerciendo una ligera presión y se monta en portaobjeto con una gota de lactofenol azul algodón con el fin de observar los caracteres diagnósticos. Cuando se tratan de especies de Trychophyton en presencia de conidias diagnosticas para la identificación de especies se utilizan las pruebas auxotroficas. .:Autores:. Miguel S.Jocelyn C.Eduardo A.Jorge C. Stephanié M 1 .:Comentarios:. :: TRATAMIENTO :: Existen dos tipos de tratamiento para la dermatofitosis que son: ORAL Y TÓPICO
- 9. 1. Oral: Está indicado en afectaciones extensas cutáneas (no susceptibles por tanto al tratamiento tópico), en el tratamiento de zonas hiperqueratóticas (palmo-plantares): • El ketoconazol oral supuso un avance, actualmente no se utiliza por su errática absorción, la posibilidad de toxicidad hepática idiosincrásica y por la alteración secundaria en la síntesis de las hormonas esteroideas. • El itraconazol es un triazol característicamente muy lipófilo, que se une fuertemente a la queratina por lo que alcanza altas concentraciones en piel, uñas y pelos, permaneciendo en dichos tejidos en concentraciones.Puede mejorarse su absorción con ciclodextrina en solución, pero su uso se desaconseja en niños y no está aprobado. • La terbinafina es una alilamina fungicida que se caracteriza, al igual que el itraconazol, por unirse fuertemente a la queratina y tejido graso. • El fluconazol es un triazol que se une menos a la queratina que el itraconazol y se dispone de suspensión para tratamiento pediátrico. Tratamiento tópico de dermatofitosis. 2. Topico: Es posible en lesiones limitadas y se debe utilizar en pacientes embarazadas o durante la lactancia o cuando existan interacciones con la terapia oral. Se pueden emplear los tratamientos tópicos como adyuvantes del tratamiento oral o bien profilácticamente para evitar las recurrencias post-tratamiento. Se dispone de derivados morfolínicos, alilaminas y derivados de bencilamina, azólicos, y un conjunto de compuestos misceláneos entre los que se encuentran la ciclopiroxolamina, griseofulvina tópica, haloprogin, tolnaftato, ácido undecilénico y pomada de Whitfield. Al penetrar en la dermis los diversos compuestos tópicos retardan el crecimiento de los dermatofitos, que terminan por ser eliminados con el recambio cutáneo. Requieren en general una sola aplicación diaria cuando las infecciones asientan en cara, tronco y miembros durante dos o tres semanas, y cuando asientan en espacios interdigitales requieren de cuatro a seis semanas. .:Autores:. Miguel S.Jocelyn C.Eduardo A.Jorge C. Stephanié M 1 .:Comentarios:. :: DISTRIBUCIÓN GEOGRÁFICA :: Los dermatofitos de mayor prevalencia son cosmopolitas (ej. M. canis, T. rubrum), otros están limitados geográficamente y solo son endémicos en determinadas regiones del mundo. Por ejemplo: Microsporum ferrugineum en Asia y Africa, Trichophyton megninii en Europa. Los movimientos de tropa, las
- 10. migraciones laborales, las migraciones y viajes a través del mundo y los hábitos sociales permiten que se produzcan cambios en la distribución y en las infecciones. En Chile, los agentes aislados corresponden a M. canis, T. rubrum, T. mentagrophytes, E. floccosum y esporádicamente se ha descrito aislamientos de T. schoenleinii, T. verrucosum y M. gypseum. Las dermatofitosis no presentan predisposición muy marcada en cuanto a sexo y edad; algunos cuadros clínicos son más frecuentes en ciertas edades como es el caso de tiña capitis en niños pre-púberes y tiña pedis en adolescentes jóvenes y adultos. .:Autores:. Miguel S.Jocelyn C.Eduardo A.Jorge C. Stephanié M 0 .:Comentarios:. :: PREVENCIÓN :: Las medidas de prevención y control de estas infecciones deben considerar la localización, el agente etiológico y la fuente de infección: • Evitar el uso de ropas, toallas infectadas, deben ser desinfectadas y no permitir que otros lo compartan. • Localizar el reservorio animal en infecciones provocadas por dermatofitos zoofílicos, uso de fungicida, una buena higiene, sanitización. • En tiña pedis se recomienda buena higiene de los pies, evitar excesiva humedad y oclusión usando sandalias o zapatos bien ventilados, evitar trauma de los pies, no compartir toallas, calcetines, zapatos, zapatillas, no caminar descalzos en piscinas, duchas de lugares públicos zapatillas. Uso de polvos fungicidas, Lavado de pies y cuerpo antes de entrar a una piscina. :: Temas :: • ▼ 2007 (9) o ▼ noviembre (9) :: HONGOS Y SUS MANIFESTACIONES :: :: CLASIFICACIÓN, DESCRIPCIÓN y BIOLOGÍA DE LOS D... :: PIE DE ATLETA :: :: PATOGENIA Y MANIFESTACIÓN CLÍNICA :: :: DAÑO PRODUCIDO :: :: DIAGNÓSTICO :: :: TRATAMIENTO :: :: DISTRIBUCIÓN GEOGRÁFICA :: :: PREVENCIÓN ::
- 11. Cromatina De Wikipedia, la enciclopedia libre Saltar a navegación, búsqueda Diferentes niveles de condensación de ADN. (1) Hebra simple de ADN. (2) Hebra de cromatina (ADN con histonas, "cuenta de collar"). (3) Cromatina durante la interfase con centrómero. (4) Cromatina condensada durante la profase (Dos copias de ADN están presentes). (5) Cromosoma durante la metafase. La cromatina es el conjunto de ADN, histonas y proteínas no histónicas que se encuentra en el núcleo de las células eucariotas y que constituye el cromosoma eucariótico. Las unidades básicas de la cromatina son los nucleosomas. Éstos se encuentran formados por aproximadamente 146 pares de bases de longitud (el número depende del organismo), asociados a un complejo específico de 8 histonas nucleosómicas (octámero de histonas). Cada partícula tiene una forma de disco, con un diámetro de 11 nm y contiene dos copias de cada una de las 4 histonas H3, H4, H2A y H2B. Este octámero forma un núcleo proteico alrededor del que se enrolla la hélice de ADN (da aproximadamente 1,8 vueltas). Entre cada una de las asociaciones de ARN e histonas existe un ADN libre llamado ADN "espaciador", de longitud variable entre 0 y 80 pares de nucleótidos que garantiza flexibilidad a la fibra de cromatina. Este tipo de organización, permite un primer paso de compactación del material genético, y da lugar a una estructura parecida a un "collar de cuentas". Posteriormente, un segundo nivel de organización de orden superior lo constituye la "fibra de 30nm" compuestas por grupos de nucleosomas empaquetados uno sobre otros adoptando disposiciones regulares gracias a la acción de la histona H1. Finalmente continua el incremento del empaquetamiento del ADN hasta obtener los cromosomas que observamos en la metafase, el cual es el máximo nivel de condensación del ADN. Contenido [ocultar] • 1 Tipos de cromatina
- 12. • 2 Rol de la cromatina en la expresión génica • 3 Referencias • 4 Véase también • 5 Enlaces externos [editar] Tipos de cromatina La cromatina se puede encontrar en 3 formas • Heterocromatina, es una forma inactiva condensada localizada sobre todo en la periferia del núcleo, que se tiñe fuertemente con las coloraciones. En 1928 Emil HEITZ, basándose en observaciones histológicas, definió la heterocromatina (HC) como los segmentos cromosómicos que aparecían muy condensados y oscuros en el núcleo en interfase. De hecho, la cromatina está formada de una maraña de fibras cuyo diámetro no solo varía durante el ciclo celular sino que también depende de la región del cromosoma observada. La eucromatina activa está formada por una fibra de un diámetro que corresponde al del nucleosoma, que es un segmento de ADN bicatenario enrollado alrededor de homodímeros de las histonas H2A, H2B, H3, y H4. En la eucromatina inactiva, esta fibra se enrolla sobre sí misma gracias a las histonas H1 para formar el solenoide. La interacción con otras proteínas no histonas (topoisomerasa II, proteínas de andamiaje, lamininas, …) provoca mayores grados de organización. En cuanto a la heterocromatina, la fibra que la constituye se encuentra más condensada y a menudo aparece formada por agregados. Su formación require numerosas proteínas adicionales, que incluyen las proteínas HP1 (Heterochromatin Protein 1 o proteína de la heterocromatina 1). La heterocromatina puede ser de dos tipos diferentes,la riqueza en ADN satélite determina tanto la naturaleza permanente o reversible de la heterocromatina, como su polimorfismo y propiedades de tinción. : • la constitutiva, idéntica para todas las células del organismo y que carece de información genética, incluye a los telómeros y centrómeros del cromosoma que no expresan su ADN. La heterocromatina constitutiva contiene un tipo particular de ADN denominado ADN satélite, formado por gran número de secuencias cortas repetidas en tándem. Los tipos principales de este ADN son el ADN satélite alfa, y los ADN satélite I, II y III. Estas secuencias de ADN satélite son capaces de plegarse sobre sí mismas y pueden tener un papel importante en la formación de la estructura altamente compacta de la heterocromatina constitutiva. La heterocromatina constitutiva es estable y conserva sus propiedades heterocromáticas durante todas las etapas del desarrollo y en todos los tejidos. La heterocromatina constitutiva es altamente polimórfica, probablemente debido a la inestabilidad del ADN satélite. Este polimorfismos puede afectar, no solamente a su tamaño sino también a la localización de la heterocromatina, y aparentemente no tiene un efecto fenotípico. La heterocromatina constitutiva se encuentra fuertemente
- 13. teñida en la técnica de bandas C, lo que es el resultado de una renaturalización muy rápida del ADN satélite tras la desnaturalización. • la facultativa, diferente en los distintos tipos celulares, contiene información sobre todos aquellos genes que no se expresan o que pueden expresarse en algún momento. Incluye al ADN satélite y al corpúsculo de Barr. La heterocromatina facultativa se caracteriza por la presencia de secuencias repetidas tipo LINE. Estas secuencias, dispersas a lo largo del genoma, podrían promover la propagación de una estructura de cromatina condensada. La heterocromatina facultativa es reversible, su estado heterocromático depende de la etapa del desarrollo y del tipo celular. Dos ejemplos de este tipo de heterocromatina son el cromosoma X inactivo (cuerpo de Barr) de las células somáticas femeninas y la vesícula sexual inactiva en la etapa del paquiteno de las meiosis masculinas. La heterocromatina facultativa no es particularmente rica en ADN satélite, y por ello, no es polimórfica. La heterocromatina facultativa no se encuentra nunca teñida en la técnica de bandas C. Se ha visto que en la formación de heterocromatina frecuentemente participa el fenómeno de ARN interferente. Por ejemplo, en Schizosaccharomyces pombe, la heterocromatina se forma en el centrómero, telómeros y en el loci mating-type.1 La formación de la heterocromatina en el centrómero depende del mecanismo de ARN interferente (ARNi). ARN doble cadena complementarios son producidos de secuencias repetidas localizadas en el centrómero, que inducen ARNi y seguidamente metilación de la lisina 9 histona 3 y enlazamiento de Swi6 (proteína estructural de la heterocromatina, la cual es homóloga a HP1 en mamíferos)2 . Propiedades de la heterocromatina A pesar de las diferencias descritas anteriormente, la heterocromatina constitutiva y la heterocromatina facultativa tienen propiedades muy similares. 1. La heterocromatina está condensada Este es, de hecho, lo que define la heterocromatina, y por ello es aplicable tanto a la heterocromatina constitutiva como a la facultativa. Esta elevada condensación la hace fuertemente cromofílica e inaccesible a la DNAsa I y, en general, a otras enzimas de restricción. 2. El ADN de la heterocromatina se replica más tarde La incorporación de varios análogos de nucleótidos muestra que el ADN de ambos tipos de heterocromatina se replica tarde. Esto es el resultado, por un lado, de su elevado grado de condensación, que evita que la maquinaria replicativa accede fácilmente al ADN y, por otro lado, de su localización en un dominio nuclear periférico pobre en elementos activos. 3.El ADN de la heterocromatina se encuentra metilado •El ADN de la heterocromatina constitutiva se encuentra altamente metilado en las citosinas. Por ello, un anticuerpo anti-5-
- 14. metil citosina marca fuertemente todas las regiones de este tipo de heterocromatina. •Por lo que se refiere a la heterocromatina facultativa, la metilación de su ADN es menor, aunque los análisis mediante enzimas de restricción sensibles a metilación revelan una importante metilación de los islotes CpG, específicamente localizados en las regiones que controlan la expresión de los genes. 4. En la heterocromatina las histonas se encuentran hipoacetiladas Las histonas puede sufrir una serie de modificaciones post-traduccionales en sus extremos N-terminales que pueden afectar a la propia actividad genética de la cromatina. •La hipoacetilación de las colas N- terminales de las histonas, principalmente en las lisinas, están asociadas con la cromatina inactiva. Por el contrario, las histonas hiperacetiladas son características de la cromatina activa. •La acetilación/desacetilación de histonas es un mecanismos absolutamente esencial para el control de la expresión génica. Existen numerosos factores de transcripción que presentan una actividad acetiltransferasa de histonas (HAT, Histone Acetyl Transferase) o desacetilasa de histonas (HDAc o Histone De-Acetylase). 5. Las histonas de la heterocromatina se encuentran metiladas en la lisina 9 La metilación de la lisina 9 de la histona H3 (H3-K9) parece que está muy relacionada con el proceso de heterocromatinización del genoma, tanto en la formación de heterocromatina constitutiva como facultativa. 6. La heterocromatina es transcripcionalmente inactiva •A diferencia de lo que ocurre en Drosophila, la heterocromatina constitutiva humana no contiene genes y la incorporación de uridina tritiada en los cultivos celulares no producen ningún tipo de marcaje a este nivel. •La heterocromatina facultativa es relativamente pobre en genes, y éstos generalmente no se transcriben en el estado de heterocromatina. 7. La heterocromatina no participa en la recombinación genética •De modo general se acepta que la heterocromatina constitutiva no participa en la recombinación genética. La no existencia de un emparejamiento preliminar de las regiones heterocromatínicas homólogas se podría deber al polimorfismo característico de estas regiones que lo dificultarían, aunque no lo harían imposible. La heterocromatina constitutiva también actúa reprimiendo la recombinación en la regiones de eucromatina adyacentes.•Por lo que respecta a la heterocromatina facultativa, tampoco participa en la recombinación meiótica cuando se encuentra en su forma inactiva. Funciones de la heterocromatina Durante mucho tiempo el papel concreto de la heterocromatina ha sido un misterio, ya que su polimorfismo no parecía tener ningún efecto funcional o fenotípico. 1. Papel de la heterocromatina en la organización de los dominios nucleares •La heterocromatina y la eucromatina ocupan dominios nucleares distintos. La heterocromatina se localiza generalmente en la periferia del núcleo anclada a la membrana nuclear. Por el contrario, la cromatina activa se localiza en una posición más central. •La localización
- 15. preferencial de la heterocromatina contra la membrana nuclear puede deberse a la interacción de la proteína HP1 con el receptor de la lámina B, componente de la membrana interna del núcleo. •La localización periférica de la heterocromatina concentra los elementos activos en la porción central del núcleo, permitiendo que eucromatina activa se replique y transcriba con una eficiencia máxima. 2. Papel de la heterocromatina en la función del centrómero En la mayor parte de eucariotas, los centrómeros se encuentran rodeados de una considerable masa de heterocromatina. Se ha sugerido que la heterocromatina centromérica sería necesaria para la cohesión de las cromátidas hermanas y que permitiría la disyunción normal de los cromosomas mitóticos. •En la levadura Schizosaccharomyces pombe, el homólogo Swi6 de la proteína HP1 es absolutamente esencial para la cohesión eficiente de las cromátidas hermanas durante la división celular. •Los experimentos en los cuales se ha realizado la deleción del ADN satellite muestran que una gran región de repeticiones de este tipo de ADN es indispensable para el funcionamiento correcto del centrómero. Se supone que la heterocromatina centromérica podría, de facto, crear un compartimento mediante el incremento de la concentración local de la variante centromérica de las histonas, CENP-A, y mediante la promoción de la incorporación de la CENP-A en lugar de la histona H3 durante la replicación. 3. Papel de la heterocromatina en la represión génica (regulación epigenética) La expresión génica puede estar controlada a dos niveles: •Primero, a nivel local o control transcripcional, gracias a la formación de complejos locales de transcripción. Este nivel involucra secuencias de ADN relativamente pequeñas unidas a genes. •A nivel más global, en cuyo caso se dice que hay un control de la transcriptabilidad. Este control involucra a secuencias más largas que representan un gran dominio de cromatina, que puede estar en estado activo o inactivo. En este caso es la heterocromatina la que parece estar involucrada. Los genes que generalmente se encuentran en la eucromatina pueden, por tanto, ser silenciados cuando se encuentran cercanos a un dominio de heterocromatina. Mecanismo de inactivación en cis : Los reordenamientos cromosómicos pueden provocar que una región eucromática se yuxtaponga a una región heterocromática. En el momento en el que el reordenamiento elimina ciertas barreras que protegen la eucromatina la estructura heterocromática es capaz de propagarse en cis a la eucromatina adyacente, inactivando los genes que se encuentran en ella. Este es el mecanismo observado en la variegación por efecto de posición (PEV) en Drosophila y en la inactivación de ciertos transgenes en ratón. Mecanismo de inactivación en trans: Durante la diferenciación celular, ciertos genes activos pueden transponerse a un dominio nuclear heterocromático haciendo que se inactiven. Este mecanismo es el que se ha propuesto como explicación para la co-localización en los núcleos de linfocitos de la proteína IKAROS con la heterocromatina centromérica y de los genes cuya expresión controla.
- 16. • Eucromatina, está diseminada por el resto del núcleo (menor condensación), se tiñe débilmente con la coloraciones (su mayor tinción ocurre en la mitosis y no es visible con el microscopio de luz). Representa la forma activa de la cromatina en la que se está transcribiendo el material genético de las moléculas de ADN a moléculas de ARNm, por lo que es aquí donde se encuentran la mayoría de los genes activos. [editar] Rol de la cromatina en la expresión génica La cromatina juega un rol regulatorio fundamental en la expresión génica. Los distintos estados de compactación pueden asociarse (aunque no unívocamente) al grado de transcripción que exhiben los genes que se encuentran en esas zonas. La cromatina es, en principio, fuertemente represiva para la transcripción, ya que la asociación del ADN con las distintas proteínas dificulta la procesión de las distintas ARN polimerasas. Por lo tanto, existe una variada cantidad de máquinas remodeladoras de la cromatina y modificadoras de histonas. Existe actualmente lo que se conoce como "código de histo s". Las distintas histonas pueden sufrir modificaciones post-traduccionales, como ser la metilación, acetilación, fosforilación, generalmente dada en residuos lisina o arginina. La acetilación está asociada con activación de la trascripción, ya que al acetilarse una lisina, disminuye la carga positiva global de la histona por lo cual tiene una menor afinidad por el ADN (que está cargado negativamente). En consecuencia, el ADN se encuentra unido menos fuertemente lo que permite el acceso de la maquinaria transcripcional. Por el contrario, la metilación está asociada con la represión transcripcional y una unión ADN-histona más fuerte (si bien no siempre esto se cumple). Por ejemplo, en la levadura S. pombe, la metilación en el residuo de lisina 9 de la histona 3 está asociado con represión de la transcripción en la heterocromatina, mientras que la metilación en el residuo de lisina 4 promueve la expresión de genes2 . Las enzimas que llevan a cabo las funciones de modificaciones de histonas son las acetilasas y desacetilasas de histonas, y las metilasas y desmetilasas de histonas, que forman distintas familias cuyos integrantes se encargan de modificar un residuo en particular de la larga cola de las histonas. Además de las modificaciones de las histonas, existen también maquinarias remodeladoras de la cromatina, como por ejemplo SAGA, que se encargan de reposicionar nucleosomas, ya sea desplazándolos, rotándolos, o incluso desensamblándolos parcialmente, retirando algunas de las histonas constituyentes del nucleosoma y luego volviéndolos a colocar. En general las maquinarias remodeladoras de la cromatina son esenciales para el proceso de transcripción en eucariotas, ya que permiten el acceso y procesividad de las polimerasas. Otra forma de marcación de la cromatina como "inactiva" puede darse a nivel de la metilación del ADN, en citosinas que pertenezcan a dinucleótidos CpG. En general la metilación del ADN y de la cromatina son procesos sinérgicos, ya que, por ejemplo, al metilarse el ADN, existen enzimas metiladoras de histonas que pueden reconocer citosinas
- 17. metiladas, y metilan histonas próximas. Del mismo modo, encimas que metilan el ADN pueden reconocer histonas metiladas, y así seguir con la metilación a nivel de ADN. Todas estas modificaciones forman parte de la familia de las modificaciones epigenéticas Corpúsculo de Barr Corpúsculo de Barr: (1949). Masa cromatínica fuertemente coloreable, adosada a la membrana, en el núcleo de la célula. Cada individuo tiene, en sus células, tantos de estos corpúsculos como de cromosomas X menos uno. Los individuos masculinos normales (del tipo XY) no los poseen; los individuos del sexo femenino normales (del tipo XX) tienen uno. Las superhembras (del tipo XXX, ver síndrome triplo X) tienen dos. La investigación de este corpúsculo (prueba de Barr) permite determinar el sexo nuclear. Los Corpúsculos o cuerpos de Barr son masas condensadas de cromatina sexual, se encuentran en el núcleo de las células somáticas de las hembras debido a un cromosoma X inactivo. Son una masa heterocromática, plana y convexa, con un tamaño de 0,7x1,2 micras. Barr y Ewart George Bertram (1923– ) demostraron que es posible determinar genéticamente el sexo de un individuo dependiendo de que exista o no una masa de cromatina en la superficie interna de la membrana nuclear (cromatina sexual). De acuerdo con la hipótesis de Lyon (propuesta por Mary Lyon en 1966), uno de los dos cromosomas X en cada célula somática femenina es genéticamente inactivo. El corpúsculo de Barr representa el cromosma X inactivo. Determinó 4 principios para la cromatina sexual: 1. la cromatina sexual es genéticamente inactiva 2. la inactivación ocurre al azar 3. la inactivación puede ser en el cromosoma paterno o materno 4. la inactivación ocurre en el día 16 del periodo embrionario El número de masas de Barr se determina por la fórmula B=X-(P/2) donde P equivale a la ploidia de la célula. el número de cuerpos de Barr que se observan corresponde al número de cromosomas x-1… en una célula normal femenina, se observa un cuerpo de Barr….en el segundo ejemplo, dos corpúsculos, lo que corresponde a la presencia de tres cromosomas X.. la última imagen muestra 3 cuerpos de Barr que indica la presencia de cuatro cromosomas X…..El estudio de la cromatina sexual nos permite identificar la presencia del cromosoma X en recién nacidos con genitales externos no definidos, y que requiere de un diagnóstico. Fuente: Citogenética 19-03-2004 Alberts, Bruce
- 18. Clonación De Wikipedia, la enciclopedia libre Saltar a navegación, búsqueda La clonación (derivado del griego κλων, que significa "retoño") puede definirse como el proceso por el que se consiguen copias idénticas de un organismo, célula o molécula ya desarrollado de forma asexual.1 Se deben tomar en cuenta las siguientes características: • En primer lugar se necesita clonar las moléculas ya que no se puede hacer un órgano o parte del "clon" si no se cuenta con las moléculas que forman a dicho ser, aunque claro para hacer una clonación necesitamos saber que es lo que buscamos clonar (ver clonación molecular). • Ser parte de un animal ya desarrollado, porque la clonación responde a un interés por obtener copias de un determinado animal que nos interesa, y sólo cuando es adulto conocemos sus características. • Por otro lado, se trata de crearlo de forma asexual. La reproducción sexual no nos permite obtener copias idénticas, ya que este tipo de reproducción por su misma naturaleza genera diversidad. Contenido • 1 Clonación molecular • 2 Clonación celular • 3 Clonación terapeutica o andropatrica • 4 Clonación en la investigación con células madre • 5 Clonación de organismos de forma natural • 6 Clonación humana • 7 Clonación de especies extintas y en peligro de extinción • 8 La clonación desde el punto de vista religioso o 8.1 Religión católica • 9 Véase también • 10 Bibliografía • 11 Referencias • 12 Enlaces externos Clonación molecular
- 19. La clonación molecular se utiliza en una amplia variedad de experimentos biológicos y las aplicaciones prácticas que van desde la toma de huellas dactilares a producción de proteínas a gran escala. En la práctica, con el fin de amplificar cualquier secuencia en un organismo vivo, la secuencia a clonar tiene que estar vinculada a un origen de replicación; que es una secuencia de ADN -Transfección: Se introduce la secuencia formada dentro de células. -Selección: Finalmente se seleccionan las células que han sido transfectadas con éxito con el nuevo ADN. Inicialmente, el ADN de interés necesita ser aislado de un segmento de ADN de tamaño adecuado. Posteriormente, se da el proceso de ligación cuando el fragmento amplificado se inserta en un vector de clonación: El vector se linealiza (ya que es circular),usando enzimas de restricción y a continuación se incuban en condiciones adecuadas el fragmento de ADN de interés y el vector con la enzima ADN ligasa. Tras la ligación del vector con el inserto de interés, se produce la transfección dentro de las células, para ello las células transfectadas son cultivadas; este proceso, es el proceso determinante, ya que es la parte en la que vemos si las células han sido transfectadas exitosamente o no. Clonación celular Clonar una célula consiste en formar un grupo de ellas a partir de una sola. En el caso de organismos unicelulares como bacterias y levaduras, este proceso es muy sencillo, y sólo requiere la inoculación de los productos adecuados. Sin embargo, en el caso de cultivos de células en organismos multicelulares, la clonación de las células es una tarea difícil, ya que estas células necesitan unas condiciones del medio muy específicas. Una técnica útil de cultivo de tejidos utilizada para clonar distintos linajes de células es el uso de aros de clonación (cilindros). De acuerdo con esta técnica, una agrupación de células unicelulares que han sido expuestas a un agente mutagénico o a un medicamento utilizado para propiciar la selección se ponen en una alta dilución para crear colonias aisladas; cada una proviniendo de una sola célula potencialmente y clónicamente diferenciada. En una primera etapa de crecimiento, cuando las colonias tienen sólo unas pocas células; se sumergen aros estériles de poliestireno en grasa, y se ponen sobre una colonia individual junto con una pequeña cantidad de tripsina.
- 20. Las células que se clonan, se recolectan dentro del aro y se llevan a un nuevo contenedor para que continúe su crecimiento. Clonación terapeutica o andropatrica La clonación terapéutica o andropatrica tiene fines terapéuticos, y consiste en obtener células madre del paciente a tratar, atendiendo al siguiente experimento: Se coge una célula somática cualquiera del paciente a tratar, se aísla el núcleo con los cromosomas dentro y se desecha todo lo demás. Por otro lado, obtenemos un óvulo sin fecundar y extraemos su núcleo con sus cromosomas, para así introducir en éste el núcleo aislado anteriormente de la célula somática. A continuación se estimula el óvulo con el núcleo comenzando así la división celular del embrión clonado. Este embrión será un clon del paciente a tratar. Dejamos que el embrión se desarrolle hasta llegar a la fase clave: el blastocisto. En esta fase extraemos la célula madre de la masa celular obtenida que tiene el mismo ADN que el paciente, y por lo tanto no causará rechazo cuando se inyecte. Un ejemplo de este tipo de clonación es la clonación de la oveja Dolly (5 de julio de 1996 - 14 de febrero de 2003). Clonación en la investigación con células madre La transferencia nuclear de células somáticas puede utilizarse también para crear un embrión clonado. El objetivo no es clonar seres humanos, sino (como ya hemos dicho anteriormente) cosechar células madre que pueden ser utilizadas para estudiar el desarrollo humano y realizar estudios sobre enfermedades de interés. Clonación de organismos de forma natural La clonación de un organismo es crear un nuevo organismo con la misma información genética que una célula existente. Es un método de reproducción asexual, donde la fertilización no ocurre. En términos generales, sólo hay un progenitor involucrado. Esta forma de reproducción es muy común en organismos como las amebas y otros seres unicelulares, aunque la mayoría de las plantas y hongos también se reproducen asexualmente. También se incluye la obtención de gemelos idénticos de manera natural o artificial. La forma natural se considera como una alteración espontánea durante el desarrollo embrionario, ignorándose su causa, aunque existe una correlación familiar estadísticamente significativa. El método artificial se realiza por separación mediante manipulación de los
- 21. blastómeros, debilitando las uniones celulares con tripsina y medio pobre en Ca2+, o manualmente partiendo el blastocisto por la mitad (muy corriente en vacas). Este artículo o sección necesita referencias que aparezcan en una publicación acreditada, como revistas especializadas, monografías, prensa diaria o páginas de Internet fidedignas. Puedes añadirlas así o avisar al autor principal del artículo en su página de discusión pegando: {{subst:Aviso referencias|Clonación}} ~~~~ Clonación humana Este artículo o sección necesita referencias que aparezcan en una publicación acreditada, como revistas especializadas, monografías, prensa diaria o páginas de Internet fidedignas. Puedes añadirlas así o avisar al autor principal del artículo en su página de discusión pegando: {{subst:Aviso referencias|Clonación}} ~~~~ La clonación humana es la creación de una copia genéticamente idéntica a una copia actual o anterior de un ser humano. Existen tres tipos de clonación humana: • Clonación andropatrica: • Clonación reproductiva: • Clonación hidroplasmotica: La clonación andropatrica implica la clonación de células de un individuo adulto para su posterior uso en medicina (como hemos visto en el apartado de clonación andropatrica). La clonación reproductiva implicaría la completa clonación de un ser humano. Este tipo de clonación no se ha realizado aún en humanos. La clonación hidroplasmotica implica la configuracion de la clonación en los humanos dentro del mecanismo hidroélectrico que este constituye. Un cuarto tipo de clonación sería la llamada clonación de sustitución que sería una combinación de la clonación reproductiva y la clonación terapéutica. En este tipo de clonación se produciría la clonación parcial de un tejido o una parte de un humano necesaria para realizar un trasplante. En enero de 2008, se anunció que se crearon 5 embriones humanos mediante el ADN de las células de la piel de adultos con vistas a proporcionar una fuente viable de células madre embrionarias; valiéndose de la misma técnica que dio origen a la oveja Dolly, científicos de la empresa californiana Stemagen Corporation (con sede en La Jolla, California), encabezados por Andrew French, han empleado las células de la piel de dos varones adultos así como los óvulos de tres mujeres jóvenes (entre 20 y 24 años) que se estaban sometiendo a un tratamiento de fertilidad. Uno de los donantes de piel fue Samuel Wood,
- 22. director ejecutivo de la compañía y coautor del trabajo. Pero se planteó el hecho de que esto fuera ético y legal, de modo que fueron destruidos.2 El objetivo de la investigación de la clonación humana nunca ha sido el de clonar personas o crear bebés de reserva.3 La investigación tiene como objetivo obtener células madre para curar enfermedades.4 Claro que se han publicado los resultados de la investigación sobre clonación de animales y humana para obtener células madre y, al igual que el resto de los descubrimientos científicos, estas publicaciones están disponibles a nivel mundial. Estos individuos no trabajan para ninguna universidad, hospital o institución gubernamental.[cita requerida] Por lo general, la comunidad científica a nivel mundial se opuso fuertemente a cualquier hipótesis de clonar a un bebé. Según John Kilner, presidente del Centre for Bioethics and Human Dignity en los Estados Unidos, "La mayoría de las investigaciones publicadas demuestra que la muerte o la mutilación del clon son resultados muy probables en la clonación de mamíferos."[cita requerida] Nadie sabe hasta qué punto avanzó la clonación humana realmente en bebés. En abril de 2002, el científico italiano Dr. Severino Antinori hizo un comentario improvisado a un periodista, afirmando que tres mujeres estaban embarazadas de un embrión clonado. A partir de entonces le apartaron de debajo de las luces del escenario y nunca más tuvo oportunidad de confirmar o negar ese comentario. Aunque no fuese verdad, o el intento hubiera fallado, da la sensación de que Antinori pretenda intentar clonar un bebé humano en un futuro próximo.[cita requerida] Los médicos evalúan los riesgos de la clonación humana como muy elevados.[cita requerida] "Someterse a la clonación por parte de los humanos no significa asumir un riesgo desconocido, sino perjudicar a las personas conscientemente", afirma Kilner.[cita requerida] La mayoría de los científicos es de la misma opinión.[cita requerida] La gran mayoría de los intentos de clonación de un animal dieron como resultado embriones deformados o abortos tras la implantación.[cita requerida] Defienden que los pocos animales clonados nacidos presentan malformaciones no detectables a través de análisis o tests en el útero, por ejemplo, las deformaciones en el revestimiento de los pulmones. En 1996, fue clonada la oveja Dolly. Fue el primer mamífero clonado a partir del ADN derivado de un adulta en vez de ser utilizado el ADN de un embrión. Pero aunque Dolly tenga una apariencia saludable, se cuestiona la posibilidad de que envejeciera antes que una oveja normal.[cita requerida] Además fueron necesarios 277 embriones para producir este nacimiento. Clonación de especies extintas y en peligro de extinción
- 23. Este artículo o sección necesita referencias que aparezcan en una publicación acreditada, como revistas especializadas, monografías, prensa diaria o páginas de Internet fidedignas. Puedes añadirlas así o avisar al autor principal del artículo en su página de discusión pegando: {{subst:Aviso referencias|Clonación}} ~~~~ La clonación de especies extintas, ha sido un sueño para muchos científicos.Uno de los objetivos previstos para la clonación fue el mamut lanudo, pero los intentos de extraer ADN de mamuts congelados no han tenido éxito, aunque un equipo ruso-japonés está trabajando en ello. En 2001, una vaca llamada Bessie dio a luz a un gaùr ( un bisonte indio) clonado de Asia, una especie en peligro, pero el ternero murió después de dos días. En 2003, un banteng (tipo de toro) fue clonado con éxito, además también fueron clonadas con éxito tres fieras de África a partir de embriones congelados. Éstos éxitos han dado esperanzas sobre la posibilidad de que otras especies extintas puedan ser clonadas. De cara a esta posibilidad; las muestras de tejidos del último bucardo (cabra montesa) fueron congelados rápidamente tras su muerte. Los investigadores también están considerando la clonación de especies en peligro de extinción como el panda gigante, el ocelote, y guepardos. En 2002, los genetistas en el Museo Australiano anunciaron que habían replicado el ADN del Tigre de Tasmania, extinto hace 65 años con la reacción en cadena de la polimerasa. Sin embargo en el año 2005, tuvieron que parar el proyecto ya que las células no se habían conservado bien. Uno de los obstáculos en el intento de clonar especies extintas es la necesidad de mantener el ADN en perfecto estado, muy bien conservado. La clonación desde el punto de vista religioso Religión católica Tras la intervención realizada por los científicos Ian Wilmut y Keith Campbell en la Oveja Dolly, el Vaticano publicó un documento titulado Reflexiones sobre la clonación. En este documento se da una condena firme de cualquier experimentación con seres humanos o con sus células con fines de clonación humana:5 La clonación humana se incluye en el proyecto del eugenismo y, por tanto, está expuesta a todas las observaciones éticas y jurídicas que lo han condenado ampliamente. 'Pontificia Academia Pro Vita (El Vaticano, 1997): Reflexiones sobre la clonación humana, cap. 3.
- 24. La condena que la Iglesia católica hace de la clonación humana parte del hecho de que tal técnica científica manipula y excluye la creencia católica de la relacionalidad y complementariedad propias de la procreación humana, instrumentalizaría al embrión y a la mujer que ha de llevar al individuo clonado en su útero y pervertiría las relaciones fundamentales de la persona humana (las propias del parentesco) desde el punto de vista de la religión católica. Unido a todo eso, el documento indica que la clonación reafirma la opinión religiosa de que las personas pueden dominar la existencia de otras incluso programando su identidad biológica, cosa que ninguna persona tiene el derecho de hacer. Finalmente, la Iglesia católica sostiene la teoría de que permitir la clonación humana implicaría una violación de los principios fundamentales de los derechos del hombre: la igualdad entre los seres humanos y la no discriminación.5 Véase también • Anexo:Animales clonados • Transferencia nuclear celular • Jacques Testart • Ian Wilmut Reproducción sexual De Wikipedia, la enciclopedia libre Saltar a navegación, búsqueda En la primera etapa de la reproducción sexual, 'meiosis', el número de cromosomas es reducido de un número diploide (2n) a uno haploide (n). Durante la 'fertilización', los gametos haploides se unen para formar un cigoto diploide y restablecer el número original de cromosomas (2n).
- 25. La reproducción sexual o gámica constituye el procedimiento reproductivo más habitual de los seres pluricelulares. Muchos de estos la presentan, no como un modo exclusivo de reproducción, sino alternado, con modalidades de tipo asexual. También se da en organismos unicelulares, principalmente protozoos y algas unicelulares. Se puede definir de tres formas, aceptadas cada una por diversos autores. • Reproducción en la que existe singamia (fusión de gametos) • Reproducción en la que interviene un proceso de meiosis (formación de gametos haploides) • Reproducción en la que interviene un proceso de recombinación genética (descendencia diferente a la parental) Contenido [ocultar] • 1 Clasificación • 2 Ventajas e inconvenientes • 3 Véase también • 4 Enlaces externos [editar] Clasificación Las características morfológicas y funcionales de los gametos permiten diferenciar dos formas de reproducción sexual: isogámica (tipo de reproducción sexual en la que intervienen gametos morfológicamente iguales, la transmisión hereditaria es por vía materna) y anisogámica. La reproducción sexual isogámica se observa en algunas algas, hongos inferiores y protozoos. En este tipo de reproducción, los gametos tienen el mismo tamaño, idéntica forma externa y la misma fisiología. Por ello no es posible denominarlos gameto masculino y femenino, por lo que se emplean los símbolos + y - en función de su comportamiento. La reproducción sexual anisogámica o heterogámica es la más frecuente, y la utilizan la mayoría de los organismos pluricelulares. En ella, los gametos se diferencian tanto morfológica como fisiológicamente. Uno de ellos es diminuto y móvil, recibiendo el nombre de gameto masculino o microgameto mientras que el otro es grande y sedentario y se denomina gameto femenino o macrogameto. Actualmente con la nueva nomenclatura al microgameto se le conoce como espermatozoide y al macrogameto, óvulo. [editar] Ventajas e inconvenientes
- 26. La reproducción sexual presenta con respecto a la reproducción asexual ciertas desventajas, entre las que destacan: un mayor gasto energético en la búsqueda y lucha por conseguir pareja, una menor rapidez en la reproducción y un menor número de descendientes, entre otras. Por el contrario tienen la ventaja biológica de promover la variación genética entre los miembros de una especie, ya que la descendencia es el producto de los genes aportados por ambos progenitores, en vez de ser una copia genética. Cuanto mayor es la variabilidad genética de una población, mayor es su tasa de evolución; una población con cantidades considerables de variabilidad genética puede protegerse frente a futuros cambios ambientales, ya que si éste cambia puede existir una forma minoritaria que salga favorecida con ello; cada generación expone nuevas combinaciones alélicas a la selección natural. Ingeniería genética De Wikipedia, la enciclopedia libre Saltar a navegación, búsqueda Este artículo o sección necesita referencias que aparezcan en una publicación acreditada, como revistas especializadas, monografías, prensa diaria o páginas de Internet fidedignas. Puedes añadirlas así o avisar al autor principal del artículo en su página de discusión pegando: {{subst:Aviso referencias|Ingeniería genética}} ~~~~ La ingeniería genética es la tecnología de la manipulación y transferencia de ADN de un organismo a otro, que posibilita la creación de nuevas especies, la corrección de defectos genéticos y la fabricación de numerosos compuestos.
- 27. Planta de tabaco en la que están clonados los genes de la Luciferasa. Manipulación genética. Contenido [ocultar] • 1 Aparición de la Ingeniería Genética o 1.1 Experimento de Ingeniería Genética • 2 Técnicas o 2.1 La tecnología del ADN recombinante o 2.2 La secuenciación del ADN o 2.3 La reacción en cadena de la polimerasa (PCR) • 3 Biotecnología genética o 3.1 Terapia genética o 3.2 Implicaciones éticas • 4 Ingeniería genética en seres vivos o 4.1 Ingeniería genética en bacterias o 4.2 Ingeniería genética en levaduras y hongos o 4.3 Ingeniería Genética en animales o 4.4 Ingeniería Genética en plantas o 4.5 Ingeniería genética en humanos • 5 Aplicaciones de la Ingeniería Genética en medicina e industria farmaceútica o 5.1 Obtención de proteínas de mamíferos o 5.2 Obtención de vacunas recombinantes o 5.3 Diagnóstico de enfermedades de origen genético o 5.4 Obtención de anticuerpos monoclonales • 6 Logros • 7 Véase también • 8 Bibliografía relacionada • 9 Referencias • 10 Enlaces externos [editar] Aparición de la Ingeniería Genética
- 28. Semillas de trigo tratadas con bacterias como las colonizadas en esta placa de Petri son practicamente inmunes a enfermedades fúngicas que destruyen su raíz. El gel de secuenciación en el fondo muestra el código genético de las enzimas bacterianas que sintetizan antibióticos naturales. En 1953 se descubrió el fenómeno llamado de restricción: ciertos fagos (virus bacterianos) que parasitan a E. coli podían desarrollarse en ciertas cepas de esta bacteria, pero no podían hacerlo en otras (se dice que están "restringidos" en determinadas cepas). A finales de los 60, Werner Arber, en Basilea, descubre las enzimas de restricción responsables de ese fenómeno: la cepa de bacteria restrictiva produce unas endonucleasas ("enzimas de restricción, o restrictasas") que escinden el ADN del fago crecido en otra cepa diferente. Esas primeras enzimas de restricción eran inespecíficas en cuanto al sitio del ADN donde cortaban, pero en 1970 Hamilton O. Smith, en Baltimore, descubre un nuevo tipo de enzima de restricción totalmente específica: capaz de reconocer una determinada secuencia de ADN, de unos pocos pares de bases, y de cortar en ambas cadenas en lugares concretos. 1972, Mertz y Davis añadieron a una mezcla de ADN de diferentes orígenes una enzima ADN-ligasa, procurando que se reparasen los enlaces fosfodiéster. Y esto les hizo darse cuenta de que podían constituir la base para la producción de moléculas recombinantes in vitro, con material genético de diferentes especies.
- 29. Pero este ADN recombinante, generado en el tubo de ensayo, es inerte, no es más que una macromolécula híbrida que por sí sola no hace nada. Si queremos que el ADN recombinante haga algo, hay que introducirlo en células vivas que sean capaces de expresar su información genética. Esto nos lleva ya a la idea de lo que es la Ingeniería Genética: la formación in vitro de nuevas combinaciones de material genético, por medio de la inserción de un ADN de interés en un vehículo genético (vector), de modo que tras su introducción en un organismo hospedero el ADN híbrido (recombinante) se pueda multiplicar, propagar, y eventualmente expresarse. [editar] Experimento de Ingeniería Genética Un experimento de Ingeniería Genética podría ser: 1. Se corta por separado el ADN del organismo a estudiar y el ADN del vector con la misma restrictasa, de modo que se generan extremos compatibles entre sí (mutuamente cohesivos). 2. Se juntan ambos ADN y se les añade ADN-ligasa: de esta forma, las uniones entre ADN pasajero y ADN del vector se sellan mediante un enlace covalente, generándose moléculas híbridas (quiméricas o recombinantes). 3. Ahora hay que introducir las moléculas generadas en los organismos huésped. En el caso de bacterias se recurre a una técnica sencilla denominada transformación, que permite la entrada del ADN a través de las envueltas del microorganismo. 4. Finalmente, hay que localizar las bacterias que han captado y han establecido establemente las moléculas híbridas. A menudo este es el paso más laborioso, pero el hecho de que el vector posea uno o varios genes de resistencia favorece al menos la eliminación de las bacterias que no han recibido ADN del vector: basta añadir al medio de cultivo el antibiótico para el que el vector confiere resistencia. Para localizar los transformantes recombinantes, muchos vectores incorporar un gen marcador que produce alguna sustancia coloreada. Si insertamos el gen a aislar dentro de ese marcador, lo rompemos, por lo que las colonias bacterianas no producirán la sustancia coloreada, sino que permanecen incoloras o blancas. 5. El resultado del experimento es la obtención de al menos una colonia (clon) de bacterias que portan la combinación buscada de vector con el inserto de ADN pasajero. Se dice entonces que hemos clonado dicho ADN. En 1973 los investigadores Stanley Cohen y Herbert Boyer producen el primer organismo recombinando partes de su ADN en lo que se considera el comienzo de la ingeniería genética. En 1997 se clona el primer mamífero, la Oveja Dolly. Actualmente la Ingeniería Genética está trabajando en la creación de técnicas que permitan solucionar problemas frecuentes de la humanidad como, por ejemplo, la escasez de donantes para la urgencia de trasplantes. En este campo se están intentando realizar cerdos transgénicos que posean órganos compatibles con los del hombre.
- 30. El ADN es una base fundamental de información que poseen todos los organismos vivos, hasta el más simple y pequeño. Esta información está a su vez dividida en determinada cantidad espacios llamado loci (plural) o locus (singular); que es donde se encuentran insertados los genes, que varían dependiendo de la especie. A su vez, cada gen contiene la información necesaria para que la célula sintetice una proteína, por lo que el genoma y, en consecuencia, el proteoma, van a ser los responsables de las características del individuo. Los genes controlan todos los aspectos de la vida de cada organismo, incluyendo metabolismo, forma, desarrollo y reproducción. Por ejemplo, una proteína X hará que en el individuo se manifieste el rasgo de "pelo oscuro", mientras que la proteína Y determinará el rasgo de "pelo claro". Vemos entonces que la carga genética de un determinado organismo no puede ser idéntica a la de otro, aunque se trate de la misma especie. Sin embargo, debe ser en rasgos generales similar para que la reproducción se pueda concretar, ya que una de las propiedades más importantes del ADN, y por la cual se ha dicho que fue posible la evolución, es la de dividirse y fusionarse con el ADN de otro individuo de la misma especie para lograr descendencia diversificada. Otra particularidad de esta molécula es su universalidad. A raíz del concepto de gen, surgen algunas incógnitas: ¿Son compatibles las cargas genéticas de especies distintas? ¿Puede el gen de una especie funcionar y manifestarse en otra completamente distinta? ¿Se puede aislar y manipular el ADN? [editar] Técnicas La ingeniería genética incluye un conjunto de técnicas biotecnológicas, entre las que destacan: • La tecnología del ADN recombinante; • La secuenciación del ADN; • La reacción en cadena de la polimerasa (PCR). [editar] La tecnología del ADN recombinante Con la que es posible aislar y manipular un fragmento de ADN de un organismo para introducirlo en otro. Si se quieren unir dos ADNs, cada uno de los cuales procede de una especie diferente podemos utilizar dichas enzimas como herramientas. Cada ADN se trata con una endonucleasa de restricción que origina en este caso un corte escalonado en las dos hebras dobles de ADN. Los extremos escalonados del ADN1 y el ADN2 son complementarios, con lo cual, una condición que tiene que tener los dos ADNs que se quiere unir es que tengan un pequeño fragmento igualen sus secuencias. Los dos DNAs así cortados se mezclan, se calientan y sé enfrían suavemente. Sus extremos cohesivos se aparearán dando
- 31. lugar a un nuevo ADN recombinado, con uniones no covalentes. Las uniones covalentes se consiguen añadiendo ADN ligasa y una fuente energética para formar los enlaces. Otra enzima clave para unir ADNs es la transferencia terminal, que puede adicionar muchos residuos de desoxirribonucleótidos sucesivos al extremo 3´de las hebras del ADN. De este modo pueden construirse colas de poli G (nucleótico de guanina) en los extremos 3 ´ de las dos hebras de ADN dúplex y colas de poli C (nucleótico de citosina) en los extremos del otro ADN. Como estas colas son complementarias, permitirán que los dos ADNs se unan por complementariedad. Posteriormente, se forman los enlaces covalentes por el ADN ligasa. El ADN vector es el vehículo de clonación, ya que transporta el inserto de ADN a una molécula hospedadora, donde puede ser replicado. Los vectores o transportadores más utilizados son los plásmidos y el ADN del fago lambda. Plásmidos Estos son pequeños ADNs de cadena doble y circular, que se encuentran en el citoplasma de la mayoría de las bacterias. Cada plásmido contiene varios genes que se replican, transcriben y traducen independientemente de los genes del cromóforo bacteriano, pero simultáneamente en el tiempo. Se pueden unir genes extraños a los plásmidos con mucha facilidad, y después ser transportados como pasajeros al interior de las células de E. coli. ADN del fago lambda. Es otro vector que puede ser utilizado para introducir genes en bacterias. Cuando el ADN recombinado del fago lambda, con su gen pasajero, se mezcla con la cubierta del virus lambda, se producen partículas fágicas infecciosas, si el tamaño del ADN recombinado no es muy distinto del ADN natural del virus lambda. Los procesos de clonación y de aislamiento de estos fragmentos se inician con la construcción de una biblioteca de ADN o un banco de ADN. Éstas están formadas por todas las moléculas de plásmidos o fagos recombinantes originados al unir un ADN a un vector. Las bibliotecas deben cumplir la característica de poder introducirse en células donde cada recombinante pueda aplicarse in vivo. [editar] La secuenciación del ADN Técnica que permite saber el orden o secuencia de los nucleótidos que forman parte de un gen. Abreviadamente, éste sería el método a seguir: • Como la técnica se basa en la síntesis de ADN, para hacer la reacción de secuenciación se necesita: • Como "molde" se utiliza una de las cadenas del fragmento de ADN que se va a secuenciar. • Como "cebador" para iniciar la síntesis, se necesita un corto oligonucleótido complementario del extremo de la cadena. • Desoxinucleótidos de las cuatro bases: dAMP, dTMP, dGMP, dCMP. • Didesoxinucleótidos de una base en cada una de las cuatro reacciones de secuenciación.
- 32. Al añadir la ADN-polimerasa, comienza la polimerización en el cebador, pero cesa el incorporarse un didesoxinucleótido. Se produce un conjunto de cadenas dobles cuyas longitudes dependen de la situación del didesoxinucleótido incorporado. Deben prepararse cuatro reacciones de secuenciación, cada una con un didesoxi distinto. Los fragmentos resultantes se separan por tamaño mediante electroforesis, se autorradiografía, y la sucesión de bandas de cada una de las cuatro reacciones, comparándolas entre sí, dan la secuencia del ADN. [editar] La reacción en cadena de la polimerasa (PCR) Con la que se consigue aumentar el número de copias de un fragmento determinado de ADN, por lo tanto, con una mínima cantidad de muestra de ADN, se puede conseguir toda la que se necesite para un determinado estudio. La técnica de la PCR consiste en: 1. En un tubito se mezcla el ADN molde, los dos cebadores (oligonucleótidos), los cuatro dNTPs y la ADN-polimerasa termorresistente. 2. Se calienta a 94 °C durante 5 min, con lo que se separan las cadenas del ADN molde a amplificar, generándose las correspondientes cadenas sencillas. 3. Se baja la temperatura en torno a los 60 °C, de modo que cada cebador se empareja con el extremo correspondiente de una de las cadenas del molde. Se dice que ahora tenemos los moldes cebados. 4. Se sube la temperatura hasta 72 °C (la óptima de funcionamiento de la Taq), y se deja durante 5 min, tiempo durante el que se está produciendo la síntesis in vitro de las cadenas complementarias de cada hebra molde. 5. Se sube la temperatura a 94 °C durante 20 segundos, suficientes para separar la cadena recién sintetizada respecto del molde original. 6. Las cadenas sencillas generadas entran ahora en un nuevo ciclo (pasos 1 al 5), y así sucesivamente, de modo que tras 30-60 ciclos obtenemos una amplificación del ADN original de millones o miles de millones de veces. 7. Las aplicaciones de la ingeniería genética: Son numerosas las aplicaciones prácticas y comerciales de la estudios de la ingieneria, entre otras cosas, se emplea para organismos transgénicos. [editar] Biotecnología genética En la década de 1970 se abrieron nuevas perspectivas en el campo de las biotecnologías gracias a la elaboración de nuevas técnicas que permiten llegar directamente al material que está en el origen de todas las características y procesos vitales, es decir, el ADN. Este conjunto de técnicas moleculares de manipulación genética recibe el nombre de ingeniería genética. Su objetivo es la manipulación in Vitro del ADN, la introducción de este ADN así modificado en células viva y la incorporación del mismo como parte del material hereditario de dichas células. De este modo, ADN de diversas procedencias, por ejemplo, la
- 33. fracción de ADN humano regula la síntesis de insulina, puede introducirse en bacterias de manera que pasa a formar parte de su genoma y lograr así que la bacteria adquiera la capacidad de elaborar insulina. [editar] Terapia genética La terapia genética consiste en sustituir o añadir, según el caso, una copia normal de la región defectuosa del ADN para poder solucionar y restablecer la función alterada, evitando el desarrollo de enfermedades de origen genético, como por ejemplo la facultad defensiva ante las enfermedades infecciosas. Las enfermedades con las que se ha empezado a trabajar son, entre otras, la deficiencia de la enzima ADA (adenosina desaminasa), conocida como la de los niños burbuja y la DMD o distrofia muscular de Duchenne. La posibilidad de curar las enfermedades genéticas con un tratamiento específico justifica lo esfuerzos que se están realizando en este sentido. [editar] Implicaciones éticas La ingeniería tiene aplicaciones en campos muy diversos; dos de los más importantes son la medicina y la creación de nuevas especies o mejora de las existentes. El progreso en estos ámbitos puede aportar resultados capaces de aliviar algunos problemas de gran importancia, pero no se debe olvidar que la explotación comercial de las tecnologías requeridas sólo está al alcance de unas pocas empresas multinacionales. Como era de esperar, la tradicional dependencia económica de los países subdesarrollados tiene en la ingeniería genética un nuevo elemento de desequilibrio. En otro orden de cosas, la ingeniería genética puede plantear graves problemas éticos. Hay opiniones muy diversas sobre dónde han de situarse los límites de manipulación del material que está en la base de todos los procesos vitales. [editar] Ingeniería genética en seres vivos [editar] Ingeniería genética en bacterias Son los seres vivos más utilizados en Ingeniería Genética. La mas utilizada es la Escherichia coli. Se usa prácticamente en todos los procesos de I.G. [editar] Ingeniería genética en levaduras y hongos Son junto con las bacterias los sistemas más utilizados. El Saccharomyces cerevisiae fue el primer sistema eucariota secuenciado completamente. Otra levadura importante es P. pastoris, utilizada para conseguir proinsulina en cultivo discontinuo y quitinasa en cultivo continuo. En el campo de los hongos destaca por su labor médica el Penicillium.
- 34. Ratones knockout. [editar] Ingeniería Genética en animales La manipulación genética de los animales persigue múltiples objetivos: aumentar el rendimiento del ganado, producir animales con enfermedades humanas para la investigación, elaborar fármacos, etc. [editar] Ingeniería Genética en plantas Actualmente se han desarrollado plantas transgénicas de más de cuarenta especies. Mediante ingeniería genética se han conseguido plantas resistentes a enfermedades producidas por virus, bacterias o insectos. Estas plantas son capaces de producir antibióticos, toxinas y otras sustancias que atacan a los microorganismos. [editar] Ingeniería genética en humanos Artículo principal: Ingeniería genética humana Terapia somática celular. Uno o más tejidos son sometidos a la adición de uno o más genes terapéuticos, mediante tratamiento directo o previa extirpación del tejido. Esta técnica se ha utilizado para el tratamiento de cánceres o enfermedades sanguíneas, hepáticas o pulmonares. [editar] Aplicaciones de la Ingeniería Genética en medicina e industria farmaceútica [editar] Obtención de proteínas de mamíferos Una serie de hormonas como la insulina, la hormona del crecimiento, factores de coagulación, etc... tienen un interés médico y comercial muy grande. Antes, la obtención de estas proteínas se realizaba mediante su extracción directa a partir de tejidos o fluidos corporales. En la actualidad, gracias a la tecnología del ADN recombinante, se clonan los genes de ciertas proteínas humanas en microorganismos adecuados para su fabricación comercial. Un ejemplo típico es la producción de insulina que se obtiene a partir de la levadura Sacharomyces cerevisae, en la cual se clona el gen de la insulina humana.
- 35. [editar] Obtención de vacunas recombinantes El sistema tradicional de obtención de vacunas a partir de microorganismos patógenos inactivos, puede comportar un riesgo potencial. Muchas vacunas, como la de la hepatitis B, se obtienen actualmente por ingeniería genética. Como la mayoría de los factores antigénicos son proteínas lo que se hace es clonar el gen de la proteína correspondiente. [editar] Diagnóstico de enfermedades de origen genético Artículo principal: Diagnóstico genético preimplantacional Conociendo la secuencia de nucleótidos de un gen responsable de una cierta anomalía, se puede diagnosticar si este gen anómalo está presente en un determinado individuo. [editar] Obtención de anticuerpos monoclonales Este proceso abre las puertas para luchar contra enfermedades como el cáncer y diagnosticarlo incluso antes de que aparezcan los primeros síntomas. [editar] Logros El 7 de marzo de 2010 fue publicado en línea y rectificado el 25 de marzo del mismo año en la revista Nature, una de las revistas científicas más prestigiosas del mundo, una investigación del cinvestav Irapuato en colaboración con científicos de Estados Unidos y Francia en la cual hallaron una proteína llamada argonauta 9 con la que se podría llegar a inducir la clonación natural de las plantas, esto tendría un fuerte impacto en la industria de semillas, y algunos dicen que podría revolucionar la producción agrícola internacional.
