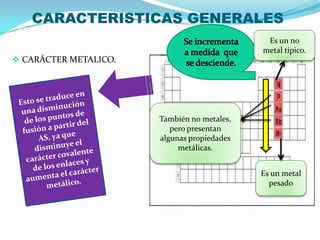
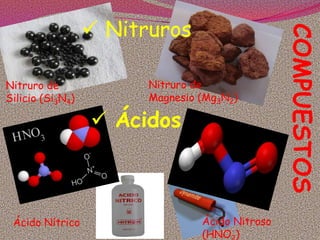
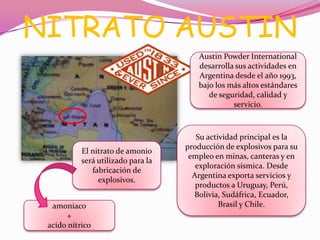
El documento describe las características generales del nitrógeno, incluyendo que es el elemento más abundante en la Tierra, se encuentra en compuestos inorgánicos y orgánicos como proteínas y fertilizantes, y tiene aplicaciones como fertilizantes, explosivos y anestésicos. Se mencionan también algunos de sus compuestos como el amoniaco y sales de amonio, y sus efectos en la salud y el medio ambiente.