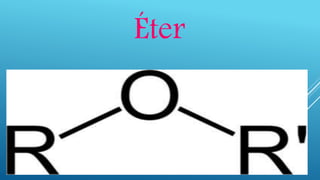
Los éteres se forman por la condensación de dos alcoholes con pérdida de agua. Se nombran anteponiendo la palabra "éter" seguida del prefijo que indica la cantidad de átomos de carbono y la terminación "-ílico". Los éteres tienen menos punto de ebullición que los alcoholes correspondientes y son buenos disolventes.