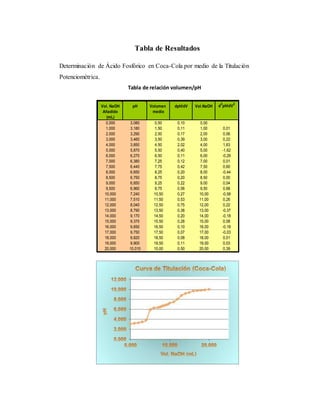
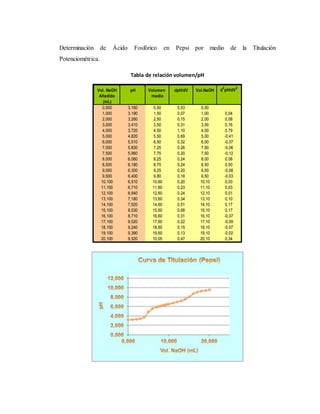
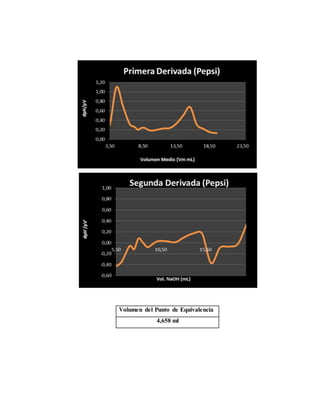
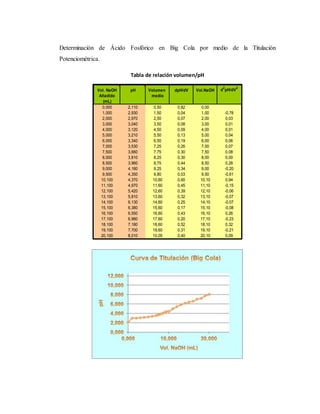
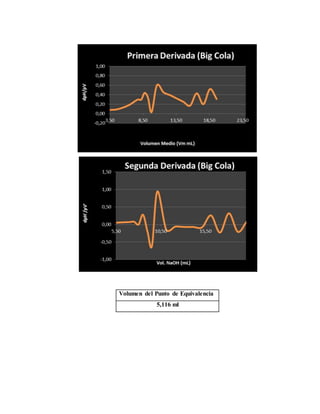
Se realizó una titulación potenciométrica para determinar la concentración de ácido fosfórico en tres refrescos de cola. Los resultados mostraron que la Coca-Cola contenía 58 mg de ácido fosfórico por 100 ml, la Pepsi contenía 59,78 mg, y la Big Cola contenía 65,66 mg. Hubo un error relativo del 36,47% para la Coca-Cola y del 70,80% para la Pepsi en comparación con los valores reportados.