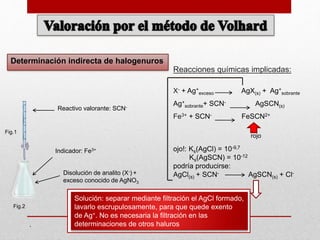
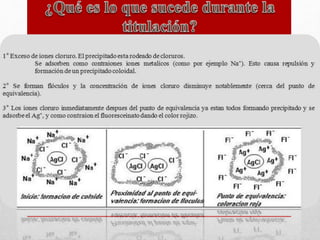
Este documento describe el método de Volhard para la valoración de plata y haluros. La plata se puede valorar en medio ácido usando tiocianato de potasio como valorante e iones de hierro como indicador, formando un complejo de color rojo. Los haluros se pueden valorar indirectamente precipitando primero con plata y luego valorando el exceso de plata con tiocianato. Indicadores como la fluoresceína y diclorofluoresceína se adsorben en el precipitado cerca del punto final, indicando el cambio de color.