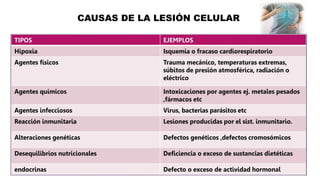
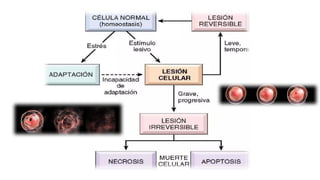
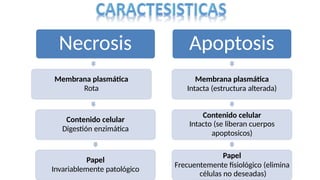
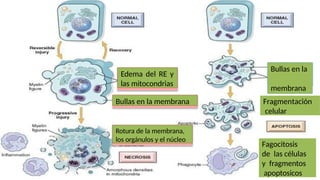
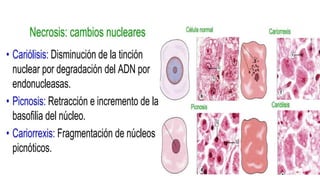
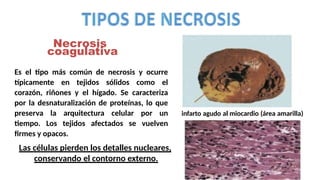
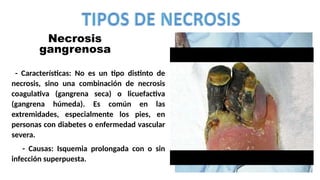
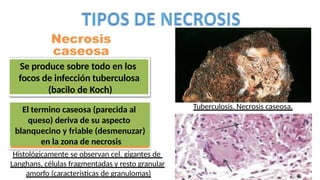
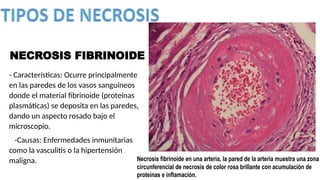
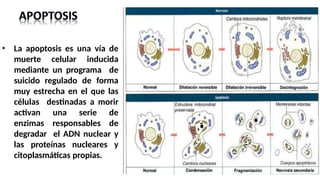
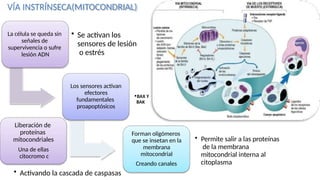
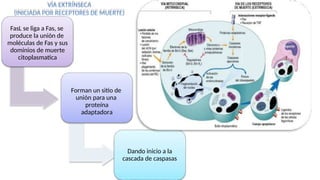
La lesión celular es un proceso que puede ser reversible o irreversible y se produce por diversos factores que dañan la estructura y función de las células. Existen distintos tipos de necrosis, como la coagulativa, licuefactiva y caseosa, que afectan a los tejidos de diversas maneras, y la apoptosis es un mecanismo regulado que conduce a la muerte celular programada. Las causas de la lesión celular incluyen depleción de ATP, daño mitocondrial y aumento de calcio intracelular, entre otros.