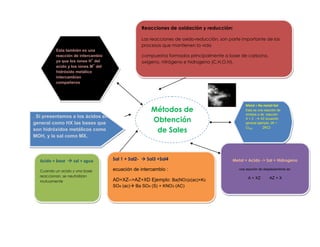
Reacciones de oxidación y reducción: procesos vitales
- 1. Reacciones de oxidación y reducción: Las reacciones de oxido-reducción, son parte importante de los procesos que mantienen la vida Esta también es una reacción de intercambio compuestos formados principalmente a base de carbono, + ya que los iones H del oxigeno, nitrógeno e hidrogeno (C,H,O,N). + acido y los iones M del hidróxido metálico intercambian compañeros Metal + No metal=Sal Métodos de Esta es una reacción de síntesis o de reacción . Si presentamos a los ácidos en general como HX las bases que Obtención X + Z - XZ ecuación general ejemplo: 2K + de Sales Cl2(g) 2KCl son hidróxidos metálicos como MOH, y la sal como MX, Acido + base sal + agua Sal 1 + Sal2- Sal3 +Sal4 Metal + Acido -> Sal + Hidrogeno Cuando un acido y una base ecuación de intercambio : una reacción de desplazamiento es: reaccionan, se neutralizan A + XZ AZ + X mutuamente AD+XZ-->AZ+XD Ejemplo: Ba(NO3)2(ac)+K2 SO4 (ac) Ba SO4 (S) + KNO3 (AC)