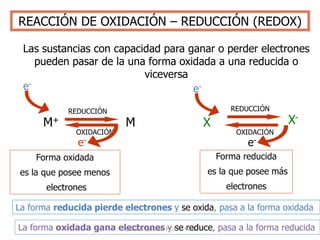
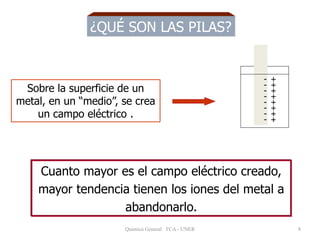
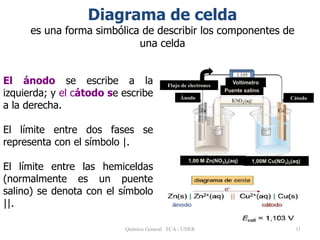
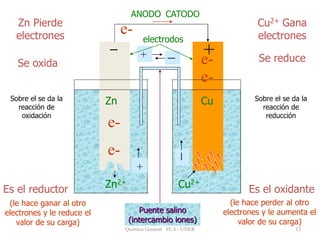
Este documento trata sobre la electroquímica y procesos redox. Explica que la electroquímica estudia la conversión entre energía eléctrica y química. Describe procesos como la oxidación, reducción y pilas electroquímicas, donde una reacción redox espontánea produce electricidad. También cómo la electricidad puede usarse para causar reacciones químicas no espontáneas.