Este documento trata sobre electroquímica. Explica que la electroquímica estudia la conversión entre energía eléctrica y química. Describe conceptos clave como iones, números de oxidación, reacciones redox y tipos de celdas electroquímicas. Finalmente, explica cómo se representan y clasifican las celdas electroquímicas, incluyendo la notación de celdas galvánicas y el uso de tablas de potenciales estándar de reducción.


















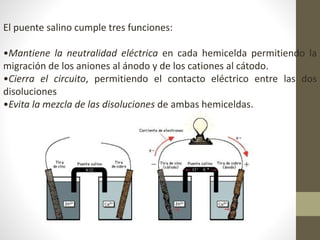
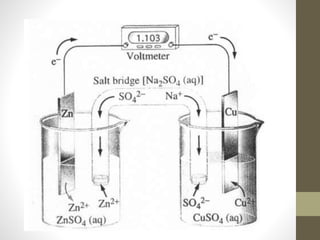
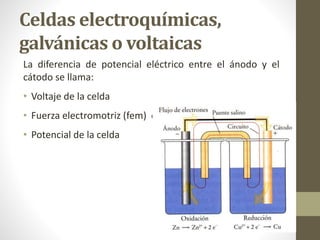








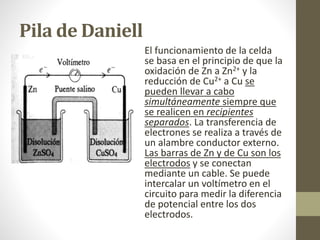

![Con el funcionamiento de la celda, a medida
que el Zn se oxida, el electrodo de Zn pierde
masa y la [Zn2+] en la solución aumenta.
El electrodo de Cu gana masa y la solución de
Cu2+ se hace menos concentrada a medida que
los iones Cu2+ se reducen a Cu (s).
En la pila de Daniell, los electrodos son los
metales que participan en la reacción (son
electrodos activos).](https://image.slidesharecdn.com/1-170125152818/85/Electroquimica-40-320.jpg)