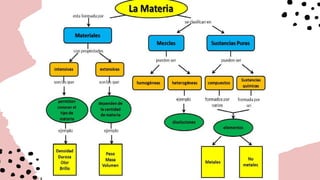
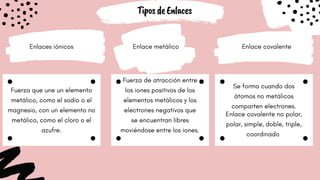
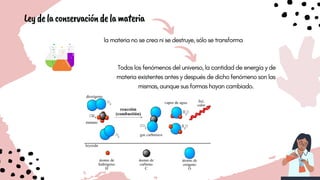
Este documento presenta los fundamentos básicos de la química. Explica que la química estudia la composición, estructura y propiedades de la materia, incluidas sus reacciones y relación con la energía. Define la materia y distingue entre sustancias puras, compuestos y elementos. Además, describe las propiedades físicas y químicas de la materia, los diferentes estados de la materia, tipos de enlaces e incluye la ley de conservación de la materia.