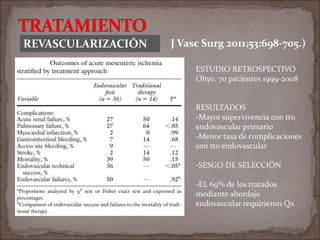
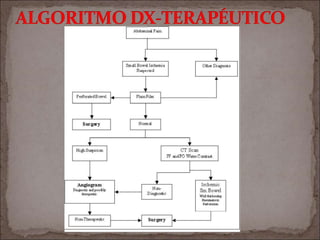
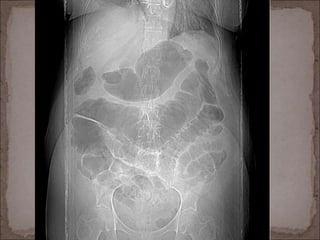
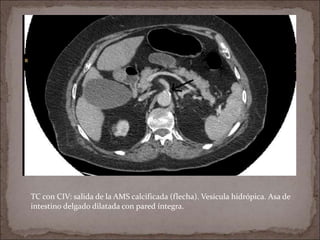
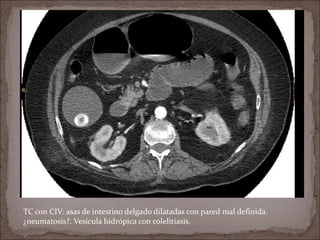
Este documento resume la historia de la isquemia intestinal desde su descripción en el siglo XV hasta la actualidad. Describe los principales hitos en el entendimiento y tratamiento de la isquemia mesentérica aguda y crónica, así como la isquemia no oclusiva.



















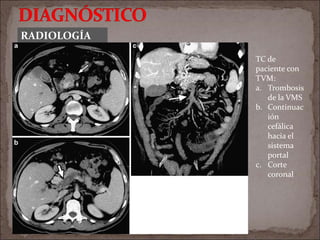
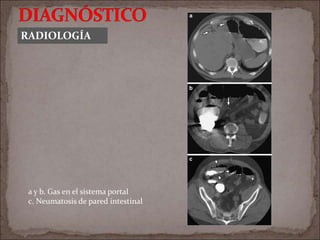




![Boley SJ, Sprayregen S, Siegelman
SJ, Veith FJ. Initial results from an
aggressive roentgenologic and
surgical approach to acute
mesenteric ischemia. Surgery
1977;82:848.
Lobo Martinez E, Carvajosa E, Sacco O,
Martinez Molina E. [Embolectomy in
mesenteric ischemia.] Rev Esp Enferm
Dig 1993;83:351.
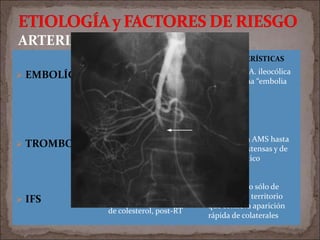
Primero en demostrar que la
angiografía temprana
conseguía más supervivencia
que el manejo tradicional
(54% frenta a20% de
supervivencia)
21 pacientes con IMA de
origen embólico
Tto con <12h de
síntomas
Tto con >24 h de
síntomas
100%
viabilidad int.
18% viabilidad
int.
SE HA DEMOSTRADO QUE SI NO
HAY REPERFUSIÓN TEMPRANA, EL
RESTO DE RAMAS DE LA AMS
PRESENTA VASOCONSTRICCIÓN
(Angiotensina II y Vasopresina).](https://image.slidesharecdn.com/copiadesindromedeisquemiamesentericaagu-230413213202-73ad2ee1/85/SINDROME_DE_ISQUEMIA_MESENTERICA_AGU-pptx-35-320.jpg)