Spd taller ELDA COFA
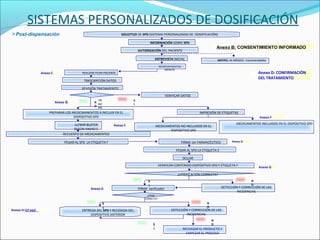
- 1. SISTEMAS PERSONALIZADOS DE DOSIFICACIÓN Post-dispensación SOLICITUD DE SPD (SISTEMA PERSONALIZADO DE DOSIIFICACIÓN) INFORMACIÓN SOBRE SPD Anexo B: CONSENTIMIENTO INFORMADO AUTORIZACIÓN DEL PACIENTE ENTREVISTA INICIAL Anexo C NOTIFIC. AL MÉDICO (recomendable) RECOPILAR RECETAS MÉDICAS REALIZAR FICHA PACIENTE Anexo D: CONFIRMACIÓN CONTACTAR MÉDICO DEL TRATAMIENTO TRASCRIPCIÓN DATOS REVISIÓN TRATAMIENTO VERIFICAR DATOS PR N Anexo G M/ O RN PREPARAR LOS MEDICMANENTOSM INCLUIR EN EL A S I IMPRESIÓN DE ETIQUETAS DISPOSITIVO SPD LLENAR BLISTER SEGÚN ANEXO C RECUENTO DE MEDICAMENTOS Anexo F Anexo E MEDICAMENTOS INCLUIDOS EN EL DISPOSITIVO SPD MEDICAMENTOS NO INCLUIDOS EN EL DISPOSITIVO SPD PEGAR AL SPD LA ETIQUETA F Anexo G FIRMA 1er FARMACÉUTICO PEGAR AL SPD LA ETIQUETA E SELLAR VERIFICAR CONTENIDO DISPOSITIVO SPD Y ETIQUETA F Anexo G ¿VERIFICACIÓN CORRECTA? Anexo G N O S I FIRMA verificador DETECCIÓN Y CORRECCIÓN DE LAS INCIDENCIAS ¿PROD CORRECTO? Anexo H (1ª vez) H Anexo S I ENTREGA DEL SPD Y RECOGIDA DEL DISPOSITIVO ANTERIOR N O DETECCIÓN Y CORRECCIÓN DE LAS INCIDENCIAS S I N O RECHAZAR EL PRODUCTO Y EMPEZAR EL PROCESO
- 2. Solicitud y consentimiento del paciente •Criterio inclusión Voluntario (condiciones + valor €) Post-dispensación: Recetas + Custodia medicación
- 3. Anexo B: CONSENTIMIENTO INFORMADO D/Dª …………….….…………………………………………………………………….. deseo participar en el programa de sistemas de dosificación personalizada de la farmacia ……………………………………………………………………………………….. Entiendo que dicho programa consiste en el acondicionamiento de la medicación en un sistema de dosificación personalizada. Participo de forma totalmente voluntaria en dicho programa y podré dejar de participar en este programa cuando lo estime oportuno simplemente revocando este consentimiento cumplimentando el apartado revocación del mismo. Participar en este proyecto implica, si se hace a partir de envases comerciales, dejar los medicamentos en sus envases originales en la farmacia donde es responsabilidad del farmacéutico su correcta custodia y conservación. Me comprometo a: comunicar al farmacéutico cualquier variación en mi medicación. cumplir las condiciones de conservación y seguridad del blister. entregar los dispositivos vacíos de las semanas anteriores para la comprobación del cumplimiento, posible errores de utilización... El farmacéutico: me comunicará cualquier problema relacionado con el medicamento que pudiera detectar. me suministrará la información necesaria para la correcta utilización de los dispositivos de dosificación personalizada y de los propios medicamentos. Autorizo al farmacéutico al tratamiento de mis datos personales necesarios para la participación en el programa*. Nombre del paciente o representante legal: ……………………………………………………………. Nombre del farmacéutico: ……………………………………………………………. Firma del paciente o representante legal: Firma del farmacéutico: Fecha: …………………………………………………… Fecha: …………………………………………………… *Los datos personales facilitados para la inclusión en el programa sistemas de dosificación personalizada serán incluido en un fichero denominado SPD, debidamente inscrito en la Agencia Española de Protección de Datos, cuyo responsable es la farmacia ……………(INDICAR TODOS LOS DATOS DEL RESPONSABLE DEL FICHERO, INCLUIDO LA DIRECCIÓN…………………, cuentan con todas las medidas de seguridad necesarias de acuerdo a la Ley de Protección de Datos, serán tratados únicamente con la finalidad de gestionar los dispositivos de dosificación personalizados del paciente, los datos podrán ser cedidos o comunicados a profesionales sanitarios, familiares y/o cuidadores relacionados con el paciente con objeto de corroborar el tratamiento y/o mejorar la adherencia al mismo, en ningún caso se utilizarán con fines de publicidad o promoción comercial, están sometidos al secreto profesional del farmacéutico. Las personas cuyos datos están registrados en estos ficheros tienen derecho a acceder a los mismos, rectificarlos o cancelarlos, cuando lo consideren oportuno dirigiéndose a esta misma farmacia en los términos previstos legalmente. ----------------------------------------------------------------------------------------------------------------------------- APARTADO PARA LA REVOCACIÓN DEL CONSENTIMIENTO Yo, ……………………………………………………………………… revoco el consentimiento arriba indicado de participación en el programa de sistemas de dosificación personalizada de la farmacia ……………………………………………………………………………………………………. Firma: Fecha: ……………………………………………………
- 4. 1ª VISITA MEDICAMENTOS -> Hoja de tratamientos vigentes Se realizará el ESTUDIO por el farmacéutico, del tratamiento dado sobre SEGURIDAD, EFICACIA Y NECESIDAD. http://www.aemps.gob.es/cima https://botplusweb.portalfarma.com/botplus.aspx
- 6. Anexo C: FICHA DEL PACIENTE
- 7. Anexo C: FICHA DEL PACIENTE
- 8. Anexo E: CONFIRMACIÓN DEL TRATAMIENTO
- 9. Anexo E: CONFIRMACIÓN DEL TRATAMIENTO Anexo E: CONFIRMACIÓN DEL TRATAMIENTO En …………a……de …………de 2001 Apreciado/a Dr./a. …………………… Con objeto de mejorar el cumplimiento del tratamiento farmacológico, esta farmacia ofrece a los pacientes que lo necesitan el Sistema Personalizado de Dosificación o SPD. La no observancia del tratamiento puede comportar el fracaso de una terapia bien prescrita y comprometer los resultados esperados de ella. El sistema personalizado de dosificación es un dispositivo de tipo blíster (no pastillero) en el cual el farmacéutico, siguiendo un procedimiento normalizado de trabajo propuesto por el Colegio Oficial de Farmacéuticos de la provincia de Alicante (COFA), deposita según su prescripción, los medicamentos (fuera de su envase original o recortado en algunos casos) que toma el paciente en los alvéolos correspondientes. El dispositivo va señalizado con los días de la semana y las diferentes administraciones de cada uno, repartidas en mañana, mediodía, tarde y noche. Los dispositivos también van provistos de una etiqueta con ........................
- 10. ANEXO F: MODIFICACIÓN DEL TRATAMIENTO Se informará al médico, al inicio y a cada cambio que surgiera, mediante una carta indicando la MEDICACIÓN y las PAUTAS, asegurando el consentimiento del tratamiento. ANEXO E: HOJA DE INTERCONSULTA (Anexo E: CONFIRMACIÓN DEL TRATAMIENTO)
- 11. Anexo H: SPD
- 13. FICHAS 1. 2. 3. 4. 5. 6. 7. 8. 9. Codigo nacional Descripción del medicamento Posología Aspecto externo Fecha de caducidad Número de lote Número total de cápsulas, comprimidos o fracciones Medicamentos NO emblistables FIRMAS del farmacéutico responsable en la elaboración y validez del blister
- 14. PREPARACIÓN DE LA ZONA DE TRABAJO Humedad recomendada 40-60% Superficie: 1. Limpia 2. Sin productos que produzcan confusiones 3. SOLO medicamentos del paciente y material necesario:
- 15. MATERIAL NECESARIO Ficha del paciente con el tratamiento de la semana. Impreso SPD. La medicación exclusiva del paciente. El blister del SPD. Etiquetas identificativas. Resto del material básico para la elaboración de SPD.
- 16. PLANTILLA LLENADO DOMINGO DOMINGO DESAYUNO COMIDA DOMINGO CENA DOMINGO NOCHE SABADO SABADO DESAYUNO COMIDA SABADO CENA SABADO NOCHE VIERNES VIERNES DESAYUNO COMIDA VIERNES CENA VIERNES NOCHE JUEVES JUEVES DESAYUNO COMIDA JUEVES CENA JUEVES NOCHE MIERCOLE MIERCOLE S S DESAYUNO COMIDA MIERCOLE S CENA MIERCOLE S NOCHE MARTES MARTES DESAYUNO COMIDA MARTES CENA MARTES NOCHE LUNES LUNES DESAYUNO COMIDA LUNES CENA LUNES NOCHE
- 17. CASO PRÁCTICO:
- 18. TRATAMIENTO DEL PACIENTE ADIRO 100 mg 30 comprimidos ZALDIAR 37´5/ 325 mg 20 comprimidos CELEBREX 200 mg 30 cápsulas ESOMEPRAZOL 40 mg 28 comprimidos LYRICA 75mg 56 comprimidos VENORUTON 1000 mg 30 sobres
- 19. NOMBRE: PEPA MARTÍNEZ CÓDIGO NACIONAL NOMBRE COMERCIAL NÚMERO FICHA: 1 POSOLOGÍA ASPECTO EXTERNO CADUCIDAD Nº LOTE Nº TOTAL PRESENTACIÓN 1 al día 0/1/0 Color blanco, redondos y pequeños 11/2017 BTAD1F2 841288 ADIRO Comprimidos gastrorresiste ntes 7 1 al día 1/0/0 Color amarillo pálido marcado con el logo del fabricante y por la otra cara T5 10/2015 00644E 714014 ZALDIAR Comprimidos con película 7 Opaca, blanca y con dos bandas doradas marcadas con 7767 y 200 01/2016 D1018513 871988 CELEBREX Cápsulas duras 7 1 al día 1/0/0 Ovalados y de color azul 02/2015 0768544R 7 1 al día 1/0/0 De color blanco, marcada con Pfizer en tinta negra y PGN 150 en el cuerpo 07/2015 0937082 7 ESOMEPRAZOL 686084 754754 Comprimidos gastrorresiste ntes LYRICA Cápsulas duras 1 al día 1/0/0
- 20. MEDICAMENTOS NO EMBLISTABLES 906214 VENORUTON Granulado para solución oral 1 al día 1/0/0 ELABORACIÓN BLISTER 1: Fecha y firma del farmacéutico Responsable. Sobres rojo y verde 02/2016 VALIDACIÓN BLISTER 1: Número total de medicamentos: 6 Número total de comprimidos: El aspecto externo coincide con el descrito. Fecha de caducidad correcta. Etiquetado Fecha y firma del farmacéutico responsable ED9876 7 ENTREGA AL PACIENTE: Fecha y firma del farmacéutico responsable
- 21. ETIQUETA PARA PEGAR EN EL BLISTER Paciente: Pepa Martínez Número SPD: 1 Fecha inicio: 16/09/13 Fecha de fin: 20/12/13 Condiciones especiales de conservación: Código nacional Nombre comercial Presentación 841288 ADIRO Comprimidos gastrorresistentes Aspecto externo Nº lote 1 al día 0/1/0 Blancos, redondos y pequeños BTAD1F2 1 al día 1/0/0 De color amarillo pálido 00644E 714014 ZALDIAR Comprimidos con película 1 al día 1/0/0 Opaca, blanca y con dos bandas doradas D1018513 871988 CELEBREX Cápsulas duras ESOMEPRAZOL 1 al día 1/0/0 Ovalados de color azul 0768544R 1 al día 1/0/0 De color blanca marcada con Pfizer en tinta negra y PGN 0937082 686084 754754 Comprimidos gastrorresistentes LYRICA Cápsulas duras Posología
- 22. MEDICAMENTOS NO EMBLISTABLES 906214 VENORUTON Granulado para solución oral 1 al día 1/0/0 Sobres rojos y verdes ED9876
- 23. MODIFICACIONES DEL TRATAMIENTO A LA SEMANA SIGUIENTE CÓDIGO NACIONAL NOMBRE COMERCIAL PRESENTACIÓN 841288 ADIRO Comprimidos gastrorresistentes 714014 ZALDIAR Comprimidos con película 871988 CELEBREX Cápsulas duras 686084 ESOMEPRAZOL 754754 LYRICA Comprimidos gastrorresistent es Cápsulas duras POSOLOGÍA ASPECTO EXTERNO CADUCIDAD Nº LOTE TOTAL 1 al día 0/1/0 Color blanco, redondos y pequeños 11/2017 BTAD1F2 7 3 al día 1/1/1 Color amarillo pálido marcado con el logo del fabricante y por la otra cara T5 10/2015 00644E 21 1 al día 1/0/0 Opaca, blanca y con dos bandas doradas marcadas con 7767 y 200 01/2016 D1018513 7 1 al día 1/0/0 Ovalados y de color azul 02/2015 0768544R 7 2 al día 1/0/1 De color blanco, marcada con Pfizer en tinta negra y PGN 150 en el cuerpo 07/2015 0937082 14
- 24. MEDICAMENTOS NO EMBLISTABLES 906214 VENORUTON Granulado para solución oral ELABORACIÓN BLISTER 1: 1 al día 1/0/0 Sobres rojos y verdes VALIDACIÓN BLISTER 1: ED9876 ENTREGA AL PACIENTE: Número total de medicamentos: 6 Número total de comprimidos: El aspecto externo coincide con el descrito. Fecha de caducidad correcta. Etiquetado Fecha y firma del farmacéutico Responsable. Fecha y firma del farmacéutico responsable Fecha y firma del farmacéutico responsable
- 25. ETIQUETA PARA PEGAR EN EL BLISTER Paciente: Pepa Martínez Fecha inicio: 16/09/13 Código nacional Nombre comercial Presentación 841288 ADIRO Comprimidos gastrorresistentes 714014 Número SPD: 1 Fecha de fin: 20/12/13 Posología Aspecto externo Nº lote 1 al día 0/1/0 Blancos, redondos y pequeños BTAD1F2 ZALDIAR Comprimidos con película 3 al día 1/1/1 De color amarillo pálido 00644E 871988 CELEBREX Cápsulas duras 1 al día 1/0/0 Opaca, blanca y con dos bandas doradas D1018513 686084 ESOMEPRAZOL Comprimidos gastrorresistentes 1 al día 1/0/0 Ovalados de color azul 0768544R 754754 LYRICA Cápsulas duras 2 al día 1/0/1 De color blanca marcada con Pfizer en tinta negra y PGN 0937082
- 26. MEDICAMENTOS NO EMBLISTABLES 906214 VENORUTON Granulado para solución oral 1 al día 1/0/0 Sobres rojos y verdes ED9876
- 27. CASO PRÁCTICO:
- 28. TRATAMIENTO DEL PACIENTE ADALAT OROS 30 mg 28 comprimidos ADIRO 100 mg 30 comprimidos ATORVASTATINA 10 mg 28 comprimidos ESCITALOPRAM 10 mg 28 comprimidos GREPID 75 mg 28 comprimidos PANTOPRAZOL 20 mg 28 comprimidos VELMETIA 50/1000 mg 56 comprimidos PRANDIN 2 mg 90 comprimidos EXELON PARCHES 9´5 / 24 horas 60 parches
- 29. NOMBRE: JUAN PÉREZ PÉREZ CÓDIGO NOMBRE COMERCIAL POSOLOGÍA NÚMERO FICHA: 2 ASPECTO EXTERNO CADUCIDAD NÚMERO LOTE NÚMERO TOTAL PRESENTACIÓN 1 al día 1/0/0 Redondos, convexos y de color rosa 04/17 BXGD161 7 750992 ADALAT OROS Comprimidos de liberación prolongada ADIRO Comprimidos gastrorresistentes 1 al día 1/0/0 De color blanco pequeños y redondos 10/17 BTADLPO 7 841288 ATORVASTATINA 1 al día 0/0/1 De color blanco y ranurados 03/16 NOILPPP 7 661067 Comprimidos oblongos 1 al día 1/0/0 De color blanco, redondos, biconvexos y ranurados 11/15 F51N1 7 663982 ESCITALOPRAM Comprimidos recubiertos 1 al día 1/0/0 De color rosa, redondos y biconvexos 05/14 F3191 7 663881 GREPID Comprimidos recubiertos PANTOPRAZOL Comprimidos 1 al día 1/0/0 De color naranja, ovalados y biconvexos 09/15 H1761 7 2 al día 1/0/1 De color rosa, ovalados y marcados con 515 en una cara 09/16 JIKOO9 14 661529 VELMETIA Comprimidos recubiertos PRANDIN Comprimidos redondos 3 al día 1/1/1 Blancos, redondos, convexos 04/17 06203898Q 21 829598 663751
- 30. MEDICAMENTOS NO EMBLISTABLES 660039 EXELON Parches transdérmicos 1 al día 1/0/0 Sobres 02/16 EDFLP ELABORACIÓN BLISTER 2: VALIDACIÓN BLISTER 2: Número total de medicamentos: 6 Número total de comprimidos: El aspecto externo coincide con el descrito. Fecha de caducidad correcta. Etiquetado ENTREGA AL PACIENTE: Fecha y firma del farmacéutico Fecha y firma del farmacéutico reponsable Fecha y firma del farmacéutico responsable Responsable
- 31. ETIQUETA PARA PEGAR EN EL BLISTER Paciente: Juan Pérez Pérez Fecha inicio: 1 Junio 2013 CÓDIGO NACIONAL Número SPD: 2 Fecha de fin: 1 Diciembre 2013 NOMBRE COMERCIAL PRESENTACIÓN POSOLOGÍA ASPECTO EXTERNO Nº LOTE 1 al día 1/0/0 Redondos, convexos y de color rosa BXGD161 750992 ADALAT OROS Comprimidos de liberación prolongada 1 al día 1/0/0 De color blanco, pequeños y redondos BTADLPO 841288 ADIRO Comprimidos gastrorresistentes ATORVASTATINA Comprimidos oblongos 1 al día 0/0/1 De color blanco y ranurados NOILPPP 661067 ESCITALOPRAM Comrpimidos recubiertos 1 al día 1/0/0 De color blanco, redondos, biconvexos y ranurados F51N1 663982 1 al día 1/0/0 De color rosa F3191 663881 GREPID Comprimidos recubierntos 1 al día 1/0/0 De color naranja H1761 663751 PANTOPRAZOL Comprimidos VELMETIA Comprimidos recubiertos 2 al día 1/0/1 De color rosa y ovalados JIK009 661529 3 al día 1/1/1 Blancos y redondos 829598 PRANDIN Comprimidos redondos 06203898Q
- 32. MEDICAMENTOS NO EMBLISTABLES 60039 EXELON Parche transdérmicos 1 al día 1/0/0 Sobres EDFLP
