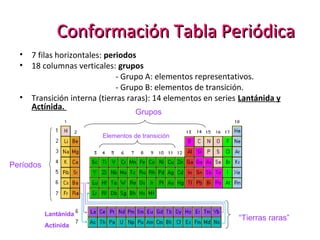
La tabla periódica está organizada en 7 períodos horizontales y 18 grupos verticales. Los grupos incluyen elementos representativos como los metales alcalinos y no metales, así como elementos de transición. Las propiedades químicas y físicas de los elementos, como el potencial de ionización y el tamaño atómico, varían de forma predecible a lo largo de los períodos y grupos debido a cambios en la configuración electrónica de los átomos.