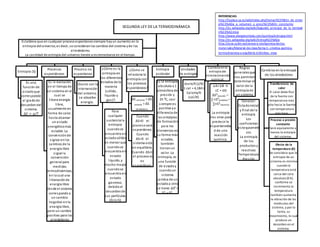
Segunda ley termodinámica entropía
- 1. SEGUNDA LEY DE LA TERMODINÁMICA Entropía (S) Es una función de estadoque corresponde al gradode desordendel sistema. ∆𝑆 = 𝑞/𝑇 Procesos espontáneos Es la evolución en el tiempode un sistema en el cual se libera energía libre, usualmente en forma de calor, hasta alcanzar un estado energéticomás estable. La convenciónde signos enlos cambios de la energía libre sigue la convención general para medidas termodinámicas, en la cual una liberaciónde energía libre desde el sistema corresponde a un cambio negativo enla energía libre, pero un cambio positivo para los alrededores Proceso no espontaneo Ocurre con la intervención del entorno, se absorbe energía. ¿Cómo es la entropía en los diferentes estados de la materia (sólido, líquido y gas)?. Para cualquier sustanciala entropía cuandose encuentra en estadosólido es menorque cuandose encuentra en estado líquido,y mucho mayor cuandose encuentra en estado gaseoso, debidoal desordende sus partículas. (G>L>S) ¿Cómo se relaciona la entropía con los procesos espontáneos? ΔS universo = ΔS sistema + ΔS alrededores Cuando ΔS>0 el procesoserá espontáneo. Cuando ΔS=0 el sistema está en equilibrio. Cuando ΔS<0 el procesono es espontáneo. Entropía estándar Es la entropía absoluta a 1 atmósfera de presión y 25 0 C, casi siempre es positiva ya diferencia de las entalpías de formación para los elementos en su forma más estable, también tienenun valor. La entropía, es una función de estadoy cuandoun sistema cambia de un estadoa otro se tiene: ∆S0 = S0 f – S0 i Unidades de entropía Joule/K(J/K) 1 cal = 4,184 J Caloria/K (cal/K) Cambios enla entropía del sistema (reacción química). aA+ bB → cC + dD ∆S0 reacción = ∑ nS0 produtos – ∑nS0 reactivos La entropía nos sirve para predecir la espontaneida d de una reacción química. Reglas generalesque nos permiten determinarel valor de la entropía en un sistema Conocer: Estadoinicial y final de la entropía Los coeficientes estequiométri cos La entropía de los productos y reactivos Temperatura Presión Cambios en la entropía de los alrededores Transferencia de calor El calor debe fluir de la fuente con temperatura más alta hacia la fuente con temperatura más baja. Proceso a presión constante Será equivalente a menos la entalpía del sistema. Efecto de la temperatura (K) Se considera que la entropía de un sistema es mínima cuando la temperatura está cerca del cero absoluto (0 K). conforme se incrementa la temperatura también aumenta la vibración de las moléculas del sistema, y por lo tanto, su movimiento, lo cual produce un desorden en el sistema. Establece que en cualquier procesoespontaneosiempre hayun aumento en la entropía deluniverso;es decir, se consideranlos cambios del sistema yde los alrededores. La cantidad de entropía del universo tiende a incrementarse en el tiempo. REFERENCIAS http://laplace.us.es/wiki/index.php/Variaci%C3%B3n_de_entro p%C3%ADa_a_volumen_y_presi%C3%B3n_constante http://es.wikipedia.org/wiki/Segundo_principio_de_la_termodi n%C3%A1mica http://www.elergonomista.com/quimica/entropia.html http://es.wikipedia.org/wiki/Entrop%C3%ADa http://ocw.uc3m.es/ciencia-e-oin/quimica-de-los- materiales/Material-de-clase/tema-5.-cinetica-quimica- termodinamica-y-equilibrio-ii/skinless_view