Primera ley de la termodinamica
•Descargar como DOCX, PDF•
0 recomendaciones•210 vistas
Primera ley de la termodinamica
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (19)
Ejercicio de primera ley sistemas abiertos (Taller den clases- Abril/2017)

Ejercicio de primera ley sistemas abiertos (Taller den clases- Abril/2017)
Solucion examen propuesto maquina frigorifica y bomba de color

Solucion examen propuesto maquina frigorifica y bomba de color
Destacado
Destacado (20)
Similar a Primera ley de la termodinamica
Similar a Primera ley de la termodinamica (20)
Más de Yesenia Jimenez
Más de Yesenia Jimenez (15)
Último
Último (20)
texto argumentativo, ejemplos y ejercicios prácticos

texto argumentativo, ejemplos y ejercicios prácticos
RETO MES DE ABRIL .............................docx

RETO MES DE ABRIL .............................docx
MAYO 1 PROYECTO día de la madre el amor más grande

MAYO 1 PROYECTO día de la madre el amor más grande
Heinsohn Privacidad y Ciberseguridad para el sector educativo

Heinsohn Privacidad y Ciberseguridad para el sector educativo
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx

TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx
Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf
Clasificaciones, modalidades y tendencias de investigación educativa.

Clasificaciones, modalidades y tendencias de investigación educativa.
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
Primera ley de la termodinamica
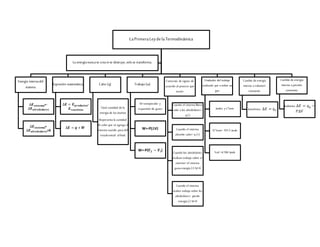
- 1. LaPrimeraLeydelaTermodinámica Energía internadel sistema ∆𝑬 𝒔𝒊𝒔𝒕𝒆𝒎𝒂=- ∆𝑬 𝒂𝒍𝒓𝒆𝒅𝒆𝒅𝒐𝒓𝒆𝒔 ∆𝑬 𝒔𝒊𝒔𝒕𝒆𝒎𝒂+ ∆𝑬 𝒂𝒍𝒓𝒆𝒅𝒆𝒅𝒐𝒓𝒆𝒔=0 Expresión matemática ∆𝑬 = 𝑬 𝒑𝒓𝒐𝒅𝒖𝒄𝒕𝒐𝒔- 𝑬 𝒓𝒆𝒂𝒄𝒕𝒊𝒗𝒐𝒔 ∆𝑬 = 𝒒 + 𝑾 Calor(q) Total cantidad de la energía de los átomos Representa la cantidad de calor que se agrega al sistema cuando pasa del estadoinicial alfinal. Trabajo(w) W=compresión y expansión de gases W=-P(∆V) W=-P(𝑽 𝒇 − 𝑽𝒊) Convenio de signos de acuerdo al proceso que ocurre Cuando el sistema libera calor a los alrededores= q(-) Cuando el sistema absorbe calor= q (+) Cuando los alrededores realizan trabajo sobre el sistema=el sistema gana energía (+) W<0 Cuando el sistema realiza trabajo sobre los alrededores= pierde energía (-) W>0 Unidades del trabajo realizado por osobre un gas Joules y L*atm 1L*amt= 101.3 Joule 1cal =4.184 Joule Cambio de energía interna a volumen constante Isométrico ∆𝐸 = 𝑞 𝑣 Cambio de energía interna a presión constante Isobárico ∆𝐸 = 𝑞 𝑝 − 𝑃∆𝑉 La energíanuncase creanise destruye, solose transforma.