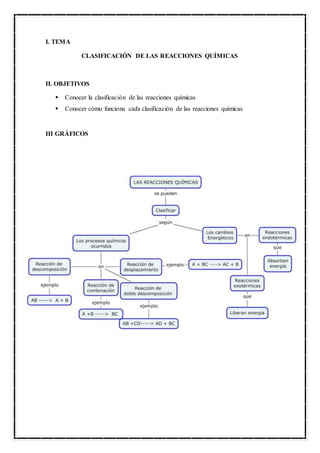
Clasificación de las reacciones químicas
- 1. I. TEMA CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS II. OBJETIVOS Conocer la clasificación de las reacciones químicas Conocer cómo funciona cada clasificación de las reacciones químicas III GRÁFICOS
- 2. IV MARCO TEÓRICO Las reacciones químicas se pueden clasificar así: 1.-REACCIONES DE ACUERDO CON EL PROCESO QUÍMICO OCURRIDO De acuerdo con el proceso químico ocurrido las reacciones químicas pueden ser: Reacciones de combinación o síntesis.- que son aquellas en las cuales dos o más sustancias reaccionantes se combinan para formar otra más compleja: 2H2(g) + O2(g) → 2H2O CaO(s) + H2O(l) → Ca(OH)2(ac) Reacciones de descomposición o análisis.- cuando un compuesto se descompone para formar otras sustancias más simples. 2HgO(s) → 2Hg(l) + O2(g) CaCO3(s) → CaO(s) + O2(g) Reacciones de desplazamiento o sustitución.- se presenta cuando hay un desplazamiento de uno o más átomos de un reaccionante, por uno o más átomos de otro elemento. En la mayoría de estas reacciones ocurre un desplazamiento de hidrógeno, de un metal o de un halógeno. 2Na(s) + H2O(l) → 2NaOH(ac) + H2(g) Fe(s) + CuSO4(ac) → FeSO4(ac) + Cu(s) Cl2(g) + 2NaI(ac) → 2NaCl(ac) + I2(s) A + B → C AB → A + B A + BC → AC + B
- 3. Reacciones de doble desplazamiento o intercambio o metátesis.- son aquellas en las cuales ocurre un intercambio entre los átomos o iones de los reaccionantes para formar otras sustancias más estables, generalmente se dan en soluciones acuosas y los átomos o iones participantes no cambian su número de oxidación al pasar de reactivos a productos. NaOH(ac) + HCl(ac) → NaCl(ac) + H2O(l) KCl(ac) + AgNO3(ac) → KNO3(ac) + AgCl(s) 2HCl(ac) + FeS(s) → FeCl2(ac) + H2S(g) 2.-REACCIONES DE ACUERDO CON LA ENERGÍA INVOLUCRADA De acuerdo con la energía involucrada las reacciones químicas se clasifican en: Reacciones exotérmicas.- que son aquellas que ocurren con desprendimiento de calor. En ellas la energía de los reactivos es mayor que la energía que poseen los productos, la combustión es un ejemplo de este tipo de reacciones C(s) + O2(g) → CO2(g) + Calor C(s) + O2(g) → CO2(g) + 94 Kcal A la cantidad de energía almacenada en los reactivos o en los productos se le llama entalpía (H), y a la diferencia entre la entalpía de los productos (Hp) y la entalpía de los reactivos (Hr) se le llama calor de reacción o cambio de entalpía (∆H).Por tanto: ∆H = Hp − Hr Como en una reacción exotérmica, la cantidad de energía almacenada en los productos es menor que la cantidad de energía almacenada en los reactivos, ∆H será negativo. C(s) + O2(g) → CO2(g) ∆H = −94 kcal. AB + CD → AD + CB
- 4. Reacciones endotérmicas.- son reacciones que absorben o requieren calor del entorno para llevarse a cabo. En estas la energía de los reactivos es menor que la energía de los productos. CaCO3 + calor → CaO + CO2 CaCO3 + 42.52 kcal → CaO + CO2 Puesto que en las reacciones endotérmicas la energía de los productos es mayor que la energía de los reactivos, ∆H es positivo: ∆H = Hp – Hr CaCO3 → CaO + CO2 ∆H = 45.2 kcal V CONCLUSIONES Se pudo conocer la clasificación de las reacciones químicas Se aprendió el proceso de cada clasificación de las reacciones químicas VI BIBLIOGRAFÍA Whitten, K. W., Gailey, K. D., Davis, R. E., Ortega, M. T. A., & Muradás, R. M. G. (1992). Química general. Madrid: McGraw-Hill.
