Tema 6 : principios básicos de la termodinámica
- 1. Tema 6: Principios de la termodinámica
- 2. 1. Definición La termodinámica es la parte de la física que se ocupa de las relaciones existentes entre el calor y el trabajo. El calor es una forma de energía, y al suministrar calor a ciertos dispositivos, estos lo transforman en trabajo mecánico útil, y en pérdidas por calor. Una máquina térmica es un dispositivo capaz de aprovechar el calor que recibe para producir trabajo útil. El calor que recibe (que se puede obtener de una reacción química, combustión) , lo absorbe un sistema, normalmente un fluido, que irá transformando parte de esa energía térmica en energía mecánica. El fluido realiza una serie de transformaciones termodinámicas, y en ellas se puede calcular el trabajo y también el rendimiento de la máquina.
- 3. 2.Sistema termodinámico Todo análisis termodinámico debe partir de la elección del sistema y de los alrededores, considerando sistema a la región del espacio (con paredes reales o imaginarias) sobre la que se analizarán los intercambios energéticos, mientras los alrededores se refieren a la región que interactúa sobre el sistema. ● Definimos pues: – Sistema abierto: Aquel en el que hay un posible intercambio de calor y materia con el exterior. – Sistema cerrado: Sólo es posible el intercambio de energía con el exterior. – Sistema aislado: no se puede intercambiar con el exterior materia o energía. ● Por ejemplo: Un sistema puede ser un motor térmico (particularmente los cilindros del motor) y los alrededores del sistema sería el medio ambiente exterior
- 4. ● Un sistema ( cuerpo) esta definido por una serie de variables físicas presión (P), volumen () , temperatura (T) y cantidad (n). El sistema intenta siempre estar en equilibrio, para ello tendrá que cambiar alguna de las variables físicas que lo definen cuando realiza o recibe trabajo . ● Cuando un cuerpo absorbe energía en forma de calor, aumenta su energía interna que se manifiesta en aumento de temperatura, para equilibrarse el sistema se dilata aumentando de volumen y realizando a su vez un trabajo) . ● Cuando aumento de volumen, el trabajo se considera positivo, y cuando disminuye el volumen, el es negativo. ● La ecuación de los gases ideales: P= Presión absoluta V= Volumen n= Moles de gas R= Constante universal de los gases ideales T= Temperatura absoluta P⋅ν=n⋅ℝ⋅T
- 5. ● Un sistema ( cuerpo) esta definido por una serie de variables físicas presión (P), volumen () , temperatura (T) y cantidad (n). El sistema intenta siempre estar en equilibrio, para ello tendrá que cambiar alguna de las variables físicas que lo definen cuando realiza o recibe trabajo . ● Cuando un cuerpo absorbe energía en forma de calor, aumenta su energía interna que se manifiesta en aumento de temperatura, para equilibrarse el sistema se dilata aumentando de volumen y realizando a su vez un trabajo) . ● Cuando aumento de volumen, el trabajo se considera positivo, y cuando disminuye el volumen, el es negativo. ● La ecuación de los gases ideales: P= Presión absoluta V= Volumen n= Moles de gas R= Constante universal de los gases ideales T= Temperatura absoluta P⋅ν=n⋅ℝ⋅T
- 6. 3.Principios de la termodinámica ● Primer principio: Básicamente, dice que hay dos formas de variar o modificar la energía interna de un sistema, o lo que es lo mismo, un sistema intercambia energía con elexterior de dos maneras diferentes: – En forma de calor, cuando existe una diferencia de temperatura. – En forma de trabajo. También se puede interpretar así: el calor suministrado se emplea en producir trabajo y en aumentar la energía interna de un sistema.
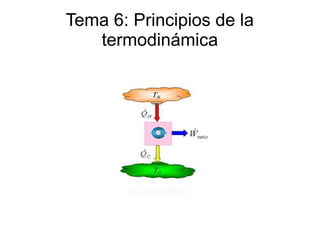
- 8. ● Segundo principio:Se puede enunciar de muchas formas según la situación, pero veamos su definición aplicado a un motor térmico. Según este principio, el calor se intercambia de forma natural y espontánea de un foco de calor más caliente (T1) a otro foco más frío ( a temperatura T2). Pues bien, una máquina cíclica que actúa entre dos focos a distintas temperaturas absorbe calor del foco caliente para convertir una parte en trabajo y el resto pasa al foco frío.
- 9. Cuanto menor sea el intercambio del calor del foco caliente al frío, más cantidad de calor se transforma en trabajo. En una máquina ideal, el calor cedido por el foco caliente (Q1) se transformaría totalmente en trabajo.
- 10. El rendimiento de un motor térmico sería: η = W/Q1 siendo W el trabajo útil realizado por la máquina Q1el calor que cede el foco caliente se puede deducir que, dado que Q1= W + Q2. η =( Q1−Q2 )/Q1 η = 1 – Q2/Q1 El segundo principio en las máquinas frigoríficas: Las máquinas frigoríficas funcionan a la inversa de las máquinas térmicas, es decir, absorben una cantidad de calor Q2 de un foco frío y ceden calor Q1 a un foco caliente, consumiendo trabajo, W. Para estas máquinas se define eficiencia como la relación entre el calor absorbido del foco frío y el trabajo necesario para ello. Eficiencia ε = Q2/W ε =Q2/(Q1−Q2) El trabajo lo suministra el compresor El mejor ciclo de refrigeración (el ideal) sería aquel que extrae la mayor cantidad de calor Q2 del foco frío a temperatura T2 con el mínimo de trabajo, e incluso, sin trabajo.
- 12. 4. Diagramas ● Ejemplo de diagrama P-V de un ciclo abierto : Partiendo de un estado (P1,V1), y llegando a un estado (P2,V2) , el trabajo realizado no tiene porqué ser el mismo”. Recuerda que este proceso es abierto, ya que los estados inicial (1) y finales (2) no coinciden . En este ejemplo si recorría el trayecto corto y directo (la curva) realizaba más trabajo (hay más area)que haciendo el recorrido en dos etapas. Sin embargo, la energía interna inicial y la energía interna final no van a depender del recorrido. Es decir: la variación de energía interna entre dos estados de un diagrama PV no depende del recorrido realizado, sino solamente de la posición del estado inicial y la posición del estado final.
- 13. ● Otro ejemplo: Partiendo de la ecuación de los gases perfectos, se pueden obtener las expresiones de trabajo realizado, calor absorbido y variación de energía interna del sistema. – Ecuación de estado de un gas ideal – p.V = n.R.T (P·V)/T=cte – Trabajo W = F.d = p.s.d = p. ΔV – Calor Q = m.Ce. ΔT = n. Ce. T Primer principio de la termodinámica Q = W + ΔU U = Q –W. – ΔU = variación de energía interna del sistema
- 14. 5. transformaciones del sistema termodinámico ● Proceso isocoro: Es aquel en el que el volumen del gas no varía a lo largo del proceso. En este caso, al no existir ni expansión ni compresión, no se realiza ningún trabajo, aunque la presión sí puede elevarse o disminuir. – En este caso WA-->B = 0. y según el primer principio: ΔU = Q
- 15. ● Proceso isobárico: Es aquel que se realiza a presión constante, es decir, que en todo momento, al pasar del estado A al estado B, la presión nunca varía. ● Si un gas pasa del estado inicial A hasta el estado final B,como en el de la gráfica, en este caso se da una expansión isobárica. El sistema ha realizado trabajo. ● WA-->B = PΔV
- 16. ● Proceso isotérmico: Es el que se realiza a temperatura constante en todo momento (T=cte) Si un gas pasa del estado inicial A hasta el estado final B como el de la gráfica, en este caso se da una expansión isotérmica. El sistema ha realizado trabajo, pero temperatura no ha variado. Debido a ello, la variación de energía interna es nula y en base al primer principio, podemos afirmar que ● ●
- 17. Proceso adiabatico: Es el proceso en el que no hay intercambio de calor entre el sistema termodinamico y el entorno (Q = 0). Si un gas pasa del estado inicial A, hasta el estado final B como el de la grafica, en este caso se da una expansion adiabatica. El sistema ha realizado trabajo y la temperatura ha descendido de TA hasta TB. En este caso, en base al primer principio, la energia interna del sistema es ΔU = -W
- 19. 6. ciclo de Carnot Carnot, en 1824, estableció el ciclo termodinámico ideal de una máquina térmica, de la que se podría obtener el máximo rendimiento teórico. Este ciclo se conoce con el nombre de “Ciclo de Carnot” y es un ciclo reversible formado por dos transformaciones isotérmicas y otras dos adiabáticas. Es un ciclo teórico e ideal que no puede realizar ninguna máquina térmica. Un ciclo reversible es aquel que puede realizarse en sentido horario y antihorario, y además la inversión se puede realizar en cualquier punto. Este ciclo es ideal, no real. Caracteristicas: 1. Actuan entre dos focos de calor, el caliente a temperatura T1 y el frio a temperatura T2 2. Se realizan en cuatro etapas o tiempos 3. Se considera reversible
- 22. Ejercicios Ejercicio 1: Dada la gráfica de la figura, que muestra un ciclo termodinámico, calcula el trabajo realizado por el sistema, suponiendo que el ciclo se realiza siguiendo el sentido de las agujas del reloj. Ejercicio 2: Un motor térmico de 120 CV consume 250.000 Kcal/h. Calcula el rendimiento del motor y el calor suministrado al foco frio. Ejercicio 3: Una máquina térmica que sigue un ciclo de Carnot toma 1100 Kcal del foco caliente a 380ºC y cede 500 Kcal al foco frio. Calcula: a) Rendimiento de la máquina b) Temperatura del foco frio
- 23. Ejercicio 4: Un motor térmico que describe el ciclo ideal de Carnot presenta un rendimiento del 45% cuando la temperatura ambiente es de 10ºC. Calcula: a) Temperatura del foco caliente b) ¿En cuántos grados se tendría que aumentar la temperatura del foco caliente para alcanzar un rendimiento del 60%? Ejercicio 5: Una máquina funciona según el ciclo reversible de Carnot entre dos focos a -3 ºC y 22 ºC y recibe desde el exterior una energía de 7000 KJ. Calcula: a) Eficiencia de la máquina cuando funciona como máquina frigorífica b) Eficiencia de la máquina cuando funciona como bomba de calor c) Energía térmica entregada al foco caliente d) Energía térmica absorbida desde el foco frio
- 24. 6. PAU Junio 2009/2010 De acuerdo al segundo principio de la termodinámica: a) Explique el fundamento del funcionamiento de los motores térmicos b) Explique el fundamento del funcionamiento de las máquinas frigoríficas 7 PAU Septiembre 2009/2010 Algunos productos hortofrutícolas pueden conservarse a una temperatura comprendida entre 6 y 12°C durante varios días hasta el momento de su consumo. Para conseguir que la temperatura de la cámara de un almacén sea constantemente 10°C se emplea una máquina térmica reversible que funciona de acuerdo al Ciclo de Carnot. Considerando que la temperatura media en el exterior es de 5°C en invierno, y 25°C en verano, calcule: a) La eficiencia de la máquina térmica en la época de invierno, y en la de verano b) El calor retirado de la cámara o aportado a la misma en cada estación, si la potencia calorífica utilizada es de 3 kW
- 25. 8. PAU Septiembre 2009/2010 Una máquina térmica funciona de acuerdo con un ciclo de Carnot perfecto entre las temperaturas T1 = 256ºC y T2 = 77ºC. Si el calor tomado del foco caliente es de 1350 J, determine: a) Rendimiento de la máquina. b) Calor aportado al foco frío. c) Trabajo realizado. d) Temperatura del foco frío si se desea conseguir un rendimiento del ciclo del 56%. 9. PAU Septiembre 2007/2008 Una máquina frigorífica de 1,5 kW de potencia mantiene una temperatura en su interior de 1°C, funcionando de acuerdo al Ciclo de Carnot. Considerando que el valor de la temperatura en el exterior de la máquina se mantiene constante en 18°C, calcule: a) El rendimiento de la máquina b) El calor eliminado por unidad de tiempo del interior del frigorífico c) El calor aportado por unidad de tiempo al exterior del frigorífico